Урок для 7 класу з теми "Багатоманітність речовин".
Клас: 7
Дата:
Урок
Тема. Хімічні формули речовин. Прості та складні речовини. Багатоманітність речовин. Лабораторний дослід № 4 «Ознайомлення зі зразками простих та складних речовин»
Мета: поглибити знання учнів про класифікацію речовин; сформувати поняття «проста речовина» і «складна речовина»; ознайомити учнів з початковою класифікацією простих речовин – металів та неметалів; навчити відрізняти металічні та неметалічні елементи за фізичними властивостями та їхнім положенням у Періодичній системі хімічних елементів; розвивати вміння аналізувати та використовувати набуті знання на уроках хімії; виховувати спостережливість.
Тип уроку: комбінований
Обладнання: Періодична система хімічних елементів; зразки речовин (сірка, залізо, вугілля, алюміній, вода, натрій хлорид, купрум(ІІ) оксид, цукор); кулестержневі моделі молекул, завдання для груп, індивідуальні завдання, завдання для ігор, портрет Лавуазьє.
Хід уроку
І. Організаційний етап .
- Сядьте відповідно до табличок:
Перша група – я все знаю і розумію,
Друга група – інколи потребую допомоги,
Третя група – я часто потребую допомоги.
ІІ. Актуалізація опорних знань.
Перевірка домашнього завдання.
Бесіда
1. Назвіть одиниці вимірювання маси атома?
2. Записати атомні маси даних елементів (інтерактивна вправа «Жаба»)
3. Що показує хімічна фомула речовини?
ІІІ. Мотивація навчальної діяльності
Чи відрізняються формули речовин і чим саме?
O2 N2 Na S8 I2 O3 Al C
NaCl CO2 H2O CH3COOH CH3OH CaC2 HNO2
Учні роблять висновок.
Повідомлення теми уроку та завдань уроку.
- Тож сьогодні ми продовжимо знайомитись з періодичною системою хімічних елементів Д.І. Менделєєва, навчимося розрізняти речовини та прогнозувати фізичні властивості лише за записом формули молекули.
IV. Вивчення нового матеріалу .
- Що ж таке формула молекули? Формула молекули – це умовний запис складу речовини за допомогою хімічних елементів та індексів. Формула молекули містить якісний та кількісний склад. Читаємо формулу відповідно – аш два о.
- Прочитати формули з попереднього слайду.
Розповідь вчителя
В природі існує багато речовин, з якими ми безпосередньо уже зустрічалися. Це речовини у вигляді газів, рідин або твердих тіл. Завдяки тому, що атоми здатні сполучатися між собою нас оточує велике розмаїття речовин. Серед них є як прості, так і складні речовини.
Речовину, утворену одним хімічних елементом, називають простою.
Речовину, утворену двома або більшою кількістю елементів, називають складною речовиною.
- Подивіться на реактиви, що у вас на столах. Чим вони відрізняються? Можете їх класифікувати? Запропонуйте свої варіанти.
Прості речовини поділяють на метали і неметали. Хімічні елементи-метали утворюють прості речовини – метали, а хімічні елементи-неметали утворюють прості речовини – неметали. Таку класифікацію простих речовин запропонував наприкінці XVIII ст. видатний французький учений А.Л.Лавуазьє(портрет).
Метали представляють собою кристалічні речовини немолекулярної будови. Вони відрізняються від решти речовин особливим «металічним» блиском. За звичайних умов тверді (лише ртуть є рідиною), добре проводять електричний струм і теплоту, мають здебільшого досить високі температури плавлення (понад 500 °С), багато з них є пластичними (їх можна кувати, витягувати з них дріт).
Неметали відрізняються від металів передусім відсутністю металічного блиску. Лише йод, графіт, кристалічні бор і силіцій мають такий блиск. Неметали не проводять електричний струм (виняток — графіт). За звичайних умов частина неметалів перебуває у газоподібному стані, інші є твердими і тільки бром – рідиною.
Завдання 1. Розгляньте малюнки. Визначіть , до яких речовин вони належать, спробуйте скласти формули речовин за кулестержневою будовою з набору атомів, запишіть формули молекул, спрогнозуйте фізичні властивості.
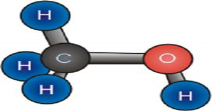
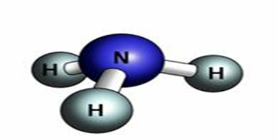
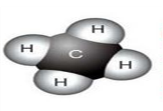
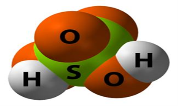


Більшість складних речовин мають молекулярну будову. Тому температури їх плавлення і кипіння невисокі. Частина таких речовин має запах. Молекулярною сполукою є вода. Вона складається з двох атомів Гідрогену і одного атома Оксигену.
До складних речовин також відносяться оцтова кислота, питна сода, цукор, кухонна сіль. Фізкультхвилинка.
Читаю прості та складні речовини, учні плескають в долоні тільки тоді, коли називаються складні речовини: сульфур (6) оксид, сірка, нітратна кислота, фосфор (5) оксид, гелій, залізо, літій оксид, мідь, натрій нітрат, магній, кисень, хлор, барій фосфат, хлоридна кислота, йод, олово.
Завдання 2 (робота в групах). Виконання лабораторного досліду № 4 за зошитом з друкованою основою по групах за рівнем підготовленості.
- Оголошення теми та мети досліду.
- Інструктаж з техніки безпеки за картками, зробленими гуртківцями:
- Заборонено брати речовини руками;
- Заборонено куштувати реактиви на смак;
- Заборонено залишати неприбраними розсипані або розлиті реактиви;
- Використовуйте шпатель для твердих речовин.
3. Завдання досліду.
V. Узагальнення та систематизація знань .
Гра «Мозаїка» - з поданих частин тексту скласти класифікацію речовин.
VI. Підведення підсумків уроку.
Учні доповнюють речення: «Сьогодні на уроці мені запам’яталось…»
VII. Домашнє завдання :
Опрацювати параграф 12, 9, задача алхіміка для групи


про публікацію авторської розробки
Додати розробку
