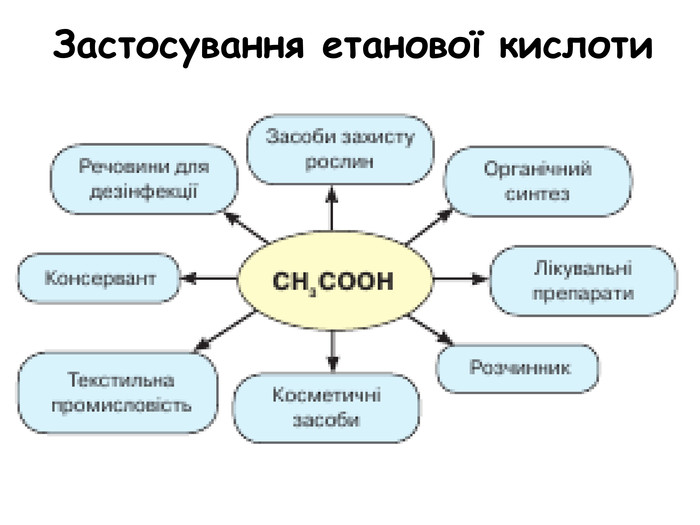
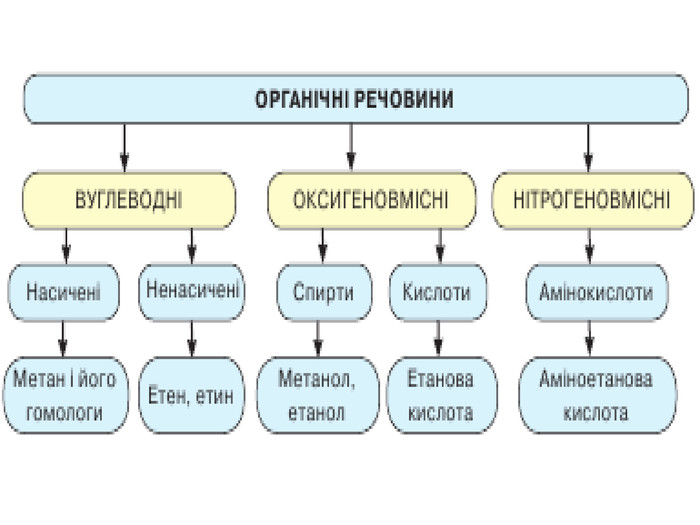
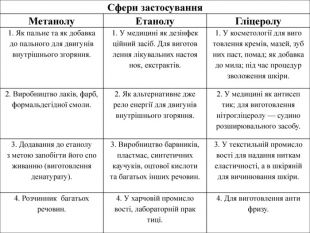
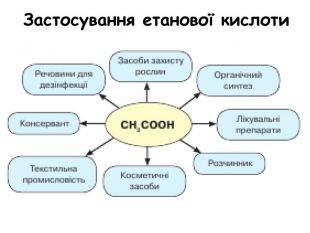
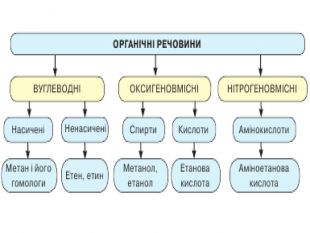
Склад, властивості, застосування окремих представників оксигеновмісних (метанол, етанол, гліцерол, етанова кислота).
Про матеріал
Презентація до уроку "Склад, властивості, застосування окремих представників оксигеновмісних (метанол, етанол, гліцерол, етанова кислота)" Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Дякую
-


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку