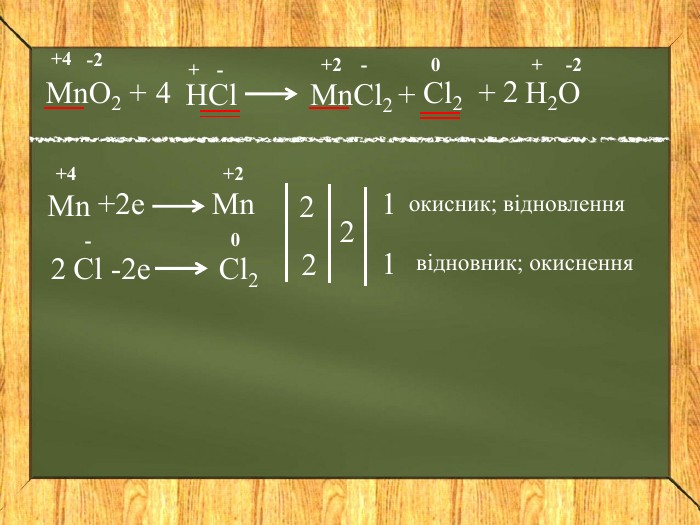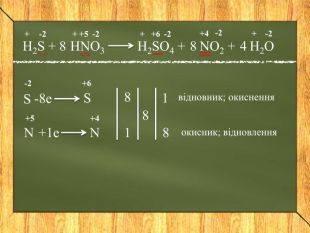Складання рівнянь окисно-відновних реакцій
Про матеріал
Розробка містить приклади складання окисно відновних реакцій. Дана презентація стане в нагоді під час удосконалення навичок складання реакцій даного типу Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку