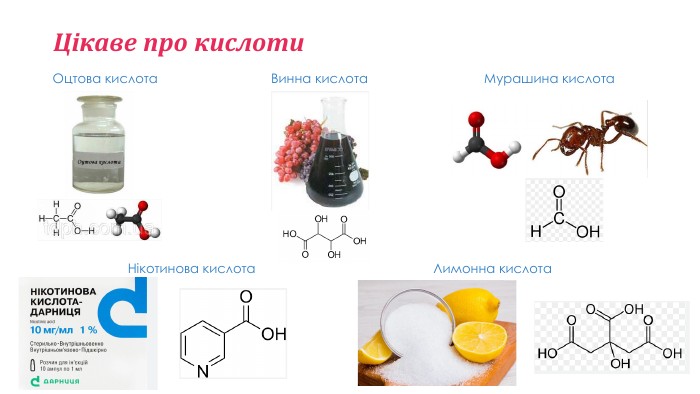
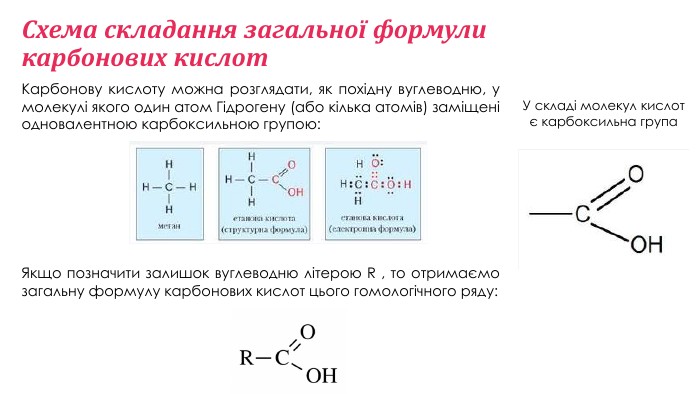
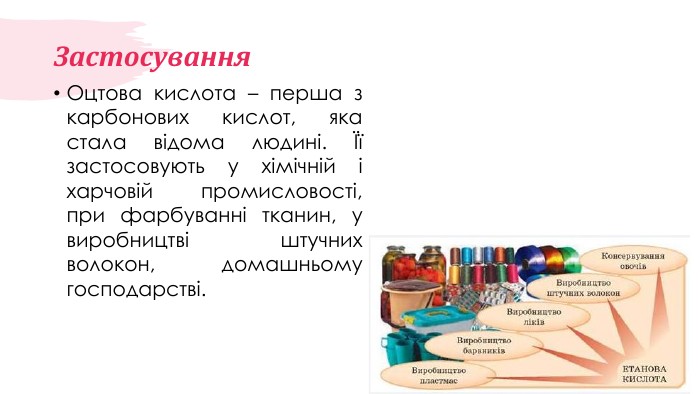
Карбонові кислоти. Етанова (оцтова) кислота
Про матеріал
Карбонові кислоти. Етанова (оцтова) кислота. Будова моллекули. Фізичні властивості. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку