Тема : Білки: склад і будова, фізичні та хімічні властивості. Біологічна роль білків.
План конспект уроку біології
Учитель Рябчук Валентина Іванівна
Дата ____/___/____ Клас 9____
Тема : Білки: склад і будова, фізичні та хімічні властивості. Біологічна роль білків.
Мета:
навчальна:формувати поняття про білки як природні полімери, первинну, вторинну, третинну й четвертинну структури білкових молекул; ознайомити учнів з фізичними й хімічними властивостями білків на прикладі гідролізу й денатурації; показати кольорові реакції білків як якісні реакції на білки.
виховна: поглибити знання про необхідність білків в житті організмів;
розвиваюча: викликати зацікавлення; встановити міжпредметні зв'язки у викладі даного матеріалу; сформувати і розвинути логічне мислення в учнів, (а також вміння формулювати висновки та порівнювати)
Обладнання й матеріали: штатив з пробірками, яєчний білок, молоко, розчин, натрій гідроксиду, купрум (II) сульфату, нітратна кислота, пробірко тримач, спиртівка, роздатковий матеріал,NаОН, СuS04.
Демонстрації:відеофільм «Структури білка» реакції денатурації.
Лабораторні досліди:
1.Дослідження розчинності білків;
2.Кольорова реакція білків (біуретова та ксантопротеїнова реакції).
Тип уроку: урок вивчення нового матеріалу.
Міжпредметні зв'язки: біологія, історія, фізіологія харчування, товарознавство та кулінарія.
Внутрішньопредметні зв'язки: неорганічна хімія (колоїдні розчини, каталізатор).
Методи та прийоми: бесіда, розповідь з елементами лекції, робота із роздатковим матеріалом, демонстрація дослідів, метод «опитування експертів», метод створення проблемних ситуацій, розгадування кросворда, завдання на усвідомлення наявних знань і конструювання нових, дидактична гра.
Девіз уроку(на дошці): «Той, хто серйозно прагне до пізнання істини, не повинен обирати якусь одну науку, бо всі вони знаходяться у взаємному зв'язку одна із одною.» філософ Рене Декарт
Структура уроків, основний зміст і методи роботи.
- Організаційна частина
ІІ. Актуалізація опорних знань учнів
(Проведення дидактичної гри з взаємоперевіркою )
Варіант 1
|
1. Назвіть речовини , яка має формулу
|
бутан |
а |
|
амінооцтова кислота |
к |
|
|
анілін |
г |
|
|
оцтова кислота |
у |
|
|
2. Який це зв’язок
|
водневий |
о |
|
йонний |
р |
|
|
металічний |
щ |
|
|
пептидний |
е |
|
|
3. NН2 - це |
гідроксильна група |
с |
|
карбоксильна |
т |
|
|
аміногрупа |
р |
|
|
карбонільна |
а |
|
|
4. Карбоксильна група є носієм … властивостей |
кислотних |
а |
|
основних |
м |
|
|
амфотерних |
н |
|
|
фізичних |
ш |
|
|
5. Амінокислоти за фізичними властивостями |
кристалічні речовини |
т |
|
гази |
ц |
|
|
рідини |
д |
|
|
6. Амінокислоти є мономерами |
вуглеводів |
ф |
|
жирів |
л |
|
|
білків |
и |
|
|
спиртів |
с |
|
|
7. В молекулах амінокислот наявні функціональні групи |
1 |
и |
|
2 |
н |
|
|
3 |
р |
|
|
4 |
ж |
Варіант2
|
1.Вкажіть назву речовини , яка має формулу
|
етан |
б |
|
α-амінопропанова кислота |
і |
|
|
ацетилен |
л |
|
|
пропанова кислота |
к |
|
|
2. Аміногрупа є носієм … властивостей
|
кислотних |
и |
|
основних |
м |
|
|
амфотерних |
н |
|
|
фізичних |
о |
|
|
3. СООН- це |
гідроксильна група |
р |
|
карбоксильна |
с |
|
|
аміногрупа |
е |
|
|
карбонільна |
т |
|
|
4. Найпростіша з амінокислот |
амінобутанова |
п |
|
амінокапронова |
о |
|
|
амінооцтова |
у |
|
|
амінопропіонова |
д |
|
|
5. При утворенні пептидного зв’язку виділяється |
вуглекислий газ |
щ |
|
вода |
л |
|
|
кисень |
в |
|
|
водень |
ж |
|
|
6. Амінокислоти є «цеглинками» з яких побудовані |
вуглеводи |
ф |
|
жири |
п |
|
|
білки |
і |
|
|
спирти |
к |
|
|
7.Український біохімік який вперше висловив думку про амінокислотний склад білків |
О.М.Бутлеров |
р |
|
В.І.Вернадський |
а |
|
|
М.А.Бунге |
с |
|
|
І.Я. Горбачевський |
н |
І варіантВідповідь: Креатин
ІІваріантВідповідь: Інсулін
Діти, а про що вам говорять ці два слова. Що ви знаєте про інсулін? Кератин?
III. Мотивація навчальної діяльності
Такі різні речовина, а спільним між ними є речовина про яку голландський біохімік ГеррітМльдер 1838 році писав «У всіх рослинах і тваринах присутня ця речовина, яка є найважливішою зі всіх речовин живої природи і без якої життя було б на нашій планеті неможливим…»
Цією речовиною є білок.
ІV. Повідомлення теми і завданьуроку.
V. Вивчення нового матеріалу
Ще Ф. Енгельс давно сказав такі слова: «Життя є спосіб існування білкових тіл». В чому ж полягає таємниця життя і яку роль в усіх життєвих процесах відіграють білки? Чим вони представлені, який в них склад, будова і властивості сьогодні протягом уроку будемо з’ясовувати.
Діти вам до дому було знайти цікаві факти, інформацію про білок. Хто справився з даним завданням (повідомлення учнів)
Символом зародження життя вважалося завжди яйце. Тому, білок пташиного яйця, дав назву всьому класові білків хоча їх ще і називають протеїнами (що в перекладі означає перший)
Білки це високомолекулярні органічні сполуки, полімери, мономерами яких є α - амінокислоти, зв'язані між собою пептидним зв'язком.
Білки обов'язково містять елементи С, Н, NО, майже завжди S, часто Р, рідше Fе, Сu, Mg та ін.
Які ж молекулярні маси білка? Для того щоб це з’ясувати давайте розважимо задачку .
В одному з білків міститься 0, 32 % S. Якою є його молекулярна маса, якщо припустити, що в молекулі лише 1 атом S.
Ми сказали що білки це полімерні сполуки. А які ще полімерні сполуки ми з вами вчили? Але формули і крохмалю, і целюлози ми можемо записати (-С6Н10О5-). А чи можемо ми записати загальну формулу білка?
Яка ж їх будова?
Жодну речовину хіміки не вивчали так довго, як білки, перш ніж вдалося розкрити таємницю їхньої будови. І вперше висловив думку, що білки складаються з амінокислот український учений Іван Горбачевський, який між іншим родом з Тернопільської області
Перегляд відеофільму«Рівні структурної організації білків».
Структура білка
Первинна Вторинна Третинна Четвертинна
З'ясувавши будову білків розглянемо їх властивості.
Пам’ятаємо про правила техніки безпеки
- Чи розчинні білки у воді ?
Виконання досліду до яєчного білка у співвідношенні 1:1 добавляємо води
За фізичними властивостями білки є нерозчинні у воді й такі, що утворюють колоїдні розчини.
- Під впливом різних фізико-хімічних чинників структура та властивості білків можуть змінюватись. Відбувається руйнування вторинної, третинної та четвертинної структур – денатурація. Ця зміна може носити тимчасовий або постійний характер, але і втому і в іншому випадку амінокислотна послідовність білка (первинна структура) залишається незмінною.Іноді денатурований білок може назад набути своєї форми.
Учитель демонструє «Денатурація білка принагріванні».
Розчин білка курячого яйця піддають нагріванню. При цьому денатурований білок випадає в осад.
Фактори що зумовлюють денатурацію білків:
- нагрівання;
- сильні кислоти та луги;
- важкі метали;
- органічні розчинники;
Використання спирту як дезинфікуючого засобу базується на тому, що він спричиняє денатурацію білка будь-яких присутніх бактерій.
- Гідроліз білка
Гідроліз веде до розпаду поліпептидів з утворенням амінокислот. Такий процес відбувається у шлунково-кишковому тракті.
Розклад білків під дією мікроорганізмів призводить до утворення не амінокислот, а амоніаку, сірководню, фенолу та ін. речовин із неприємним запахом. Його поява свідчить про те, що відбувається процес розкладу(гниття) білка.
- Для доказу наявності білка в розчинах використовують якісні кольорові реакції:(Вчитель проводить інструктаж з безпеки життєдіяльності
Лабораторний дослід
Біуретовареація
Ксантопротеїнова
Робота в група
Фізіолог харчування:
Товарознавець:
Кулінар –технолог
Біологи
Вчитель хімії:
Ви говорили про функцію білка таку як каталітична. В чому її суть? Хто такі ферменти?
Півстоліття тому король Данії Христіан Х вручав відомому біохіміку Ландерстрем-Лангу високу наукову нагороду – медаль Ерстера за дослідження у вивченні будови та властивостей білків і ферментів. Після урочистої церемонії його екселенція попросив ученого розповісти про ферменти. Той повідав таку історію:
(Вчитель розповідає історію вручення нагороди відомому біохіміку Ландерстрем-Лангу).
“…Помирав старий араб. Усе його багатство складалося з 17 прекрасних білих верблюдів. Він зібрав своїх синів і оголосив їм останню волю: ”Старший, опора сім’ї, повинен одержати після моєї смерті половину верблюдів. Середньому заповідаю третину, але мій найменший, улюблений мусить отримати одну дев’яту частину отари”. Поховавши батька, три брати почали ділити тварин. Але виконати волю батька їм ніяк не вдалося, бо вони не могли поділити 17 верблюдів на половину, на 3 і 9 частин. Саме тоді через пустелю проходив дервіш. Бідний він вів з собою чорного верблюда, навантаженою книгами. Брати звернулися до нього за допомогою і той сказав: ”Я дарую вам свого верблюда, а ви спробуйте розділити багатство. У братів стало 18 верблюдів, і тоді всі проблеми зникли. Старший син одержав половину верблюдів - 9, середній - 6, молодший - 2. Після поділу виявилося одна тварина зайвою – і дервіш сказав:”Віддайте мені назад мого верблюда за те, що я допоміг розділити багатство. Інакше мені доведеться самому тягнути книги через пустелю”.
- Ось цей верблюд, - закінчив розповідь учений, - подібний до ферменту. Він зробив можливим такий процес, який без його участі був би немислимий, а сам залишається без змін.
V. Узагальнення та систематизація знань Фронтальна бесіда.
- Знаючи властивості білків поясніть чому висока температура небезпечна для людського організму;
2. Я придбала нитки на базарі, мене запевнили що вони з вовни, як це перевірити?
3. Як довести що в молоці є білок?
VI. Закріплення набутих знань (дебрифінг)
Для встановлення зворотного зв'язку, закріплення, повторення та систематизації вивченого учнями пропонується закінчити складати хімічний словник (письмово спочатку простим олівцем, а потім правильно - ручкою), а також розв'язати кросворд.
Кросворд «Білки»
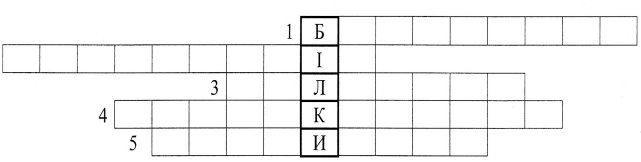
2
По горизонталі:
- Як називається кольорова якісна реакція на білки з Сu(ОН)2
- Білок що переносить кисень до тканин.
- Високомолекулярні сполуки.
- Речовини з яких складаються білки.
- Як називається зв'язок між залишками амінокислот.
VII. Підбиття підсумків уроку
VIII. Домашнє завдання
Опрацювати § 33. Вправа 2, 3
Вправа 6 (ІVрівень)
Творче завдання:
Підготувати повідомлення за темами:
- Ферменти – біокаталізатори хімічних реакцій.
- Їжа – джорганізмуерело будівельного матеріалу.
-
Дуже дякую! Цікавий урок! Сама хочу на такому побувати!


про публікацію авторської розробки
Додати розробку
