Уро - Практична робота з хімії "Виявлення органічних сполук у харчових продуктах"
Клас__________ Дата______
Урок
Тема: Практична робота №5 Виявлення органічних сполук у харчових продуктах
Мета: освоїти основні методи виявлення органічних сполук у харчових продуктах та ознайомитися з основним призначенням їхнього використання.
Реактиви та обладнання (поруч із назвами речовин запишіть відповідні формули): розчини натрій гідроксиду NaOH купрум(ІІ) сульфату CuSO4, глюкози C6H12O6, сахарози C12H22O11, лакмусу, йодна настоянка, відвар рису, кондитерський виріб (із умістом у ньому гліцеролу, наприклад, жувальна гумка, де гліцерол використовують як замінник цукру, солодкі газовані напої, тістечка, де гліцерол (харчова добавка Е442) використовують як стабілізатор або інші харчові продукти з цією харчовою добавкою), розсіл сквашених (маринованих) огірків, штатив із пробірками, нагрівний прилад, пробіркотримач.
3. Заповніть таблицю.
|
Що робили |
Що спостерігали |
|
Дослід 1. Дослідіть, у якій з двох пробірок міститься розчин глюкози, а в якій — сахарози. |
|
|
Добули з NaOH і CuSO4 свіжий купрум (ІІ) гідроксид (синій осад) і добавили його у дві пробірки, гарно струсили |
В одній з пробірок утворився розчин блакитного кольору, в іншій — змін не відбулося (осад залишився). |
|
Висновок: |
|
|
Дослід 2. Доведіть, що клейстер відвареного рису містить крохмаль. |
|
|
До зціженої води з відвареного рису додаємо розчин йодної настойки |
Утворився синій колір досліджуваної суміші. |
|
Висновок: швидко засвоюється організмом, є високоенергетичним вуглеводом (гідроліз у шлунку — утворення глюкози). |
|
|
Дослід 3. Дослідіть наявність гліцеролу в кондитерському виробі. |
|
|
Добули з NaOH і CuSO4 світлий Cu(OH)2 і додали його до вмісту досліджуваного кондитерського виробу |
Спостерігаємо розчин яскраво-блакитного кольору. |
|
Висновок: гліцерол добавляють до кондитерських виробів як замінник цукру, або харчова добавка E442, як стабілізатор. |
|
|
Дослід 4. Підтвердіть, що у розсолі від сквашених (маринованих) огірків є органічна кислота. |
|
|
До розсолу додали кілька крапель лакмусу і розчин набув червоного кольору. |
|
|
Висновок: кислота виконує функцію консерванта, який збільшує термін придатності продукту. |
|
4. Сформулюйте висновок. У висновку дайте відповідь на запитання: яка біологічна роль білків, жирів, вуглеводів?
Білки, жири і вуглеводи є основними речовинами життєдіяльності нашого організму. Білки є будівельним матеріалом структур організму і ферментів; жири і вуглеводи — основа енергетичної функції організму і процесів у організмі.
Реактиви: хліб, йодна настойка, дистильована вода; молоко, розчин етанової кислоти з масовою часткою 10 %, розчин фенолфталеїну, розчин лугу концентрацією 0,1 моль/л, нітратної кислоти.
Обладнання: хімічні стакани, мірний циліндр, конічна колба, піпетка, лійка, фільтрувальний папір, окуляри й гумові рукавички.
Мета роботи: навчитися виявляти органічні сполуки у харчових продуктах.
Хід роботи
Дослід 1. Виявлення крохмалю у хлібі
Приготуйте йодну воду. Для цього в стакані холодної води розчиніть 1 краплю настойки йоду. Далі на шматочок білого хлібу нанесіть 1-2 краплі йодної води. Що спостерігаєте?
Протягом 5 хв пережовуйте такий самий шматочок білого хліба. Помістіть отриману кашицю на предметне скло та знову нанесіть 1-2 краплі йодної води. Запишіть одержаний результат.
У першому шматочку хліба міститься нерозчинний крохмаль, тому спостерігається відсутність будь-яких змін із забарвленням йоду. Під час жування хліба (другий шматочок) під дією слини відбувається поступове перетворення крохмалю на глюкозу, а тому і зміна забарвлення йоду від синього через синьо-фіолетовий до оранжевого:
![]()
Дослід 2. Виявлення білка в молоці
У хімічний стакан налийте 5 мл свіжого молока, додайте 10 мл дистильованої води та 1 мл розчину етанової кислоти з масовою часткою 10 %. Перемішайте суміш. Утворюються пластівці.
Дайте осаду відстоятися, відфільтруйте рідину. Осад, що залишився на фільтрувальному папері, промийте дистильованою водою та висушіть у сушильній шафі за температури 50-60 °С. Потім нанесіть на осад кілька крапель концентрованої нітратної кислоти (працюйте в окулярах і гумових рукавичках!). Поява жовтого забарвлення осаду під дією нітратної кислоти свідчить про наявність у ньому білка.
Дослід 3. Визначення кислотності молока
Показником якості молока є його кислотність. У процесі зберігання кислотність молока зростає, оскільки під дією бактерій
утворюється молочна кислота
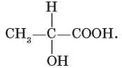
Вона також
утворюється під час квашення капусти, приготування солінь, виконуючи при цьому роль консерванту, через те що здатна перешкоджати утворенню гнилісних бактерій.
У конічну колбу піпеткою внесіть 10 мл молока, додайте 20 мл дистильованої води, 3 краплі спиртового розчину фенолфталеїну й ретельно збовтайте суміш.
Заповніть бюретку розчином лугу концентрацією 0,1 моль/л. Поступово доливайте розчин до суміші з молоком, безперервно збовтуючи її до появи слаборожевого забарвлення, яке не зникає протягом 1 хвилини.
Обчисліть, який об’єм розчину лугу пішов на нейтралізацію молочної кислоти у 100 мл молока. Якщо молоко свіже, то на нейтралізацію має піти 16-19 мл лугу.


про публікацію авторської розробки
Додати розробку
