Урок - проект на тему "Білки"
Про матеріал
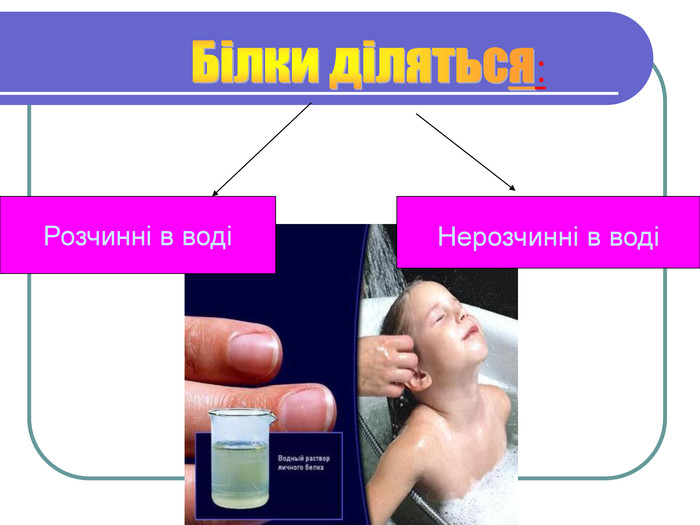
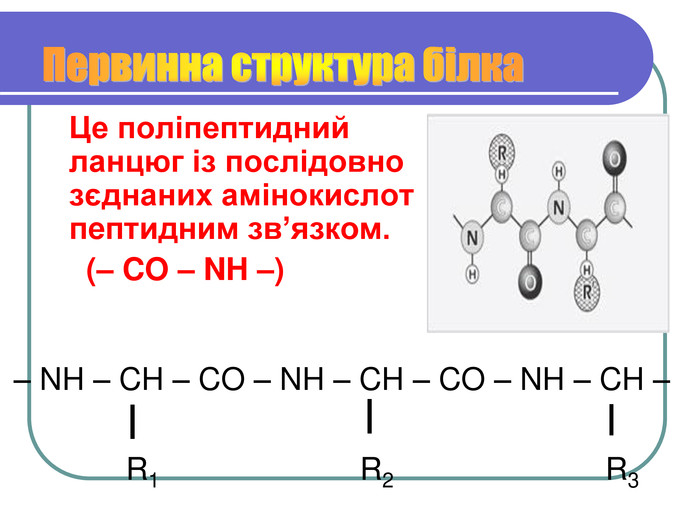
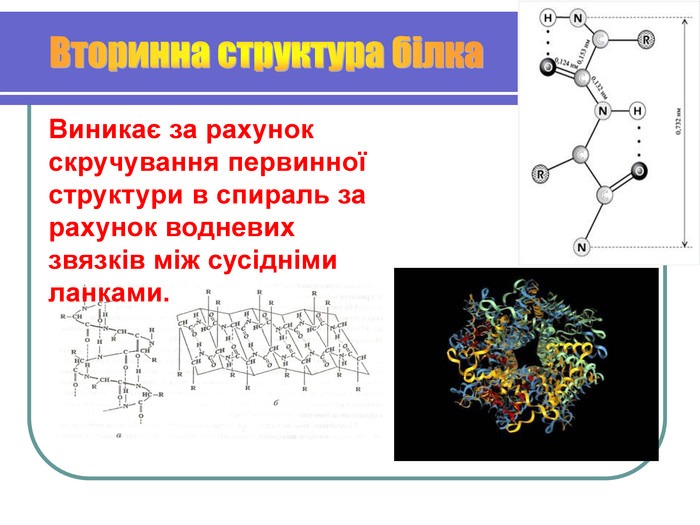
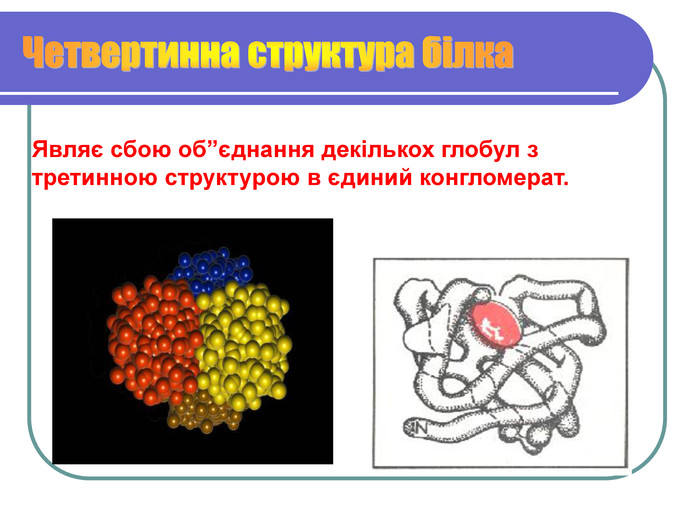
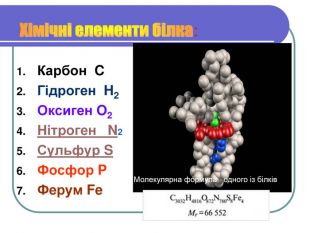
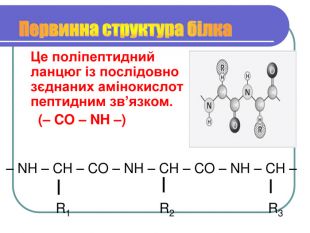
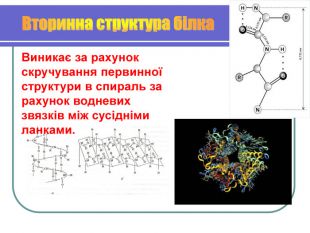
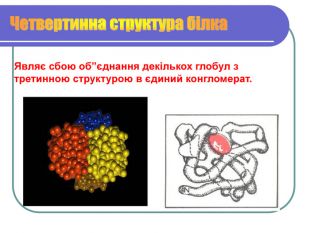
Вивчити будову білкової молекули
Утворення зв'язків
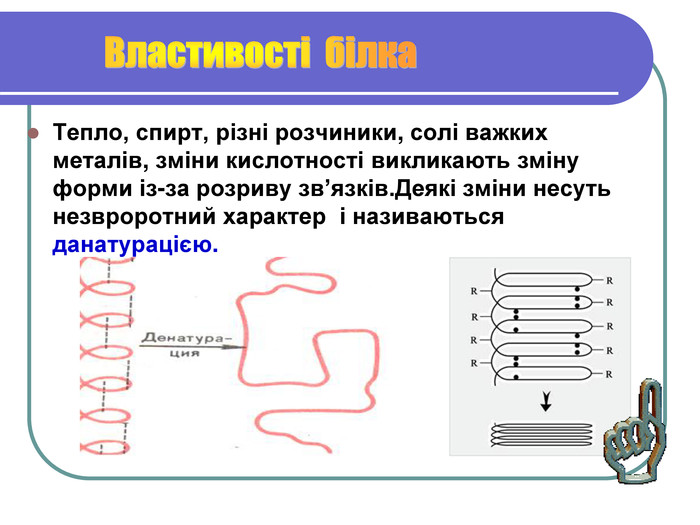
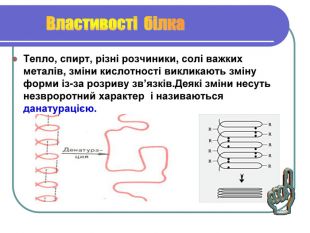
Фізичні і хімічні властивості
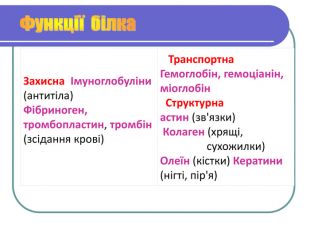
Значення для людини
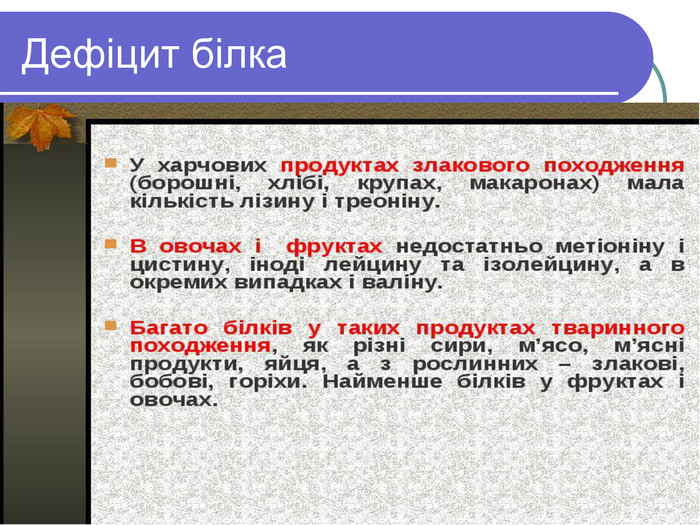
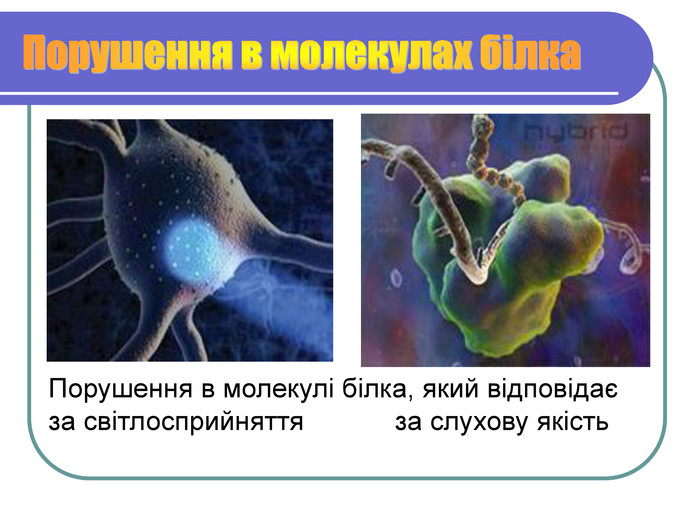
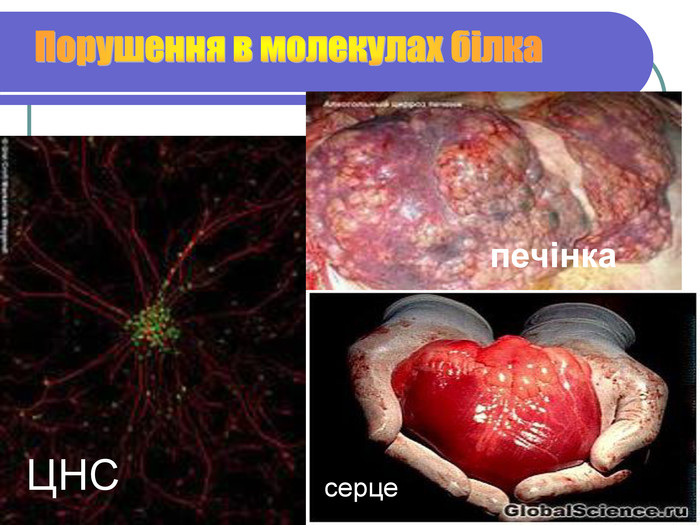
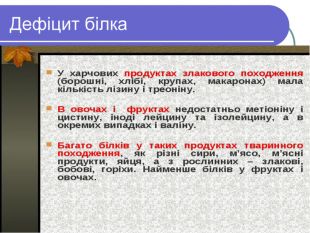
Хвороби зв'язані з відсутністю білків
Норми вживання білка
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Хороша робота! Дякую!
ppt
До підручника
Хімія (профільний рівень) 10 клас (Буринська Н.М. та інші)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку