Урок "Багатоманітність речовин. Прості й складні речовини. Метали й неметали. Металічні та неметалічні елементи, їх розміщення в періодичній системі"
Урок
Клас. 7
Тема. Багатоманітність речовин. Прості й складні речовини. Метали й неметали. Металічні та неметалічні елементи, їх розміщення в періодичній системі.
Мета уроку:
освітня: сформувати поняття про прості та складні речовини; ознайомити з поділом простих речовин на метали і неметали; навчити їх розрізняти, а також визначити металічні і неметалічні елементи за їх розміщенням у Періодичній системі; показати відмінність понять «проста речовина» та «хімічний елемент», «складна речовина», пояснити причину багатоманітності речовин; розвивати вміння й навички учнів описувати фізичні властивості речовин і порівнювати їх; виховувати інтерес до вивчення хімії на основі хімічного експерименту.
розвивальна: формувати навички учнів користуватися періодичною системою як джерелом інформації, складати формули сполук;
виховна: формувати стійкий інтерес до вивчення предмета.
Обладнання: Періодична система хімічних елементів Д. І. Менделєєва, моделі молекул.
Матеріали: зразки простих речовин (сірка, вугілля, залізо, алюміній), зразки складних речовин (вода, натрій хлорид, купрум(ІІ) оксид, цукор), пробірки, пробіркотримач, спиртівка, сірка, залізний порошок, магніт.
Базові поняття та терміни: атоми, молекули, хімічний елемент, прості та складні речовини, суміш, метали і неметали.
Тип уроку: комбінований.
Методи та прийоми: словесні: бесіда, розповідь; наочні: демонстрації; практичні: лабораторний дослід, самостійна робота; репродуктивні; проблемно-пошукові; логічні; дослідницькі.
Хід уроку
І. Організаційний етап
Добрий день, дорогі діти! Не поспішайте сідати, бо для цього вам потрібно сказати пароль – слово, яка б охарактеризувало ваш настрій». Учитель бажає учням успіхів і звертається зі словами: «Усміхніться одне одному – і до вас прийде гарний, радісний настрій. А тепер до праці!»
II. Актуалізація опорних знань
1. Інтелектуальна розминка.
Учні самостійно формулюють основні поняття попередньої теми й дають їм визначення, один з учнів записує їх на дошці:
- атом;
- молекула (електронейтральна частинка речовини, яка складається з кількох атомів і здатна до самостійного існування);
- йони (заряджені одноатомні або багатоатомні частинки);
- хімічний елемент (вид атомів з певним зарядом ядра);
- відносна атомна маса (відношення абсолютної маси до атомної одиниці маси);
- період (горизонтальний ряд елементів);
- група (вертикальний стовпчик хімічних елементів).
Упродовж уроку на дошці будуть дописуватися ще нові поняття:
- прості речовини;
- складні речовини;
- хімічна формула (умовний запис складу речовин за допомогою хімічних знаків та індексів);
- метали;
- неметали.
2. Гра «Хімічні елементи»
У дітей та вчителя є набір карток із символами хімічних елементів. Учитель промовляє назву елемента, діти піднімають картки (модифікація гри: вчитель показує картку, а діти промовляють назву).
Н, С, O , F, Cu, Zn,Fe, Cl, S, K, N, P. (12 хімічних елементів). Набір карток.
3. Робота в парах – узаємоопитування.
а) Учні тренують одне одного в назвах і символах хімічних елементів.
б) Знаходять відповідність назв і символів у зошитах і взаємно перевіряють одне одного.
Картка № 1
Установіть відповідність між назвою хімічного елемента та його символом.
![]() а) I 1) Нітроген
а) I 1) Нітроген
 б) Au 2) Йод
б) Au 2) Йод
![]()
 в) Hg 3) Аргентум
в) Hg 3) Аргентум
г) Ag 4) Аурум
![]() ґ) Si 5) Меркурій
ґ) Si 5) Меркурій
д) N 6) Силіцій
Картка № 2
Установіть відповідність між назвою хімічного елемента та його символом.
![]()
 а) Al 1) Калій
а) Al 1) Калій
 б) Na 2) Алюміній
б) Na 2) Алюміній
![]() в) Ca 3) Станум
в) Ca 3) Станум
![]() г) Sn 4) Плюмбум
г) Sn 4) Плюмбум
ґ) Pb 5) Натрій
д) K 6) Кальцій
IV. Мотивація навчальної діяльності
Чи замислювалися ви коли-небудь, що вся література, написана українською мовою, складається із слів, що утворені всього із 33 літер; а вся музика, коли-небудь створена композиторами, написана з використанням різноманітних сполучень усього лише 7 нот; а всі числа, які ми записуємо, складаються лише із 10 символів?
А скільки ж хімічних елементів нам відомо? А скільки ж речовин вони можуть утворювати? Тож сьогодні на уроці ми поговоримо про багатоманітність речовин.
Повідомлення теми та мети уроку.
V. Вивчення нового матеріалу
1. Багатоманітність речовин.
Речовини можуть складатися як з окремих атомів, так із молекул, або заряджених частинок — йонів.
2. Прості та складні речовини.
Демонстрація.
Учням демонструємо зразки різних речовин, добре їм знайомі, на дошці вчитель записує формули цих речовин: цукор — C12H22O11, кухонна сіль — NaCl, марганцівка — KMnO4, цинк — Zn, алюміній — Al, сірка — S. Можна згадати, що до складу повітря входять кисень - О2 і азот — N2.
Чим відрізняються ці речовини? (за складом).
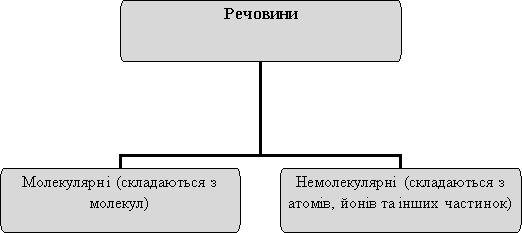
Даємо поняття «прості» й «складні речовини», складаємо схему і пропонуємо учням самостійно розподілити речовини на прості й складні. Схема заповнюється поступово: спочатку ділимо речовини на прості й складні, а потім доповнюємо поділ простих речовин на метали й неметали.
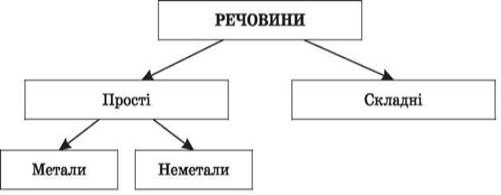
Прості – речовини, молекули яких складаються з атомів одного хімічного елемента (О2, N2, Al, S).
(Індекс унизу праворуч вказує на число атомів у молекулі)
Складні – речовини, молекули яких складаються з атомів двох і більше хімічних елементів (C12H22O11, NaCl, KMnO4).
Поняття про прості та складні речовини було введене Робертом Бойлем.
Назва простої речовини часто відрізняється від назви хімічного елемента, який її утворює: наприклад, Оксиген утворює просту речовину кисень, молекула якого складається з двох атомів, а Гідроген утворює просту речовину водень. За правилами сучасної української номенклатури назви елементів пишуться з великої літери, а назви речовин – з маленької. Наприклад, речовина алюміній складається з атомів Алюмінію, речовина бром складається з атомів Брому. В клітинках Періодичної системи наведені назви простих речовин, які відрізняються від назв елементів.
Назви складних речовин даються за певними правилами з якими ви познайомитеся пізніше. Вони складаються з двох слів і є похідними від назв елементів, що входять до складу складної речовини. Для складних речовин використовують тривіальні, або побутові назви (сода, крейда, кухонна сіль)
3. Метали й неметали.
Прості речовини поділяються на метали і неметали.
1. Яких елементів у космосі більше — металів чи неметалів? (Неметалів Н, Не).
А тепер подивімося в періодичну систему. Умовна діагональ від Бору до Астату поділяє періодичну систему на дві частини: у нижній частині таблиці ліворуч від діагоналі знаходяться елементи-метали, а у верхній лівій частині знаходяться елементи-неметали (крім елементів побічних груп).
Відомі також елементи, що в сполуках виявляють властивості як металів, так і неметалів. Вони називаються перехідними елементами. До них належать, наприклад, Ре, Gе та інші.
Окрема група елементів — це елементи головної підгрупи VIII групи: Не, Ne, Аг, Кг, Хе, Rn. Їх називають інертними, або благородними, елементами, оскільки вони не виявляють ні властивостей металів, ні властивостей неметалів.
Робота з підручником Попель П.
Учитель пропонує учням провести пошукове читання матеріалу підручника «Багатоманітність речовин. Прості й складні речовини. Метали й неметали» (с. 80-81). Вони мають знайти відповідь на запитання:
- Які фізичні властивості мають метали? (Немолекулярної будови, мають металевий блиск, сірі (крім міді); тверді, проводять електричний струм, ковкі (пластичні) - властивість металів деформуватися без руйнації під впливом певного навантаження, висока електропровідність).
- Які фізичні властивості мають неметали? (Неметали можуть мати як молекулярну, так і не молекулярну будову, погано проводять електричний струм і теплоту, крихкі).
Отже, кожна речовина має свої фізичні властивості: колір, запах, агрегатний стан, блиск тощо.
VІ. Узагальнення та систематизація знань учнів
Лабораторний дослід № 1. Ознайомлення зі зразками простих і складних речовин. Інструктаж з БЖД.
В учнів на столі зразки:
простих речовин: сірка, залізо, вугілля, алюміній;
складних речовин: вода, натрій хлорид, купрум(ІІ) оксид, цукор.
- Розгляньте речовини та відзначте:
- агрегатний стан;
- колір;
- відношення до води;
- запах.
2) Зробіть висновок про фізичні властивості простих і складних речовин.
3) Ґрунтуючись на власному досвіді, запропонуйте можливі способи застосування цих речовин.
4) Чи можна за зовнішнім виглядом судити про приналежність речовини до простих чи складних речовин?
Учні записують у зошитах спостереження й оформляють їх у вигляді таблиці, окремо для простих і складних речовин.
1. «Мікрофон».
Учні по черзі передають одне одному уявний мікрофон і дають визначення вивченим поняттям, які дописані по ходу уроку на дошці, доповнюють одне одного.
- Прості речовини;
- складні речовини;
- хімічна формула;
- метали;
- неметали.
VII. Підбиття підсумків уроку
Отже, давайте з’ясуймо:
- На які дві групи поділяються хімічні елементи? (Метали і неметали).
- Чи можна за властивостями розрізнити метали чи неметал?
- На які дві групи поділяються всі речовини?
VІІІ. Домашнє завдання
§ 13-14 (опрацювати), стор. 89 № 92 (ІІ рівень), № 93 (ІІІ рівень), № 94-95
(ІV рівень) - виконати письмово.
Творче завдання. Повідомлення про походження назв хімічних елементів.


про публікацію авторської розробки
Додати розробку
