Урок "Бензен як представник ароматичних вуглеводнів"
Тема уроку: Бензен як представник ароматичних вуглеводнів.
Мета уроку: ознайомити учнів з бензеном як представником гомологічного ряду аренів, особливостями утворення ароматичного хімічного зв’язку; розширити знання про систематичну номенклатуру на прикладі гомологів та ізомерів ароматичного ряду; ознайомити з фізичними властивостями бензену та його гомологів.
Тип уроку: вивчення нового матеріалу.
Хід уроку
I Організація класу
ІІ Актуалізація опорних знань
Аналіз самостійної роботи
ІІІ Мотивація навчальної діяльності
Сьогодні ми з вами продовжуємо вивчати органічні речовини. Розглянемо ще один клас вуглеводнів.
Повідомлення теми і мети уроку.
ІV Вивчення нового матеріалу
1. Ароматичні вуглеводні (арени).
Арени – це органічні сполуки, молекули яких мають 6-членне циклічне угруповання атомів Карбону, котре називають бензеновим ядром, або бензеновим кільцем.
Інша назва – ароматичні вуглеводні. Прямого відношення до запахів (ароматів) цей термін не має. Перші представники гомологічного ряду ароматичних вуглеводнів мають дійсно приємний запах, однак сьогодні відома значна кількість сполук цієї групи, які мають неприємний запах. Отже, цей термін – це швидше данина історії.
Арени або ароматичні вуглеводні – це сполуки, молекули яких містять стійкі циклічні групи атомів (бензенові ядра) з особливим характером хімічних зв'язків.
2. Склад і будова молекули бензену.
Вивчаючи конденсовані залишки світильного газу, який одержували з кам’яного вугілля, М. Фарадей у 1825 р. виділив вуглеводень з температурою кипіння 80 °С і визначив співвідношення Карбону й Гідрогену в ньому як 1:1. У 1834 р. Е. Мітчерліх шляхом нагрівання солей бензойної кислоти одержав подібний вуглеводень і дав йому назву бензин. Згодом Ю. Лібіх запропонував називати цю речовину бензеном.
Молекулярна формула бензену — C6H6.
Поширена структурна формула бензену, запропонована в 1865 р. німецьким ученим А. Кекулє, являє собою цикл із подвійними й одинарними зв’язками між атомами Карбону, що чергуються.
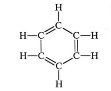 або просто
або просто 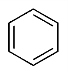
Молекула бензену є плоским правильним шестикутником, у вершинах якого розміщуються атоми Карбону, що перебувають у стані sp2-гібридизації. Кожен атом Карбону утворює σ і π-зв’язки. Довжина всіх С–С-зв’язків однакова і є проміжною між довжинами одинарних і подвійних зв’язків (їх називають полуторними).
Щоб показати, що в молекулі бензену немає простих і кратних зв’язків у чистому вигляді, було Л. Полінг запропонував зображувати структурну формулу як правильний шестикутник із кільцем усередині.

![]()
3. Фізичні властивості.
За стандартних умов бензен – безбарвна рідина з характерним запахом, температурою кипіння 80ºС, майже нерозчинна у воді, але сама є розчинником багатьох органічних речовин. Температура плавлення 5,5ºС, пара його з повітрям утворює вибухову суміш, бензен легший за воду (його густина 0,88 г/см3).
Бензен отруйна речовина. Вдихання його парів викликає запаморочення, головний біль, подразнення слизових оболонок. Рідкий бензен проникає крізь шкіру, що спричиняє отруєння.
4. Гомологи бензену
Унаслідок заміщення в молекулі бензену атомів Гідрогену на алкільні групи утворюються гомологи бензену, наприклад:
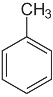
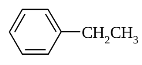
Метилбензен (толуен) Етилбензен
Загальна формула гомологів бензену (ароматичних вуглеводнів) — CnH2n-6, де n>6.
Гомологам бензену властива структурна ізомерія, зумовлена числом і положенням замісників у бензеновому ядрі. Молекулярній формулі С8Н10 відповідає 4 ізомери:
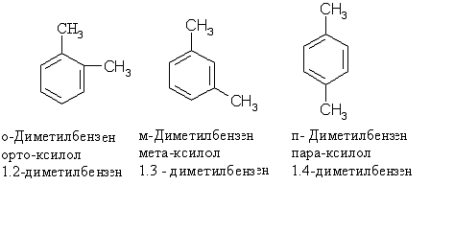
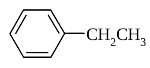
Етилбензен
Нумерація відбувається за годинниковою стрілкою. Для нумерації атомів Карбону в бензеновому ядрі дотримуються правил:
- для гомологів бензену, які містять два однакові замісники, послідовність нумерації атомів Карбону вибирають таким чином, щоб локанти були найменшими:
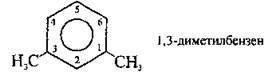
-
якщо замісники різні, використовують алфавітний порядок:
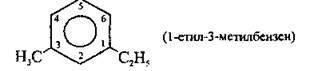
- у дизаміщених гомологах бензину для утворення тривіальних назв використовують префікси, які виділяють курсивом і відокремлюють дефісом:
|
Локанти замісників |
Префікси |
|
1,2 |
Орто – (о-) |
|
1,3 |
Мета – (м-) |
|
1,4 |
Пара – (п-) |
V Закріплення нового матеріалу
- Вкажіть формулу ароматичного вуглеводню та назвіть його за номенклатурою ІЮПАК:
а) С6Н6; б) С6Н12; в) С6Н10.
2. Серед наведених формул вкажіть формулу толуену:
а) С6Н6; б) С6Н5–СН3; в) С6Н5–С2Н5.
3. Вкажіть гомологи бензену:
а) 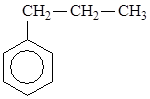 б)
б) 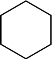 в)
в)  г)
г) ![]()
4. Вкажіть ізомери бензену:
а) 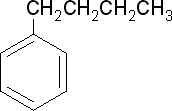 б)
б) 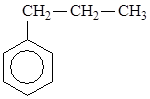 в)
в) 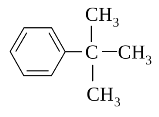
г) д)
д)
5. Назвіть наступні сполуки:
![]()
![]()
![]()
![]()
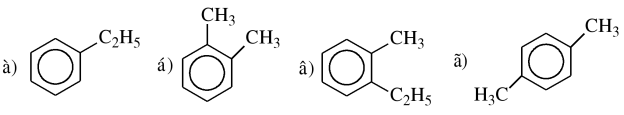
VI Підбиття підсумків уроку
VII Домашнє завдання
§16-17 опрацювати.
Напишіть ізомери пропілбензену і назвіть їх.
1


про публікацію авторської розробки
Додати розробку
