Урок "Хімічні властивості бензену"
Тема уроку: Хімічні властивості бензену.
Мета уроку: формувати в учнів знання про хімічні властивості бензену та його похідних, про реакції приєднання й заміщення в бензольному кільці; розвивати вміння складати хімічні рівняння на прикладі властивостей бензену.
Тип уроку: комбінований.
Хід уроку
I Організація класу
ІІ Актуалізація опорних знань
Перевірка домашнього завдання.
Які сполуки називають аренами?
Напишіть молекулярну і структурну формули молекули бензену і поясніть її будову.
Які фізичні властивості бензену?
Напишіть 3 гомологи бензену. Вкажіть як вони утворюються.
ІІІ Мотивація навчальної діяльності
Сьогодні ми з вами продовжуємо вивчати бензен.
Повідомлення теми і мети уроку.
ІV Вивчення нового матеріалу
Хімічні властивості бензену зумовлені наявністю π-електронної системи, що стабілізує ядро. Через це бензен стійкий проти дії окисників, він не знебарвлює розчин калій перманганату. Цим бензен нагадує насичені вуглеводні.
Хімічні властивості бензену
- Повне окиснення (горіння)
2C6H6 + 15О2 → 12СО2 + 6Н2О; ∆Н<0
- Часткове окиснення
Бензенове ядро стійке проти дії окисників (розчин калій перманганату не знебарвлюється)
- Заміщення
Відбувається легше, ніж у насичених вуглеводнів
нітрування:
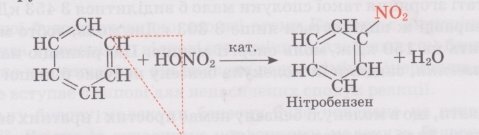
Нітробензен – жовта рідина із запахом гіркого мигдалю.
сульфурування:
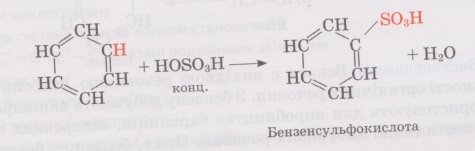
хлорування:
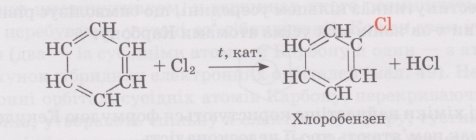
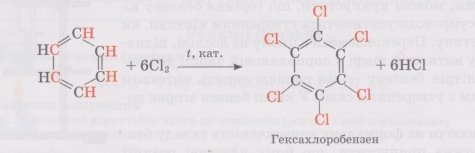
- Приєднання
Відбувається важче, ніж у ненасичених вуглеводнів (бромна вода не знебарвлюється)
водню:
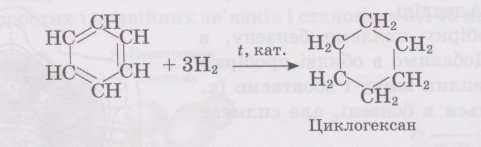
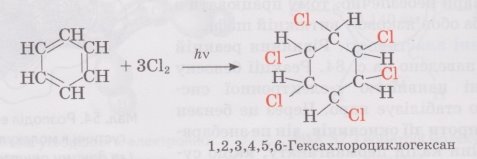
галогенів:
Отже, бензен вступає як в реакції заміщення, так і в реакції приєднання. Однак бензену більше властиві реакції заміщення.
V Закріплення нового матеріалу
Задача 1: У результаті реакції бензену з бромом утворився бромобензен масою 235,5 г. Вкажіть масу брому, необхідного за рівнянням реакції. (240 г)
Задача 2: Унаслідок спалювання вуглеводню масою 15,6 г утворились СО2 об’ємом 26,88 л (н.у.) та вода масою 10,8 г. Виведіть формулу вуглеводню, якщо відносна густина пари цього вуглеводню за киснем дорівнює 2,4375. (C6H6)
VI Підбиття підсумків уроку
VII Домашнє завдання
§16 опрацювати.
Задача 25 ст. 88: Із бензену масою 156 г добули хлоробензен. Визначте масу продукту реакції. (225 г)
1

про публікацію авторської розробки
Додати розробку
