Урок "Екзотермічні та ендотермічні реакції. Термохімічні рівняння."
Тема уроку. Екзотермічні та ендотермічні реакції. Термохімічні рівняння.
Мета уроку: сформувати поняття про тепловий ефект реакції та термохімічні рівняння, навчити розрізняти екзо- та ендотермічні реакції, складати термохімічні рівняння реакцій, розв’язувати задачі з їх використанням, характеризувати реакції за тепловим ефектом; розвинути знання про класифікацію хімічних реакцій; сформувати навички оцінювання практичного значення та ролі термохімічних реакцій у природі й житті людини.
Обладнання та матеріали: мультимедійна презентація уроку, негашене вапно, вода, фарфорова чашка, свічка, свіжовиготовлений купрум (ІІ) гідроксид; спиртівка; сірники
Тип уроку: засвоєння нових знань.
Форми роботи: розповідь учителя, інтерактивна бесіда індивідуальна робота, демонстраційний експеримент, робота з підручником.
Девіз уроку: «Єдиний шлях, що веде до знань, - діяльність» (Бернард Шоу).
Хід уроку
І. Організаційний момент.
ІІ. Актуалізація опорних знань та їх коригування.
«Мозковий штурм» (Слайд 1)
Пригадайте, якими зовнішніми ефектами характеризується перебіг хімічної реакції.
ІІІ. Мотивація навчальної діяльності
Сьогодні панує тренд – дбати про своє здоров’я. Чи знаєте ви, як обчислюється енергетична цінність харчових продуктів?
Чи уявляєте ви життя сучасної людини без холодильника? Не думали, як в ньому підтримується низька температура? (холодоагент)
Чи можна уявити еволюцію людства без вогню, без можливості приготувати їжу, обігріти житло?
Що об’єднує холодильник і піч? Як досягається в обох випадках зміна температури?
В їх основі – хімічні реакції, під час яких відбувається виділення або поглинання тепла.
 ІV. Оголошення теми, мети, завдань уроку.
ІV. Оголошення теми, мети, завдань уроку.
Тема урок.
(Слайд 2)
 Мета уроку
Мета уроку
(Слайд 3)
V. Вивчення нового матеріалу (первинне засвоєння)
- Тепловий ефект реакції.
Атоми або йони в сполуках реагуючих речовин і утворених із них продуктів реакції мають між собою хімічні зв’язки.
Які зв’язки зруйнуються, а які мають утворитись?
Чи погодитесь, що для того, щоб щось зруйнувати, треба докласти зусиль? Отже, на це витрачається енергія?
![]() Розрив зв’язків Утворення зв'язків
Розрив зв’язків Утворення зв'язків
Поглинається Е Виділяється Е
(Поглинається тепло) (Виділяється тепло)
Запишіть в зошит визначення теплового ефекту реакції. (Слайд 4)

Що, на вашу думку, треба знати для визначення енергетичної цінності харчових продуктів?
(Щоб обчислити енергетичну цінність харчових продуктів, треба знати тепловий ефект реакції їх згоряння)
-
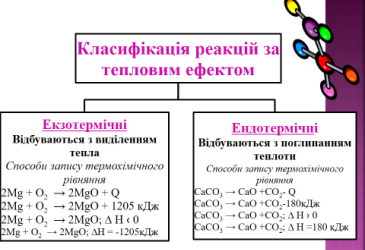
Класифікація реакцій за тепловим ефектом: екзо- та ендотермічні реакції. (Слайд 5)
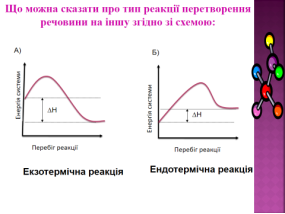
Пригадайте з фізики - кожна речовина характеризується певним запасом енергії, що утворюється внаслідок хаотичного руху структурних частинок цієї речовини (молекул, атомів, йонів тощо). Як називається така енергія? (Слайд 6).
![]() Реагенти Продукти
Реагенти Продукти
Внутрішня Е Внутрішня Е
Що відбудеться, якщо внутрішня енергія реагентів більша, ніж внутрішня енергія продуктів? ( Енергія у вигляді тепла виділяється)
Що відбудеться, якщо внутрішня енергія реагентів менша , ніж внутрішня енергія продуктів? (Енергія у вигляді тепла поглинається)
Дослід 1. Взаємодія кальцій оксиду з водою - «гасіння вапна».
На дно фарфорової чашки покладемо кілька шматочків кальцій оксиду й обережно доллємо воду. Спостерігаємо бурхливу реакцію, закипання» суміші з виділенням великої кількості тепла
![]()
Тепло виділяється, чи поглинається? Позначення теплового ефекту знайдіть на с. 107 , як називається така реакція. Запишіть в зошит
Наведіть ще приклади реакцій, під час яких виділяється тепло.
Дослід 2. Розклад купрум(ІІ) гідроксиду.
Нагріємо в полум'ї спиртівки синій осад купрум(ІІ) гідроксиду, добутий реакцією обміну. За кілька хвилин спостерігаємо утворення чорного осаду — порошку купрум(ІІ) оксиду. Реакція відбувається тільки за нагрівання, тобто з поглинанням тепла.
На с. 108 підручника знайдіть, як називають такі реакції. Запишіть в зошит
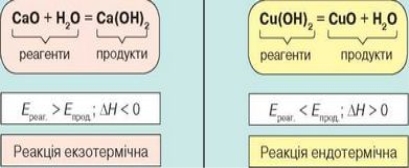
- Термохімічні рівняння
Зверніть увагу на запис рівнянь реакцій горіння магнію та розкладу кальцій карбонату. Що в них незвичне? Знайдіть на с.113, як називають такі рівняння. Запишіть в зошит. (Слайд 7)

VI. Осмислення нових знань, умінь.
1. Які з наведених реакцій є екзотермічними? (Слайд 9) 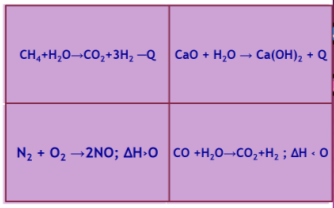
2.Складання термохімічних рівнянь реакцій. Робота з підручником с.114. Обговорення розв’язування задач.
VIІ. Закріплення, систематизація та узагальнення.
- Запишіть рівняння горіння водню. Тепловий ефект реакції дорівнює 572кдж. (Слайд 10)

- До якого типу належать реакції, що відбуваються в пробірках? (Слайд 11)
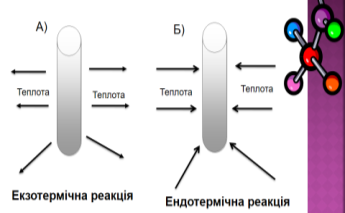
VІІІ. Контрольно-коригувальний етап. - Обчислення за термохімічними рівняннями
(3 варіанти)(Слайд 12)

І Х. Підбиття підсумків уроку.
Х. Інструктаж щодо виконання домашнього завдання. (Слайд 13) 
-
Дуже вдалий конспект!


про публікацію авторської розробки
Додати розробку
