Урок "ХІМІЧНІ ВЛАСТИВОСТІ КИСНЮ: ВЗАЄМОДІЯ ЗІ СКЛАДНИМИ РЕЧОВИНАМИ."
1
ТЕМА УРОКУ: ХІМІЧНІ ВЛАСТИВОСТІ КИСНЮ: ВЗАЄМОДІЯ ЗІ СКЛАДНИМИ РЕЧОВИНАМИ.
МЕТА УРОКУ:
навчальна: засвоїти поняття про окиснення складних речовин; закріпити знання про оксиди та реакції сполучення.
розвивальна: розвивати навички складання рівнянь хімічних реакцій, які характеризують хімічні властивості кисню; розвивати логічне мислення, пам’ять, пізнавальну активність, увагу.
виховна: виховувати самостійність, уважність, позитивні риси характеру.
ОБЛАДНАННЯ: підручник, періодична система хімічних елементів, роздатковий матеріал для учнів у вигляді карток-опорних схем.
ТИП УРОКУ: Комбінований.
МЕТОДИ І МЕТОДИЧНІ ПРИЙОМИ: словесний (бесіда, розповідь, пояснення, складання опорних схем), наочний (демонстрація наочності).
Хід уроку
І. ОРГАНІЗАЦІЙНИЙ ЕТАП. (2 хв)
Привітання класу. Перевірка готовності учнів до уроку.
ІІ. МОТИВАЦІЯ НАВЧАЛЬНОЇ ДІЯЛЬНОСТІ УЧНІВ (2 хв)
Учитель: Минулого уроку ви дізналися про процеси окиснення, взаємодію кисню з простими речовинами з утворенням одного оксиду. Але виявляється що може утворитися не лише один оксид, а декілька. Яким чином це буде відбувається ви дізнаєтесь сьогодні на уроці. Також наприкінці уроку ми з вами складемо опорну таблицю, яка допоможе вам краще опанувати тему, розкласти всі свої знання «по поличках» та підготуватися до контрольної роботи. Отже, записуємо тему нашого уроку «Хімічні властивості кисню: взаємодія зі складними речовинами».
ІІІ. АКТУАЛІЗАЦІЯ ОПОРНИХ ЗНАНЬ УЧНІВ (3 хв)
Учитель: Перед тим як перейти до нової теми давайте пригадаємо:
- Які умови необхідні для процесу горіння?
- Які фізичні властивості кисню ви знаєте?
ІV. ВИВЧЕННЯ НОВОГО МАТЕРІАЛУ (15 хв)
Учитель: Кисень може взаємодіяти не лише з простими речовинами, а й зі складними. Такі реакції відбуваються, наприклад, коли горить етиловий спирт, ацетон, природний газ (він переважно складається з метану) тощо. Молекула метану СН4 у своєму складі містить атоми Карбону і Гідрогену. Внаслідок цих речовин з киснем утворюються оксиди Карбону і Гідрогену – вуглекислий газ і вода (в газуватому стані). Запишіть в зошит:
CН4 + O2 = CO2 + Н2О
Метан у чистому вигляді горить синім полум’ям, а при недостатньому вмісті кисню у повітрі він починає горіти яскраво помаранчевим полум’ям.
Ці оксиди виділяються також при спалюванні деревини, нафтопродуктів і багатьох інших органічних речовин.
Гідроген сульфід або сірководень, – газ, що має формулу H2S. Цей газ безбарвний, ви можете його розрізнити серед інших за специфічним запахом. За наявності кисню чи надлишку повітря він горить з утворенням сірчистого газу і водяної пари. Запишіть у зошит:
H2S + O2 = SO2 + H2O
Треба зауважити, що кисень взаємодіє з деякими оксидами. Продуктами таких реакцій є інші оксиди, в яких елементи виявляють вищі значення валентності, ніж у вихідних сполуках. Наприклад, чадний газ, взаємодіючи з киснем, перетворюється на вуглекислий газ, записуємо у зошити:
2CO +O2 = 2CO2
З наведених рівнянь реакції видно, що під час взаємодії складних речовин з киснем, утворюються оксиди тих хімічних елементів, які входили до складу складної речовини.
Запишемо загальну формулу взаємодії простих речовин з киснем:
АВ + О2 = АхОу + ВхОу
Що ж, хімічні властивості кисню ми з вами сьогодні розглянули, а тепер давайте складемо опорну схему, що буде складатися з 4 блоків, а саме:
- Загальна характеристика кисню.
- Добування кисню.
- Фізичні властивості кисню.
- Хімічні властивості кисню.
- Біологічна роль кисню.
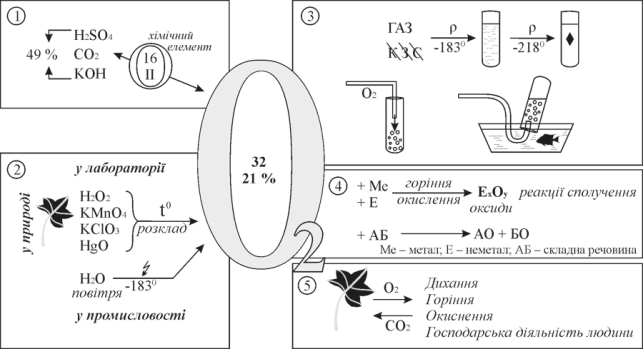
V. УЗАГАЛЬНЕННЯ І СИСТЕМАТИЗАЦІЯ ЗНАНЬ (20 хв)
Фронтальне опитування. Для підведення підсумків нагадайте мені:
1. Чому в результаті горіння може утворитися декілька оксидів?
2. Які ви знаєте типи хімічних реакцій?
3. До якого типу належить реакція горіння сірки? Сірководню? Добування кисню?
4. Чому в кисні речовини горять краще, ніж у повітрі?
Робота біля дошки
- Складіть формули оксидів для вказаних нижче елементів і назвіть їх:
Ca(II), Mn(VII), Cr(VI), K(I), Mn(IV), Cl(VII), Fe(II), P(III).
- Закінчіть рівняння реакцій та вкажіть назви отриманих оксидів:
|
Р + О2 → Cl +O2 → |
Mg + O2 → Cu + O2 → |
CaS + O2 →
C2H2 + O2 → |
VIІ. ДОМАШНЄ ЗАВДАННЯ (3 хв)
Підручник: прочитати та вивчити §18. Виконати вправи після параграфу № 1, 7, 8.

про публікацію авторської розробки
Додати розробку
