Урок "Класифікація хімічних реакцій. Реакції сполучення, розкладу, обміну"
Клас 9 дата урок
ТЕМА УРОКУ . Класифікація хімічних реакцій. Реакції сполучення, розкладу,
заміщення й обміну.
Очікувальні результати. Після цього заняття учні зможуть:
- розрізняє реакції сполучення, заміщення, обміну, розкладу;
- наводить приклади основних типів хімічних реакцій;
- характеризує процеси сполучення, розкладу, заміщення,
обміну;
- дотримується правил використання побутових хімікатів;
Навчально – методичне та матеріальне забезпечення: періодична система
хімічних елементів, таблиця розчинності,
ряд активності металів, правила техніки безпеки,
комп’ютер, проектор, інтерактивна дошка, смартфони або
планшети.
Тип уроку : комбінований .
Методи та методичні прийоми : словесні (бесіда, пояснення, розповідь
вчителя), проблемно–пошукові (проблемне запитання),
практичні (демонстрації).
Хід уроку
1.Вступна частина .Організація класу.
2. Мотивація навчальної діяльності.
Учитель: На початку уроку я хочу прочитати вам уривок з твору
Л. Керрола «Аліса в Країні чудес»: «За кілька кроків від неї сидів на гілці Чеширський кіт.
Скажіть, будь ласка, куди мені звідси йти?
А куди ти хочеш потрапити?–спитав кіт у відповідь.
Мені все одно…– сказала Аліса.
Тоді все одно куди йти, - зауважив кіт».
Питання до класу: « Що хоче сказати цим кіт Алісі та навіщо я прочитала ці слова на самому початку уроку?» (відповідь учнів)
Слайд 1
Учитель. Так, правильно, потрібно знати мету своєї роботи. І сьогодні на уроці ми будемо вчитися спостерігати і робити висновки. Ці вміння потрібні в житті кожної людини. Для нас спостерігати – це не просто помічати, адже спостереження – перший етап людського пізнання. Тому постарайтеся сьогодні починати свою відповідь словами: «А от я помітив…; я думаю , що…». Хочу нагадати вам , що всі учні під час уроку оформляють опорний конспект, де виконують всі запропоновані вправи, записують спостереження та висновки з лабораторних дослідів, записують рівняння реакцій, визначення понять, що вивчаються. Не забувайте проставлять набрані за кожне завдання бали. Тому, що сума цих балів – це оцінка вашої роботи на нашому уроці.
Світ, який нас оточує надзвичайно різноманітний і може бути визначеним одним поняттям – матерія, що існує в різних формах.
Речовина – предмет науки хімії є одним з видів матерії, яка існує тільки в русі.
Атоми, молекули, іони , кристали і інші частинки з яких складається речовина також перебувають в постійному русі. Тому хімічну реакцію необхідно розглядати як одну з форм руху матерії.
Саме тому девізом сьогоднішнього уроку є слова « Безліч реакцій споріднює критерій, а будь яка реакція – це форма руху вічних матерій»

Як стверджували стародавні філософи: « Все тече, все змінюється» , а будь –яка зміна в природі , світі , суспільстві як називається? (явище)
На уроках фізики ми вивчаємо фізичні явища, біології – біологічні, історії – суспільні. На уроках хімії ми розглядаємо хімічні явища. Скажіть, яку ще назву мають хімічні явища? ( хімічні реакції)
Тема нашого уроку « Класифікація хімічних реакцій». Тема вивчатиметься на протязі 9 уроків на при кінці теми контрольна робота у вигляді тестів.

Мета уроку. Вправа мозковий штурм. Давайте разом сформулюємо мету нашого уроку. Приклад мети яку можуть сформулювати учні
• Навчитись класифікувати рівняння реакцій по кількості та складу вихідних речовин та продуктів реакції.
• Продовжувати формувати вміння складати рівняння реакцій.
• Розвивати вміння спостерігати та робити висновки.

3. Актуалізація опорних знань учнів. Робота в парах. На партах є карточки – доміно потрібно швидко скласти правильний ланцюжок відповідей. Перші три пари отримують за роботу по 1 балу.(далі всі учні які відповідають на уроці, додають до свого рахунку оцінки по 1 балу за відповідь)
Для повторення вивченого раніше матеріалу скористаємось деякими іграми:
Хімічне доміно
--кислоти – речовини, що містять Гідроген та кислотний залишок;
--хімічне рівняння – скорочений запис хімічної реакції;
--оксиди – складаються з двох елементів, один з них Оксиген;
--основи – речовини,що містять метал і гідроксогрупу;
--солі – речовини,що містять метал і кислотний залишок;
--луги – розчинні у воді основи;
--реакція – перетворення одних речовин на інші.
Індивідуальна робота.
Назвіть зовнішні ознаки , що можуть супроводжувати хімічні реакції. Встановіть відповідність між реакціями зображеними на слайді та їх ознаками
- зміна забарвлення ;
- виділення чи поглинання газу;
- утворення чи розчинення осаду;
- поява запаху ;
- виділення чи поглинання теплоти і світла.

Які умови необхідно створити, щоб почалась хімічна реакція?
- змішати;
- нагріти;
- додати каталізатор.

2. Основна частина.
Що називається класифікацією?
Що ми будемо називати класифікацією реакцій?
Щоб розібратись у різномаїтті хімічних реакцій, їх класифікують за різними ознаками , критеріями.
Метод «Кластер», на першому уроці починаємо складати кластер, на кожному наступному уроці з теми доповнюємо новими поняттями.
Сьогодні на уроці ми з вами почнемо складати «Дерево теми». На папері (папір для фліптчатів, ватман і т.д.) зображаємо початок кластера.
На сьогоднішньому уроці ми розглянемо класифікацію за першою ознакою - кількість і склад вихідних речовин та продуктів реакцій. відкрийте§20 та вкажіть ознаку за якою ми сьогодні класифікуємо реакції.(по кількості та складу вихідних речовин та продуктів реакції)
Скільки типів реакцій вирізняють за цією ознакою?(4 типи)
Перерахуйте ці типи реакцій. (реакції сполучення, розкладу, заміщення, обміну) На наступних уроках цієї теми ми розглянемо класифікацію і за іншими ознаками.
На уроках у 8 класі ми вже вивчали ці типи реакцій. Для того , щоб пригадати ці реакції, ви на минулому уроці розділились на 4 команди. Кожна команда досліджувала певний тип реакцій за допомогою Інтернет ресурсу. Потрібно було знайти відеозапис реакції певного типу. Один учень з кожної команди презентує роботу своєї команди.
Метод Ланцюжок думок. Учні по черзі коментують позначки на картках з правилами техніки безпеки.
Давайте пригадаємо найважливіші правила техніки безпеки які використовують під час роботи з реактивами.

Забороняється пробувати речовини на смак(а);
брати речовини руками (б);
залишати відкритими банки з реактивами (в);
висипати та виливати залишки реактивів в банки з яких вони були взяті (г) ;
залишати неприбраними розлиті чи розсипані реактиви (д); змінювати пробки та піпетки з різних банок (е);
працювати потрібно над столом (ж) ;
якщо реактив потрапив на шкіру чи одяг, його необхідно змити водою та нейтралізувати відповідним розчином (з);
збирати залишки реактивів у відповідний спеціальний посуд (и)
Демонстрація роботи домашніх груп та заповнення учнями опорного конспекту. Представник домашньої групи після демонстрації свого типу реакцій доповнює кластер.
Реакції сполучення.
Перегляньте відео дослід та заповніть таблицю
|
Що робили |
Що спостерігали |
Рівняння |
|
Спалили магнієву дротину |
|
|
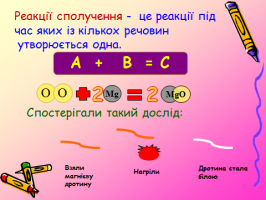
Які ознаки хімічних реакцій ми бачили?яка кількість речовин була до реакції та утворилась в результаті реакції? До якого типу реакцій належить дана реакція?
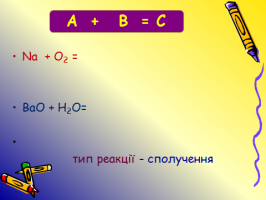
Допишіть рівняння реакцій заданих в опорному конспекті.
Nа+ О2 = Н2+ О2=
ВаО+ Н2О= SО2+ Н2О=
Реакції заміщення
Перегляньте відео дослід та заповніть таблицю.
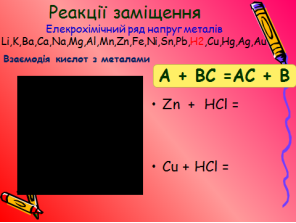
|
Що робили |
Що спостерігали |
Рівняння |
|
В дві пробірки насипали порошків Сu (міді) та Zn (Цинку) та в кожну долили НСl |
|
|
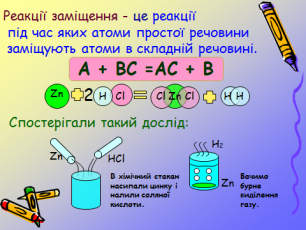
Які ознаки хімічних реакцій ми бачили? За яким правилом метали вступають в реакцію заміщення? Яка кількість речовин була до реакції та утворилась в результаті реакції? До якого типу реакцій належить дана реакція? Допишіть рівняння реакцій заданих в опорному конспекті.
Мg + Сr2О3= Мg + НСl=
СuСl2 + Fе= Аg + НСl =
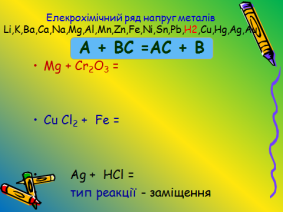
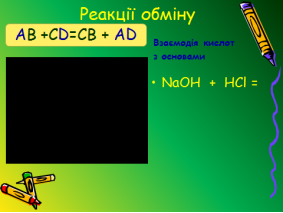
Реакції обміну.
Перегляньте відео дослід та заповніть таблицю.
|
Що робили |
Що спостерігали |
Рівняння |
|
В пробірку налили розчин NаОН і додали кілька крапель фенолфталеїну потім долили розчину НСl |
|
|
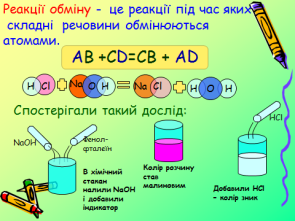
Які ознаки хімічних реакцій ми бачили? Яка кількість речовин була до реакції та утворилась в результаті реакції? До якого типу реакцій належить дана реакція? Допишіть рівняння реакцій заданих в опорному конспекті.
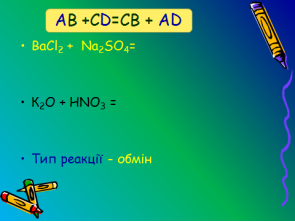
ВаСl2 + Nа2SО4= НІ + Аl(ОН)3=
СаСО3 + НВr= К2О + НNО3=
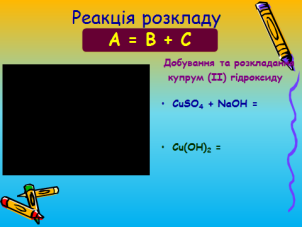
Реакції розкладу.
Перегляньте відео дослід та заповніть таблицю.
|
Що робили |
Що спостерігали |
Рівняння |
|
В пробірку налили розчину купрум сульфату CuSO4 і долили NaОН натрій гідроксид, утворений розчин нагріли |
|
|
Яку кількість реакцій ми бачили на відео?
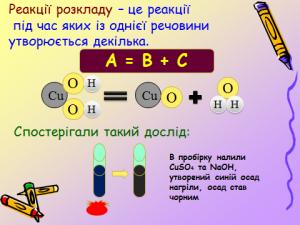
Які ознаки хімічних реакцій ми бачили? Яка кількість речовин була до реакції та утворилась в результаті першої реакції? До якого типу реакцій належить дана реакція? Яка кількість речовин була до реакції та утворилась в результаті другої реакції? До якого типу реакцій належить дана реакція? Допишіть рівняння реакцій заданих в опорному конспекті.
Аl(ОН)3= Fе(ОН)3=
Zn СО3= Са(ОН)2=

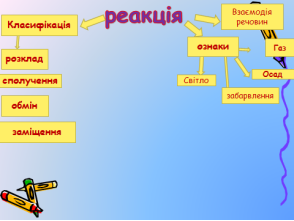
Вид кластера в кінці презентацій роботи груп.
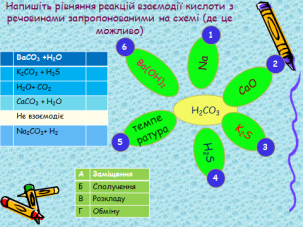
Завдання 1 для самостійного опрацювання в опорному конспекті. Через дві хвилини . ( рекомендую використовувати цифрову платформу classtime для створення тестового опитування)
Встановіть відповідність між початком , закінченням та типом реакції:
- Н2СО3+Na= А. BaСО3 + H2O
- Н2СО3+ CaO= Б. K2СО3 + H2S
- Н2СО3+ K2S= В. СаО + СО2
- Н2СО3+ H2S= Г. CaСО3 + H2O
- Н2СО3+ Cu= Д. не взаємодіє
- Н2СО3+Ba(OH)2= Е. Na2СО3+ H2
|
1 |
2 |
3 |
4 |
5 |
6 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Завдання 2 Самостійна робота
1 варіант
1. Виберіть чинник, який покладено в основу класифікації реакцій на реакції розкладу, сполучення, заміщення , обміну
(0,5 балів) :
А) природа реагуючих речовин;
Б) величина теплового ефекту реакції;
В) зміна чи не змінність ступенів окислення елементів;
Г) зміна кількості та складу речовин.
2. Виберіть твердження щодо реакцій обміну ( 0,5 балів):
А) у ній беруть участь лише прості речовини;
Б) у ній беруть участь прості та складні речовини;
В) у ній беруть участь лише складні речовини;
Г) у ній беруть участь лише органічні речовини.
3. Допишіть рівняння реакцій , вкажіть реакції заміщення ( 1 бал) :
А)SO3 + H2O = ; Б) H2O + K = ;
В) Fe2O3 + H2= ; Г) NaOH + H3РO4 = ;
4. Встановіть відповідність наведених реакцій їх типу
( 1 бал):
Реакція: Тип реакції:
1)CuSO4 + Fe = Cu + FeSO4 ; а) реакція обміну;
2) (CuOH)2CO3 = 2CuO+ CO2 + H2O; б) реакція сполучення;
3)Ba(OH)2 +2HCl = BaCl2 + 2H2O ; в) реакція розкладу
г) реакція заміщення.
2 варіант
1. Виберіть твердження щодо реакції розкладу (0,5 балів):
А) число продуктів реакції менше числа вихідних речовин;
Б) утворюється тільки дві речовини ;
В) може утворитись дві чи більше речовин;
Г) число реагентів має дорівнювати числу продуктів реакції.
2. Виберіть твердження щодо реакцій заміщення (0,5 балів):
А) число вихідних речовин завжди більше числа продуктів реакції;
Б) число вихідних речовин завжди менше числа продуктів реакції;
В) число вихідних речовин завжди дорівнює числу продуктів реакції;
Г) не змінюється ступінь окислення елементів у речовинах, що реагують.
3. Допишіть рівняння реакції, вкажіть реакції сполучення (1 бал):
А) CaO + CO2 = ; Б) Zn (OH)2 = ;
В) Al2O3 + HCl = ; Г) Fe + S= ;
4. Встановіть відповідність типів наведеним реакціям (1 бал) :
Реакція: Тип реакції:
1) Cu(OH)2 = CuO + H2O ; а) реакція сполучення;
2) CaO + H2O = Ca(OH)2 ; б) реакція обміну;
3) Fe2O3 + 3H2 = 2Fe +3H2O; в) реакція розкладу.
4) ZnSO4 + BaCl2 = ZnCl2 + BaSO4 ;
Взаємоперевірка самостійної роботи та підрахунок оцінок за урок.

Рефлексія:
1.Метод Ланцюжок запитань. Учень запитує однокласника, той відповідає на запитання і ставить запитання наступному учню класу.
Поставте запитання щодо вивченої своєму однокласнику. Приклади можливих запитань
• Що таке класифікація реакцій?
• Що називається хімічною реакцією?
• Які ознаки хімічних реакцій вам відомі?
• За якою ознакою ми сьогодні на уроці класифікували хімічні реакції?
• Які реакції називаються реакціями розкладу?
• Які реакції називаються реакціями обміну?
• Які реакції називаються реакціями заміщення?
• Які реакції називаються реакціями сполучення?
Домашне завдання : підручник Григорович О.В. Хімія 9 клас §20 Впр. № 248
Творче завдання: скласти кросворди з ключовими
словами : «реакція», «сполучення», «заміщення», «обмін».


про публікацію авторської розробки
Додати розробку
