Урок "Масова частка розчиненої речовини"
ТЕМА УРОКУ: Масова частка розчиненої речовини.
МЕТА УРОКУ: Ознайомити учнів із кількісним зображенням складу розчину; дати уявлення про масову частку розчиненої речовини, навчитися обчислювати масову частку і масу розчиненої речовини в розчині, готувати розчини з певною масовою часткою розчиненої речовини, поглибити знання учнів про значення розчинів, розвивати вміння оформляти задачі, логічно мислити.
ХІД УРОКУ
І. Організація класу.
Перевірка присутності і готовності учнів до уроку. Відповіді на запитання учнів.
ІІ. Мотивація уроку.
Працюючи з розчинами, важливо знати, скільки розчиненої речовини міститься в них, знати кількісний склад розчинів, бо в медицині, наприклад, в залежності від кількості речовини розчини можуть бути шкідливими або корисними.
ІІІ. Повідомлення теми, мети уроку.
Про склад розчину можна дізнатися за допомогою масової частки розчиненої речовини. Протягом уроку ми з'ясуємо:
- що таке масова частка розчиненої речовини;
- як обчислювати масову частку розчиненої речовини;
- як вести розрахунки, необхідні для приготування розчинів;
- як правильно приготувати розчин з певною масовою часткою розчиненої речовини.
IV. Актуалізація знань.
Бесіда.
- Які суміші називають розчинами?
- 3 яких компонентів складаються розчини?
- Які розчини називають насиченими, ненасиченими, розбавленими, концентрованими?
- Чи може розбавлений розчин бути насиченим?
- Чи обов'язково концентрований розчин буде насиченим?
- Чи зустрічалися ви з поняттям «масова частка» і що воно означає?
V. Вивчення нового матеріалу.
1. МАСОВА ЧАСТКА РОЗЧИНЕНОЇ РЕЧОВИНИ
При вивченні хімії у 8 класі ви знайомилися з поняттям «масова частка елемента в сполуці». Пропонується учням скласти формулу для масової частки розчиненої речовини за аналогією. Записати на дошці формули масової частки розчиненої речовини і масової частки елемента в сполуці, а потім проаналізувати подібність і відмінність цих понять:
Масова частка розчиненої речовини - це відношення маси розчиненої речовини до маси розчину:
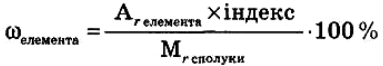
ω виражають в частках або відсотках.
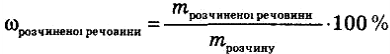
Оскільки маса розчину складається з маси води и маси розчиненої речовини, то вихідна формула перетворюється на
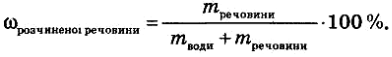
2. РОЗВ'ЯЗУВАННЯ ЗАДАЧ НА ЗАСТОСУВАННЯ МАСОВОЇ ЧАСТКИ ()
1) Розрахуйте масову частку натрій хлориду в 150 г розчину, який містить 15 г солі.
 2). Розрахуйте масову частку цукру в розчині, який містить 200 г води і 50 г цукру. Відповідь: 20 %
2). Розрахуйте масову частку цукру в розчині, який містить 200 г води і 50 г цукру. Відповідь: 20 %
3). Яка маса натрій сульфату міститься в розчині масою 50 г з масовою часткою розч. речовини 25%. Відповідь: 12,5 г Na2SO4.
4) Розрахуйте масу розчину сульфатної кислоти з масовою часткою З0 %, який містить 90 г кислоти. Відповідь: 300 г.
5) Обчисліть масову частку розчиненої речовини, що отримали при розчиненні натрій сульфату масою 40 г у воді масою 300 г.
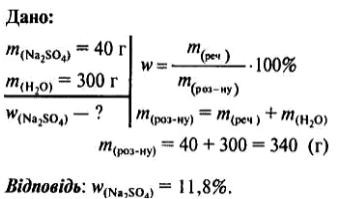
6) У якому співвідношенні слід змішати 5% -й розчин їдкого калію з 40%-м розчином цієї ж речовини, щоб добути 250 г 25%-го розчину калій гідроксиду?
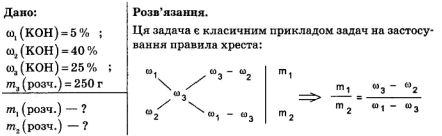
.

- До розчину масою 300 г з масовою часткою натрій нітрату 20% додали розчин масою 500 г з масовою часткою натрій нітрату 40%. Обчисліть масову частку солі в утвореному розчині.
VI. Закріплення знань учнів.
1). Розрахуйте масову частку нітратної кислоти в розчині, 1 л якого містить 224 г нітратної кислоти; густина розчину 1,12 г/мл.

2). Визначте масу води, у якій треба розчинити 2 г натрієвої селітри NaNOg, щоб добути розчин з масовою часткою селітри 0,1 %.

3). До розчину натрій гідрокарбонату масою 200 г з масовою часткою гідрокарбонату 10 % додали 5 г натрій гідрокарбонату. Визначте масову частку солі в добутому розчині.
4).3 400 г розчину солі з масовою часткою 50 % випарували 100 г води. Визначте масову частку солі в розчині після випарювання.
VIІ. Завдання додому.
- Вивчити § підручника.
- Розв'язати завдання після параграфа
- Скласти свою задачу по темі «Розчини». Записати її на картці розміром 2см7см з білого аркушу паперу. На наступному уроці буде влаштована лотерея з цих завдань. Ви будете вирішувати завдання один одного і ставити оцінки.
VIIІ. Підсумок уроку.
Підсумовується робота учнів на уроці, визначаються змістовні і слабкі відповіді, виставляються оцінки за урок.
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ:
Література:
- Попель П.П. Хімія: підруч. для 9 кл. загальноосвіт. навч. закл. / П.П.Попель, Л.С.Крикля – К.: ВЦ «Академія», 2009 – 232 с.: іл. (книга двох авторів).
- Дігавцова Л.Ю. Хімія. 9 клас : Плани-конспекти уроків на друкованій основі / Л. Ю. Дігавцова — Х. : Вид-во «Ранок», 2013. — 128 с. — (Серія «Конструктор уроку»). (книга одного автора).
- Старовойтова І.Ю. Усі уроки хімії 9 клас / І.Ю.Старовойтова, О.В.Люсай. – Х.: Вид. Група «Основа», 2009 – 239, [1]с.: іл.,табл. – (Серія « 12 – річна школа»). (книга одного автора).
- Григорович О.В. Хімія. 9 клас: Розширене календарне планування уроків / О.В. Григорович, О.М. Гостинникова, А.В. Трушина – Х.: Веста: Видавництво «Ранок», 2007. – 96 с. – (На допомогу вчителю). (книга трьох авторів).
- Гранкіна Т.М. Хімія. 9 клас: Плани-конспекти уроків / Т.М. Гранкіна, О.В.Григорович. – Вид. 3-тє, випр. – Х.: Веста: Видавництво «Ранок», 2005. – 272 с. – (На допомогу вчителю) (книга двох авторів).
- Буринська Н.М. Тестові завдання та вправи з неорганічної хімії / Н.М. Буринська– К.: АТ «ОКО», 1996. – 203 с. (книга одного автора)
- [Електронний ресурс]. – Режим доступу: http://festival.1september.ru/articles/653304/
- (електронне джерело).
- [Електронний ресурс]. – Режим доступу: http://him.1september.ru/article.php?ID=200500408 (електронне джерело).
- [Електронний ресурс]. – Режим доступу: http://studydoc.ru/doc/4706114/rastvory-raschet-massovoj-doli-rastvora-raznymi-sposobami-... (електронне джерело).
- [Електронний ресурс]. – Режим доступу: http://elearning.sumdu.edu.ua/free_content/lectured:5df7011dd2ba3fd1467ffc0f892ff9da2731ded5/latest/258393/index.html (електронне джерело).
1


про публікацію авторської розробки
Додати розробку
