Урок на тему: "Ступінь окиснення"
Тема: Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки.
Мета: сформувати уявлення про ступінь окиснення, розділити поняття «валентність» і «ступінь окиснення»; формувати навички визначення ступеня окиснення в сполуках за формулами, а також за будовою атомів, що утворюють ці сполуки. . Вказати спільність та відмінність між валентністю та ступенем окиснення атомів.
- розвивати в учнів творчість мислення, мобільність, творчий підхід до вивчення цієї теми;
- виховати вміння співпраці та взаємодії,використовувати логічне мислення, прострову уявудля складання структурних формул
Обладнання: Періодична система хімічних елементів Д. І. Менделєєва
Тип уроку: комбінований
ХІД УРОКУ
Девіз уроку: «Найди всьому початок
і ти багато чого зрозумієш»
І. Організація класу
II Актуалізацяі опорних знань учнів
1.Дати визначення валентність. Як визначити валентність у сполуках?
2. Визначіть валентність елементів за формулою
P2O5 BaO HBr Cl2O7 , KCl
3. Назвіть класифікацію хімічних реакцій
4. Напишіть рівняння реакції заміщення
5. Як визначити валентність у сполуках?
IIІ. Мотивація навчальної діяльності
У йонних сполуках немає спільних пар електронів, тому для цих речовин поняття про валентність не можна використовувати. Для всіх сполук, незалежно від виду хімічних зв’язків, застосовується більш універсальне поняття — ступінь окиснення.
IV. ВИВЧЕННЯ НОВОГО МАТЕРІАЛУ
1. ДАЄМО ПОНЯТТЯ «СТУПІНЬ ОКИСНЕННЯ».
Ступінь окиснення елемента — це умовний заряд атома в речовині, обчислений із припущенням, що вона складається з іонів. Ступінь окиснення характеризує число умовно прийнятих або умовно відданих електронів.
![]()
![]()
![]() Ступінь окиснення
Ступінь окиснення
Позитивним Негативним
(якщо атом віддав електрони (якщо атом
прийняв електрони)
Дорівнювати нулю
Він позначається арабською цифрою зі знаком «плюс» або «мінус» над символом елемента.
2. ПРАВИЛА ВИЗНАЧЕННЯ СТУПЕНЯ ОКИСНЕННЯ.
- Ступінь окиснення атомів в простій речовині дорівнює нулю.
- Атомам деяких хімічних елементів звичайно приписують сталі ступені окиснення. Наприклад, ступінь окиснення Флуору в сполуках завжди дорівнює –1; елементи І, ІІ, ІІІ групи головної підгрупи мають с.о що дорівнює № групи із знаком +.
- Ступінь окиснення Гідрогену в більшості сполук +1, і лише в сполуках з металами він дорівнює –1.
-
Ступінь окиснення Оксигену в більшості сполук –2, і лише в деяких сполуках йому приписують ступінь окиснення –1 (
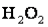 ,
, 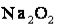 або +2 (
або +2 (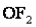 ).
).
- Ступінь окиснення атома металлу побічної підгрупи в сполуках позитивний і чисельно дорівнює його валентності.
- Сума ступенів окиснення всіх атомів у сполуці дорівнює нулю.
- Атоми багатьох хімічних елементів виявляють змінні ступені окиснення.
Преіодична система елементів дає змогу за місцем того чи іншого елемента в ній дізнатися про ступінь його окиснення
Деякі значення ступенів окиснення елементів 3 – го періоду періодичної системи
|
Групи |
I |
II |
III |
IY |
Y |
YI |
YII |
|
Хімічний елемент |
Na |
Mg |
Al |
Si |
P |
S |
Cl |
|
Найвищий позитивний Ступінь окиснення |
+1 |
+2 |
+3 |
+4 |
+5 |
+6 |
+7 |
|
Негативний ступінь окиснення |
|
|
|
-4 |
-3 |
-2 |
-1 |
Номер групи у періодичній системі чисельно дорівнює вищому позитивному ступеню окиснення хімічного елемента даної групи у сполуках з оксисеном.
Наприклад, для сульфуру як елемента шостої групи ступінь окиснення дорівнює+6, для нітрогену, елемента п’ятої групи. +5 , для Барію, елемента другої групи, +2. На підставі теорії будови атома це легко пояснити, Адже зовнішній електронний шар атомів цих елементів містить відповідно 6, 5,2 валентні електрони. Під час взаємодії з більш електронегативними елементом, наприклад з оксисеном, електрони зміщуються в бік Оксигену, а сполучені з ним елементи набувають ступеня окиснення відповідно +6,+5,+2.
Прикладами можуть бути сполуки SO3 P2O5 BaO
+6 -2 +5-2 +2 -2
SO3 P2O5 BaO
Складання формул за ступенями окиснення елементів .
Повторюємо на декількох прикладах порядок складання формул.
Наприклад: скласти формули кальцій нітриду, алюміній сульфіду, натрій фосфіду.
Кальцій нітрид Кальцій - у другій групі - ступінь окиснення +2
Нітроген більш електронегативний, знаходиться у V групі, його ступінь окиснення розраховується - № групи = -3
+2 -3 Cпільне кратне = 6
Сa3 N2
Отже, індекси у формулі будуть відповідно 3 і 2.
Алгоритм складання формули сполуки за відомими ступенями окиснення
• На першому місці у формулі записують елемент з позитивним ступенем окиснення, на другому — з негативним.
• Записують відповідні ступені окиснення.
• Для визначення числових значень ступенів окиснення знаходять найменше спільне кратне.
• Значення найменшого спільного кратного ділять на значення ступеня окиснення.
• Записують індекси.
Користуючись наведеними правилами визначте ступені окиснення атомів елементів у сполуках, формули яких:
N, NO2 , NO, N2O5, N2O, N2O3,H2O, Cu, KCl, H3PO4, Cu3N2, NaClO3, СO2
Назвіть яку ступінь окиснення проявляє Нітроген у сполуках
УЗАГАЛЬНЕННЯ ТА СИСТЕМАТИЗАЦІЯ ЗНАНЬ
Прийом «Вибери мене» ( Робота в групах) клас ділиться на 3 групи
Виберіть формули у яких ступінь окиснення сполученого з Оксисеном елемента найнища і найвища?
1. CO, SO2, Al2O3, Na2O, N2O, Cl2O5
2. Cl2O7 , MnO2, O2 , H2S, NaCl, SO3
3. Mn2O7 ,CrO3, N2O5, H2, AlCl3, NH3
Завдання За відомими валентностями визначіть ступінь окиснення і складіть формули сполук
III YII IY II II I
AlO, ClO , CO, Ba Cl , CaCl.
Підбиття підсумків
Наш урок підійшов до кінця. Сьогодні ми відкрили дверцята у світ нових знань. Ще багато нового нам належить дізнатися і осягнути. Сподіваюся, що урок Вам сподобався.
Домашнє завдання
Скласти формули сполук кислот і визначити ступені окиснення ( не менше 6 )
Тема: . Складання формули сполуки за відомими ступенями окиснення атомів елементів.
Мета: розвивати навички визначення ступеня окиснення в сполуках за формулами, а також за будовою атомів, які утворюють ці сполуки; сформувати навички складання хімічних формул за відомими ступенями окиснення атомів.. На основі набутих знань сприяти розвитку вміння поєднувати теорію з практикою, логічно мислити, робити висновки. Застосовувати математичні методи для розв’язування завдань
Обладнання: : Періодична система хімічних елементів Д. І. Менделєєва, картка-інструкція з визначення ступенів окиснення.
Тип уроку :узагальнення знання
Хід уроку:
Девіз уроку: «Просто знати – це ще не все, знання потрібно використовувати»
Гете
І. Організація класу
Сьогодні гарна погода, і настрій у вас, бачу, теж гарний “Рада вас бачити. Нас чекає сьогодні незвичайний матеріал...”, “Подібне ми вже робили, тому ви з цим завданням легко впораєтесь. Спробуємо закріпити успіх”,
Перевірка домашнього завдання
Гра « Продовжи речення»
- 1. Ступінь окиснення елементів в простих речовинах дорівнює (нулю)
- Ступінь окиснення це умовний заряд атома в речовині, обчислений із припущенням, що вона складається з (іонів)
- Cтупінь окиснення поділяють позитивне,негативне( дорівнює нулю)
- Значення ступеня окиснення і валентності елемента часто( збігається).
- Від чого залежить, який СО елемента у сполуці?
- Пригадайте правила складання формул за відомими ступенями окиснення
Мотивація
Завдання Визначіть ступінь окиснення
Na3PO4, K2CO3, BaSO4, LiNO2. H2O2 Ca3P2; Н3РO4
Вправа « Ти мені, а я тобі»
Один учень називає формулу інший визначає ступінь окиснення, потім навпаки
Робота в парах.
- Пропонуємо учням виконати тренувальні вправи на знаходження ступенів окиснення елементів в сполуках.
CO2 , SO3 , P2 O5 , H2 S , NH3 , Cu , Cu 2S , Cr2 S3 , N2 , O2 , H2.H2SO4. H2S CaSO4 CaO ZnCl2
Робимо перевірку виконання завдання, пояснюємо ще раз , якщо треба.
- Вкажіть формули сполуки, в якій Нітроген виявляє ступінь окиснення +5
NH3, HNO3, NaNO2
- Передбачте мінімальний і максимальний ступені окиснення Селену
Гра «хрестики нулики»
I команда: Обрати лінію, яка сполучає формули сполук, що мають ступінь окиснення+1.
|
Li2O |
Al2O3 |
Fe2O3 |
|
PbO2 |
H2O |
AlCl3 |
|
Cl2O7 |
CuO |
K2O |
ІІ команда: Шляхом до виграшу є оксиди з ступенем окиснення елемента +5
|
N2O5 |
P2O5 |
CL2O5 |
|
SiO2 |
K2O |
SO2 |
|
V2O5 |
CaO |
CuO |
.
IІІ команда: Обрати лінію, яка сполучає формули сполук, що мають ступінь окиснення+3.
|
N2O |
P2O5 |
PbO2 |
|
MgO |
CO2 |
BaO |
|
|
Al2O3 |
|
ЗАКРІПЛЕННЯ ВИВЧЕНОГО МАТЕРІАЛУ
Самостійна робота
1. Вкажіть формулу речовини, в якій Сульфур має вищий ступінь окиснення
А) Na2SO4 Б ) Na2S В )Na2SO4 Г) SCl2
2. Виберіть рядок ступенів окиснення Нітрогену відповідно до послідовності сполук:NH3, N2O , NO2,, N2O5
А) -3,+1,+4,+5 В) -3,+2,+4,+5
Б) +3,+1,+4,+5 Г) -3,+1,+2,+3
3. Складіть формули за відомими ступенями окиснення:
|
Хімічний елемент |
Ступені окиснення |
|||
|
Сулфур |
+2 |
+4 |
+6 |
0 |
|
Хімічний елемент |
Ступені окиснення |
|||
|
Хлор3 |
+7 |
+1 |
+3 |
0 |
|
Хімічний елемент |
Ступені окиснення |
|||
|
Нітроген |
+1 |
+2 |
+3 |
0 |
Складіть формули бінарних сполук і назвіть їх, визначте ступені окиснення
|
Елемент |
Кисень |
Сірка |
Хлор |
|
Ггідроген |
|
|
|
|
Натрій |
|
|
|
|
Магній |
|
|
|
Прослідкуйте чи змінюються ступені окиснення
![]() Mg +O2 2 MgO
Mg +O2 2 MgO
![]() Zn +2 HCl ZnCl2 +H2
Zn +2 HCl ZnCl2 +H2
.Проблемні запитання до всіх учнів:
а) Чи змінюється стпупінь окиснення атомів елементів до і після реакції?
б) Чи відображає це тип реакції (сполучення, заміщення, розкладу, обміну)?
Робота в парі – скласти формули сполук за відомими ступенями окиснення (2-3 хв)
+1 -2 -3 +1 +1 -2 +3 -2 +2 -2 +1 +4 -2 +1 +6 -2
NaO, PH, HS, AlO, CuO, HCO, HSO.
ПІДБИТТЯ ПІДСУМКУ УРОКУ
«Що ти дізнався за урок? Як ти займався на уроці? Чи задоволений тим, як пройшов урок? »
Домашнє завдання
- Скласти формули складних речовин і визначити ступені окиснення 10 прикладів
- Повторити правила складання формул за відомими ступенями окиснення


про публікацію авторської розробки
Додати розробку
