Урок: «Оцтова кислота, її молекулярна та структурна формули, фізичні властивості. Функціональна (характеристична) карбоксильна група. Застосування оцтової кислоти».
Мета:
üсформувати знання учнів про карбоксильну функціональну групу на прикладі оцтової кислоти;
Завдання:
навчальні: ознайомити учнів зі структурною й електронною формулами оцтової кислоти;
виховні: виховувати науковий світогляд учнів, сприяти естетичному, екологічному вихованню;
розвивальні:розвивати вміння досліджувати, спостерігати, робити висновки та узагальнення
Методи проведення: словесний: розповідь - пояснення, опис, бесіда, робота
з підручником; словесно - наочний: ілюстрація.
Тип уроку: засвоєння нових знань.
1
Фесенко Юлії Дмитрівни 9 клас 20.03. 2018 р.
Конспект уроку з хімії
Тема: «Оцтова кислота, її молекулярна та структурна формули, фізичні властивості. Функціональна (характеристична) карбоксильна група. Застосування оцтової кислоти».
Мета:
- сформувати знання учнів про карбоксильну функціональну групу на прикладі оцтової кислоти;
Завдання:
- навчальні: ознайомити учнів зі структурною й електронною формулами оцтової кислоти;
- виховні: виховувати науковий світогляд учнів, сприяти естетичному, екологічному вихованню;
- розвивальні: розвивати вміння досліджувати, спостерігати, робити висновки та узагальнення
Методи проведення: словесний: розповідь - пояснення, опис, бесіда, робота
з підручником; словесно - наочний: ілюстрація.
Тип уроку: засвоєння нових знань.
ПЛАН УРОКУ
I. Організаційний етап …………………………………………………………....3 хв.
II. Актуалізація опорних знань……………………………………………………2 хв.
III. Мотивація навчальної діяльності……………………………………………..5 хв.
IV. Пояснення нового матеріалу…………………………………………….......20 хв.
V. Закріплення нового матеріалу…………………………………………….... 10 хв.
VI. Підбиття підсумків уроку та повідомлення домашнього завдання……..…...5 хв.
Хід уроку
- Організаційний етап.
Добрий день! Сідайте. Скажіть, хто сьогодні на уроці відсутній?
- Актуалізація опорних знань (Перевірка дз)
- Що ми вивчали на минулому уроці?
- Написати загальну формулу спиртів
- Написати структурну формулу етанолу та пропанолу
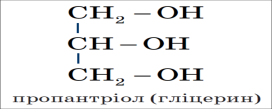
- Назвати представників багатоатомних спиртів, написати формули
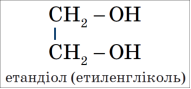
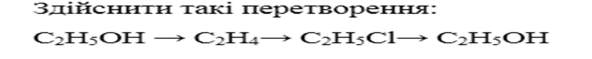
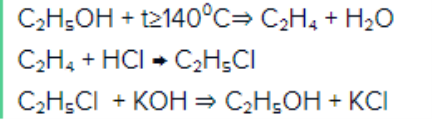
- Мотивація навчальної діяльності.
Чи знаєте Ви про таку кислоту,
Яку повсякчас додаєм до борщу,
ЇЇ ми кладемо завжди в маринад
Для всяких смачнючих солінь і принад?
Ну звичайно, це оцтова кислота, а в побуті – оцет (6, 9, 12%).
Аналогічно спиртам до оксигеновмісних органічних сполук належать карбонові кислоти. Одного з представників карбонових кислот ми сьогодні і будемо вивчати. Записуємо тему уроку.
IV. Пояснення нового матеріалу.
Клас карбонових кислот відрізняється від спиртів наявністю в молекулах нової функціональної групи – карбоксильної:
![]() – СООН
– СООН
Назва карбоксильної групи походить від двох груп, що входять до її складу:
карбонільної та гідроксильної.
– С = О – ОН
Карбонові кислоти – це похідні вуглеводнів, що містять одну або декілька карбоксильних груп.
Загальна формула одноосновних насичених карбонових кислот:
CnH2n+1COOH або RCOOH
Класифікація карбонових кислот
За природою вуглеводневого радикала (за наявністю кратних
зв’ язків у вуглеводневих залишках молекул):
- насичені
- ненасичені
- ароматичні.
За кількістю гідроксильних груп:
- одноосновні (одна група ОН)
- двохосновні (дві групи ОН)
За кількістю карбоксильних груп у молекулі кислоти:
- монокарбонові (молекули містять одну групу – СООН)
- дикарбонові (молекули містять дві групи – СООН)
Добре, тепер у себе в зошитах малюємо таку табличку:
Гомологічний ряд одноосновних насичених карбонових кислот
|
CnH2n+1COOH |
Назва кислоти |
Назви солей |
|
Н - СООН |
Мурашина(метанова) |
Форміати |
|
СН3 - СООН |
Оцтова(етанова) |
Ацетати |
|
С2Н5 - СООН |
Пропіонова (пропанова) |
Пропіонати |
|
С3Н7 - СООН |
Бутанова (масляна) |
Бутирати |
Відповідно до систематичної номенклатури, назви кислот походять від назв відповідних вуглеводнів з додаванням закінчення –ова.
Робота з підручником с. 184
Карбонові кислоти:
- нижчі (їхні молекули містять менше 10 атомів Карбону)
- вищі жирні кислоти – бо добували з рослинних і тваринних жирів (їхні молекули містять більше 10 атомів Карбону) С15Н31 – СООН пальмітинова або гексадеканова; С17Н35 – СООН стеаринова; С17Н33 – СООН олеїнова (ненасичена).
З деякими карбоновими кислотами вам доводилось стикатись. Пекучий біль від укусу мурашки спричинений мурашиною кислотою, що входить до складу отрути, яку виділяє комаха. Столовий оцет – це розчин оцтової кислоти. Масляна кислота надає неприємних запаху і смаку згірклому вершковому маслу, вона виділяється також потовими залозами людини.
Давайте напишемо молекулярну, структурну та електронну формулу оцтової кислоти (ацетатної, етанової):
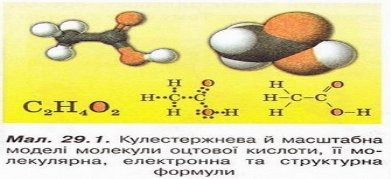
До складу молекули оцтової кислоти входять 2 атоми О, один з них міститься в гідроксильній групі. Другий атом О сполучений подвійним зв’язком з тим самим атомом С, до якого приєднана й гідроксильна група. Групу атомів
С = О називають карбонільною групою. Поєднавши фрагменти слів карбонільна і гідроксильна, дістанемо назву функціональної групи карбонових кислот – карбоксильна група.
Фізичні властивості
Перші три кислоти гомологічного ряду за стандартних умов (t = 25 оС) рідини з різким кислим запахом, добре розчинні у воді; наступні шість – оліїсті рідини з неприємним запахом; починаючи з кислоти з десятьма атомами Карбону в молекулі, - тверді речовини.
Оцтова кислота — за кімнатної температури безбарвна рідина з різким характерним запахом. За температури нижчої за 17ОС (температура плавлення) кристалізується і стає схожою на лід, тому її називають «крижаною» оцтовою кислотою. Температура кипіння 118ОС. Розчиняється у воді в будь - яких кількостях: 9%-й розчин називається оцтом, 70—80%-й розчин — оцтовою есенцією.
Застосування оцтової кислоти
Застосування оцтової кислоти досить різноманітне. У хімічній промисловості з неї виробляють пластичні маси, різні барвники, лікарські речовини, штучне волокно (ацетатний шовк), незаймисту кіноплівку та багато інших речовин. Солі оцтової кислоти – ацетати алюмінію, хрому, феруму – застосовують як протиотруту при фарбуванні тканин. Оцтова кислота має широке застосування і як розчинник. У харчовій промисловості застосовується як консервувальний засіб та смакова приправа. Е - 260
- Закріплення нового матеріалу
Цікаво знати…Як визначити якість пива?
Щоб визначити і переконатися, що гіркота в пиві не додана штучно і має природне походження, необхідно додати до пива невелику кількість оцтової кислоти. У рідині при цьому відразу ж випаде осад. Так осаджується хміль, який надає пиву характерну гіркоту. Потім рекомендується продовжити підливати оцет, поки не припиниться утворення осаду, і дати суміші відстоятися. І вже після цього пробувати рідину на смак.
Якщо пиво начисто втратило гіркий смак, значить домішок у ньому не було. Але якщо рідина продовжує гірчити, значить, гіркоту пива додана штучно. Вся справа в тому, що виробники-фальсифікатори для штучного посилення гіркоти пива додають до нього відвар гірких, часто шкідливих, трав. Оцтова кислота може осаджувати лише хміль, а сторонні гіркі домішки, як правило, залишаються неосажденими.
Іноді фальсифікатори для надання пиву гіркоти додають пікрінову кислоту, дуже шкідливу для людського організму. Щоб визначити її нехай навіть дуже малу присутність, потрібно прокип’ятити в пиві протягом 10 хвилин шматочок чистої білої вовняної тканини, після чого добре прополоскати її у воді. Якщо матерія забарвилася в жовтий колір, таке пиво пити не можна.
Метод «Мікрофон»
Що сьогодні на уроці ви дізнались нового та цікавого?
V. Підбиття підсумків уроку та повідомлення домашнього завдання
Опрацювати § 33 ст. 184 – 187
* Підготувати реферат з малюнками й титулом про будь – яку карбонову кислоту, про її фізичні властивості та застосування.


про публікацію авторської розробки
Додати розробку
