Урок та Презентація "Узагальнююче повторення. Розв'язування задач за періодичною системою елементів Д.І.Менделєєва.
Урок та презентація до нього на тему "Узагальнююче повторення.
Розвязування задач за періодичною системою елементів Д.І.Менделєєва."
Українська ЗЗСО І-ІІІ ступенів Коблевської сільської ради
ПОКАЗОВИЙ УРОК ХІМІЇ В 8 КЛАСІ
на тему:
Узагальнююче повторення.
Розвязування задач за періодичною системою елементів Д.І.Менднлєєва.
Вчитель І категорії
Самойлова Т.М.
2018-2019 н.р.
Цілі: формування ключових компетентностей:
саморозвитку і самоосвіти створення проблемних ситуацій, уміння розв’язувати задачі;
інформаційної – відпрацювання вмінь робити висновки і узагальнення;
соціально-трудової – вміти оперувати знаннями, розвивати гнучкість отримання знань;
комунікативної – вміння працювати в групі.
Формування предметних компетентностей: узагальнити і систематизувати знання з теми, розвивати вміння і навички користуватися періодичною системою, складання електронних схем і формул будови атомів хімічних елементів з їхніми властивостями; закріпити вміння розв’язування логічних і розрахункових задач з використанням періодичного закону й періодичної системи.
Обладнання: періодична система хімічних елементів Д.І. Менделєєва, картки із завданням, алгоритм характеристики елемента, ПК та проектор.
Тип уроку: узагальнення і систематизація знань.
Хімія – це край чудес,
де приховане людське щастя.
І найвищі завоювання розуму
будуть зроблені в цій галузі.
Д.І. Менделєєв
Хід уроку:
 І. Організація уроку та мотивація.
І. Організація уроку та мотивація.
Добрий день діти, здрастуйте шановні гості!(пауза, поки діти сіли на свої місця) Хімія – це край чудес,де приховане людське щастя. І найвищі завоювання розуму будуть зроблені в цій галузі. Спонуканням до діяльності на уроці звучали слова Дмитра Івановича Менделєєва
 ІІ. Оголошення теми і завдань уроку.
ІІ. Оголошення теми і завдань уроку.
Урок проведеться у незвичній для вас формі, клас заздалегідь я поділила на 2 команди Метали(хлопці) і Неметали (дівчата). Ваше завданням на сьогодні: змагаючись із суперниками збагатити свій розум і достойно підготуватися до контрольної роботи на наступному уроці. Отже записуємо тему уроку:
Узагальнююче повторення. Розв’язування задач за періодичною системою елементів.
А зараз, учасники, пропоную вам обрати капітанів команд функції якого є роздавання отриманих балів (кольорових паличек), виявлення активних учнів під час розв’язання командних завдань.
ІІІ. Актуалізація опорних знань
- Перевірка ДЗ
Характеристика елемента №6. (Вчитель на екрані по черзі розкриває відповіді на кожне питання за планом характеристики). Взаємоперевірка з оцінюванням.
|
|
№ 6 |
|
І. Місце елемента в П.С.: |
|
|
1)назва елемента; |
Карбон |
|
2)відносна атомна маса елемента; |
Ar(C)=12 |
|
3)номер періоду (малий чи великій) |
2, малий |
|
4)номер групи (головна чи побічна підгрупа) |
IV, головна |
|
ІІ. Будова атома: |
|
|
1)знак хімічного елемента, протонне, нуклонне число; |
|
|
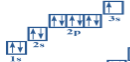
2)електронна схема, електронна формула, графічний розподіл електронів по комірках; |
|
|
3)протони, електрони,нейтрони; |
Протонів – 6, електронів – 6, нейтронів – 6. |
|
4)кількість неспарених електронів; |
два |
|
5)кількість електронів на зовнішньому шарі; |
4 |
|
ІІІ. Властивості елемента і його сполук: |
|
|
1)проста речовина,формула,метал чи неметал; |
проста речовина графіт, сажа, вуглець, С, неметал |
|
2)формула вищого оксиду, його характер; |
СО2, кислотний |
|
3)формула гідроксиду, що відповідає вищому оксиду, його характер; |
H2CO3, кислотний |
|
4)формула леткої сполуки з Гідрогеном (для неметалів); |
СH4 |
|
5)рівняння реакцій утворення вищого оксиду та гідроксиду. |
C+O2=CO2 CO2+H2O=H2CO3 |
2. Теоретичні питання. Гра «Хрестики Нулики» (Капітани команд обирають по 2 учасники, які змагаються з суперниками біля дошки, оперуючи символами елементів металів або неметалів - відповідно назві
команди)
3. Закінчи речення (на екрані почергово з’являються речення, за правильне продовження якого учасник отримує 1 бал)
- Горизонтальний ряд елементів, що починається лужним металом і закінчується інертним газом, - це …
- Стовпчик, який містить елементи з подібними властивостями, - це …
-
 Вкажіть кількість малих періодів у Періодичній системі Д. І. Менделєєва …
Вкажіть кількість малих періодів у Періодичній системі Д. І. Менделєєва …
- Нітроген розташований у …
- Алюміній розташований у …
- Протонне число фосфору…
- Нуклонне число Арсену …
- 12й хімічний елемент періодичної ...
-
 Найменша хімічно неподільна електронейтральна частинка речовини – це ….
Найменша хімічно неподільна електронейтральна частинка речовини – це ….
- Вид атомів з однаковим протонним числом - …
- Атом з певним числом протонів і нейтронів у ядрі називають ….
- Частинку із зарядом 0 та масою 1 називають …
- Частинку із зарядом +1 та масою 1 називають …
- Навколо ядра атоми рухаються….
- Заряд ядра атома дорівнює …
- Кількість протонів у ядрі визначається за …
- Вкажіть кількість електронів у атомі Карбону.
- Визначте елемент, який має 15 протонів.
- Визначте елемент, який має заряд ядра атома +35.
IV. Розв’язування задач і вправ
1. Хімічний диктант(робота в групах)
Виконавши роботу, капітан зачитує результат та отримує бали відповідно кількості правильних відповідей, які розподіляє між учасниками команди за активністю.
Лужні метали
- До лужних металів належать:
- ….
- ….
- …..
- …..
- ….
- ….
- Валентність у сполуках - ….
- Загальна формула оксидів - …
- Загальна формула гідрооксидів - …
- Виходячи із загальної формули оксидів, складіть формули оксидів перших чотирьох елементів:
а) ….; б) ……; в)….; г)…. .
- Атом- найдрібніша частинка речовини, що складається з ……….. та ………оболонки.
- Протони – частинки із зарядом …… і масою…….. .
Галогени
- Ядра атомів складаються з ….., які поділяються на…… і…….
- Нейтрони - …… частинки масою …. .
- Группу галогенів утворюють елементи:….
а)…; б)….; в) ….; г)….; д)…. ..
- Молекули простих речовин складаються з … .
- Формули простих речовин перших чотирьох:
а)…; б)….; в) ….; г)…. .
- У сполуках з металами та Гідрогеном - … .
- У вищих оксидах валентність …. за винятком …. .
2. Хто швидше. (Самостійна робота. Найшвидший виконавець отримує 3 бали за правильну відповідь, Хто не розв’язав задачу, знайомиться з розв’язком на екрані.)
Задача
 Метали
Метали
Оксид хімічного елемента І групи головної підгрупи має формульну масу 94, назвіть хімічний елемент, покажіть будову його атома
Розв’язок:
|
Дано: X2O Mr(X2O)=94 |
|
Х- ? |
2х+16=94
2х=78
х=39, Калій (К2О)
Відповідь: Калій
Задача
Неметали
Елемент утворює легку сполуку з гідрогеном типу RH. Відносна молекулярна маса вищого оксиду цього елемента дорівнює 272. Який це елемент? Вкажіть кількість протонів і нейтронів у ядрі його атома.
Розв’язок:
|
Дано: (RH)=VII в M(R2O7)=272 |
|
R- ? |
2*х+7*16=272
2х=272-112
2x=160
x=80, Бром (Br)
Відповідь: Бром
3. Характеристика хімічного елемента за положенням в періодичній системі.
(взаємоперевірка, капітани команд, учасники команди переможець отримують по 1 балу)
|
|
№ 11 Метали |
№ 17 Неметали |
|
І. Місце елемента в П.С.: |
||
|
1)назва елемента; |
Натрій |
Хлор |
|
2)відносна атомна маса елемента; |
Ar(Na)=23 |
Ar(Сl)=35.5 |
|
3)номер періоду (малий чи великій) |
3-й період, малий |
3-й період, малий |
|
4)номер групи (головна чи побічна підгрупа) |
І гр.. головна |
VІІ гр.. головна |
|
ІІ. Будова атома: |
||
|
1)знак хімічного елемента, протонне, нуклонне число; |
|
|
|
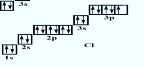
2)електронна схема, формула, графічний розподіл електронів по комірках; |
|
|
|
3)протони, електрони,нейтрони; |
протонів 11, нейтронів 12 |
протонів 17, нейтронів 18 |
|
4)кількість неспарених електронів; |
1 електрон |
1 електрон |
|
5)кількість електронів на зовнішньому шарі; |
1 електрон |
7 електронів |
|
ІІІ. Властивості елемента і його сполук: |
||
|
1)проста речовина,формула,метал чи неметал; |
Проста, Na |
проста, |
|
2)формула вищого оксиду, його характер; |
|
|
|
3)формула гідроксиду, що відповідає вищому оксиду, його характер; |
NaOH - основа |
|
|
4)формула леткої сполуки з Гідрогеном (для неметалів); |
не утворює |
HCl |
|
5)рівняння реакцій утворення вищого оксиду та гідроксиду. |
|
|
 V. Підсумок
V. Підсумок
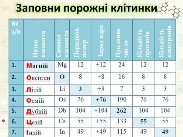
Заповни порожні клітини (по черзі)
|
з/п |
Назва елемента |
Символ елемента |
Порядков. номер |
Заряд ядра |
Нуклонне число |
Кількість протонів |
Кількість
|
|
|
Магній |
Mg |
12 |
+12 |
24 |
12 |
12 |
|
|
Оксиген |
O |
8 |
+8 |
16 |
8 |
8 |
|
|
Літій |
Li |
3 |
+3 |
7 |
3 |
3 |
|
|
Осмій |
Os |
76 |
+76 |
190 |
76 |
76 |
|
|
Дубній |
Db |
105 |
+105 |
262 |
105 |
105 |
|
|
Цезій |
Cs |
55 |
+55 |
133 |
55 |
55 |
|
|
Індій |
In |
49 |
+49 |
115 |
49 |
49 |

VI. Домашнє завдання
- підготуватися до КР
- повторити теоретичний матеріал розділу
- Дати відповіді на запитання заповнюючи кросворд у підручнику №5 стор. 70
VІІ. Рефлексія.
Підвидемо підсумки уроку, пропоную дати відповідь на запитання
 Чим я збагатив свій розум?
Чим я збагатив свій розум?
|
Команда «Метали» |
||||
|
|
Прізвище, ім’я учня |
Посада (капітан чи учасник) |
Кількість балів |
Оцінка (виставляє учитель) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Всього балів: |
|
|
||
ДОДАТКИ
|
Команда «Неметали» |
||||
|
|
Прізвище, ім’я учня |
Посада (капітан чи учасник) |
Кількість балів |
Оцінка (виставляє учитель) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Всього балів: |
|
|
||
1


про публікацію авторської розробки
Додати розробку