Урок з хімії на тему: "Карбонові кислоти"
- Балан Л.О. хімія.docx docx
- ПРЕЗЕНТАЦІЯ.ppt ppt
ДНЗ “КРИЖОПІЛЬСЬКИЙ ПРОФЕСІЙНИЙ БУДІВЕЛЬНИЙ ЛІЦЕЙ”
МЕТОДИЧНА РОЗРОБКА УРОКУ
З ХІМІЇ
НА ТЕМУ:
“Карбонові кислоти, їх поширення в природі та класифікація. Карбоксильна характеристична (функціональна) група. Склад, будова молекул насичених одноосновних карбонових кислот, їхня загальна та структурні формули, ізомерія, систематична номенклатура і фізичні властивості”

Викладач: Балан Людмила Олександрівна
Крижопіль
2023р.
Тема : Карбонові кислоти, їх поширення в природі та класифікація. Карбоксильна характеристична (функціональна) група. Склад, будова молекул насичених одноосновних карбонових кислот, їхня загальна та структурні формули, ізомерія, систематична номенклатура і фізичні властивості.
Мета:
- Формування ключових компетентностей:
o Спілкування державною мовою;
o Уміння вчитися впродовж життя;
o Екологічна грамотність і здорове життя;
o Основні компетентності у природничих науках і технологіях;
o Інформаційно-цифрова компетентність;
o Соціальна та громадянська компетентності;
- Формування предметних компетентностей:
o Дати поняття «карбонові кислоти», їх поширення у природі та класифікацію, уявлення про карбоксильну характеристичну групу; вивчити склад, будову молекул насичених одноосновних карбонових кислот, їхню загальну та структурні формули, ізомерію, систематичну номенклатуру; фізичні властивості насичених одноосновних карбонових кислот.
o Розвивати хімічну мову, логічне й екологічне мислення, вміння аналізувати;
o Виховувати здоровий спосіб життя;
o Виховувати інтерес до вивчення хімії.
Тип уроку: вивчення нового матеріалу.
Засоби навчання
Мережні: інтернет-ресурс:
- Підручник: Попель П.П. Хімія (рівень стандарту): підруч. для 10 кл. закладів загальної середньої освіти/ П.П. Попель, Л.С. Крикля.- Київ: ВЦ “Академія”, 2018.–§ 18, 19 с. 109-120.
https://dtek.dp.ua/wp-content/uploads/2018/10/ximiya_10_kl_popel.pdf
- Навчальна гра «Класи органічних сполук»
- https://learningapps.org/watch?v=peuassjok23
- Навчальна гра «Знайти відповідність»
https://learningapps.org/watch?v=puj30q6ka23
-презентація про карбонові кислоти в природі та житті людини
-Тест-контроль «Карбонові кислоти»
https://naurok.com.ua/test/karbonovi-kisloti-2104759.html
Хід уроку
І. Організаційний момент.
ІІ. Оголошення теми й мети уроку.
ІІІ. Актуалізація опорних знань .
Завдання за допомогою сервісу learningApps.Org «Класифікація органічних сполук»
Навчальна гра «Класи органічних сполук»
https://learningapps.org/watch?v=peuassjok23
ІV. Мотивація навчальної діяльності
Хіба ми можемо уявити життя без цієї речовини? Без маринованих огірочків, грибів? Всі ми знаємо запах цієї речовини і не сплутаємо його ні з якою іншою речовиною. Скажіть, будь ласка, з якою речовиною ми ознайомимось сьогодні на уроці? Так, ми ознайомимося з основною складовою частиною столового оцту – з оцтовою кислотою.
Сьогодні ми вивчаємо речовини, які можна назвати «Знайомі незнайомці».
Зверніть, будь ласка, увагу на продукцію (лимон, столовий оцет, щавель, кефір, яблуко, квашена капуста). Що в них спільного?
(Вони мають кислий смак. Містять органічні кислоти.)
Навчальна гра «Знайти відповідність»
https://learningapps.org/watch?v=puj30q6ka23
В ході гри ви переконалися, що продукція, яку ми використовуємо в побуті, містить органічні кислоти.
V. Вивчення нового матеріалу
1. Знаходження в природі
⮚ Мурашина кислота виробляється мурахами, знаходиться у кропиві і в хвої ялини.
⮚ Масляна кислота – утворюється у разі прогіркання масла, є запахом поту.
⮚ Капронова кислота - входить до складу козячого масла.
⮚ Ізовалеріанова кислота – в коренях валеріани лікарської.
⮚ Стеаринова і пальмітинова кислота – виділені з пальмової олії.
⮚ Щавлева кислота - в щавлі, ревені, кислиці, шпинаті.
⮚ Яблучна кислота – яблука.
⮚ Лимонна кислота - апельсин, грейпфрут, лимон.
⮚ Оцтова кислота – утворюється при прокисанні вина
2. Поняття про карбонові кислоти.
Карбонові кислоти — це органічні речовини, молекули яких містять одну або кілька карбоксильних груп, сполучених з вуглеводневим радикалом або водневим атомом.
3. Функціональна група й будова карбонових кислот.
. 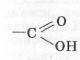 - карбоксильна група. Назву отримала від поєднання двох груп атомів карбонільної і гідроксильної.
- карбоксильна група. Назву отримала від поєднання двох груп атомів карбонільної і гідроксильної.
Загальна формула має вигляд: СnH2n+1COOH або R – COOH
4. Карбонові кислоти класифікують:
а) залежно від кількості карбоксильних груп у молекулі — на одноосновні, двохосновні та багатоосновні;
Перегляньте презентацію про карбонові кислоти .
5. Гомологічний ряд і номенклатура карбонових кислот.
Назви насичених одноосновних карбонових кислот згідно з правилами IUPAC будують з назви відповідного вуглеводню з додаванням суфікса -ов і закінчення -а.
Перед коренем назви записують бічні замісники, зазначають їхнє положення й кількість. Нумерацію карбонового ланцюга починають з атома Карбону карбоксильної групи.
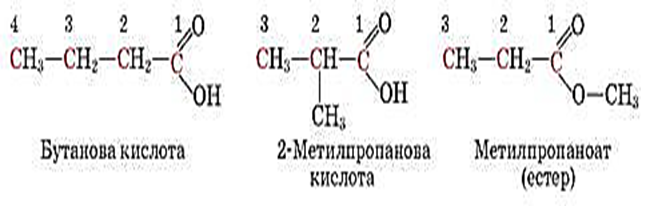
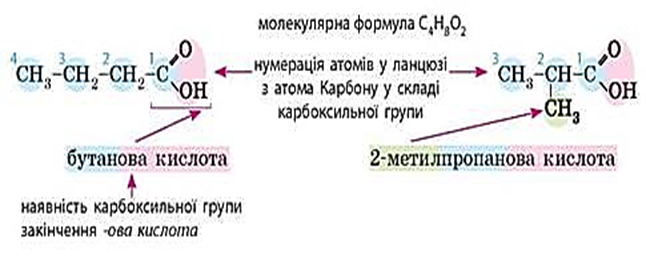
.
НАЗВИ КАРБОНОВИХ КИСЛОТ І ЇХНІХ СОЛЕЙ
|
Формула |
Назва |
Сіль |
|
|
IUPAC |
традиційна |
||
|
HCOOH |
Метанова |
Мурашина |
Форміат |
|
CH3COOH |
Етанова |
Оцтова |
Ацетат |
|
CH3CH2COOH |
Пропанова |
Пропіонова |
Пропіоат |
|
CH3 (CH2 )2COOH |
Бутанова |
Масляна |
Бутилат |
|
CH3 (CH2 )3COOH |
Пентанова |
Валеріанова |
Валеріат |
|
CH3 (CH2 )4COOH |
Гексанова |
Капронова |
Капронат |
|
СІ5Н31СООН |
Гексадеканова |
Пальмітинова |
Пальмітат |
|
СІ7Н35СООН |
Октадеканова |
Стеаринова |
Стеарат |
6. Фізичні властивості карбонових кислот.
Нижчі карбонові кислоти — рідини з гострим запахом, добре розчинні у воді. З підвищенням відносної молекулярної маси розчинність кислот у воді зменшується, а температура кипіння підвищується. Вищі кислоти, починаючи з пеларгонової (нонанової) СН3—(СН2)7—СООН,— тверді речовини, без запаху, нерозчинні у воді.
ФІЗИЧНІ ВЛАСТИВОСТІ КАРБОНОВИХ КИСЛОТ
|
Формула
|
Назва |
t пл. С |
t кип. С |
Розчинність у воді |
|
НСООН |
Мурашина |
8,2 |
100,7 |
Необмежено |
|
СН3СООН |
Оцтова |
16,6 |
117,7 |
Необмежено |
|
С2Н5СООН |
Пропіонова |
-20,8 |
140,8 |
Необмежено |
|
С3Н7СООН |
Масляна |
-5,3 |
163,3 |
Добре |
|
С4Н9СООН |
Валеріанова |
-34,5 |
186,4 |
Погано |
|
С5Н11СООН |
Капронова |
-3,9 |
205,3 |
Погано |
|
СІ5Н31СООН |
Пальмітинова |
52,5 |
390 |
Не розчиняється |
|
СІ7Н35СООН |
Стеаринова |
71,0 |
432 |
Не розчиняється |
Необхідно відзначити такі властивості кислот, як їхня порівняно мала леткість, розчинність у воді одних і нерозчинність інших. У встановленні водневих зв'язків беруть участь атоми Оксигену гідроксильних груп. Унаслідок рухливості π-зв'язку електронна густина на карбонільному атомі Оксигену більша, він переважно бере участь в утворенні водневих зв'язків.
Оскільки в молекулах кислот одночасно присутні й негативно, й позитивно заряджені атоми, можуть утворюватися подвоєні молекули — дімери з двома водневими зв'язками:
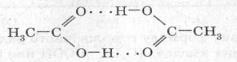
У такому випадку асоціація молекул виявляється більш міцною, ніж за наявності одного водневого зв'язку.
7. Електронна будова карбоксильної групи.
Електронні взаємодії в карбоксильній груді досить складні, спостерігається сполучення неподіленої електронної пари гідроксильного Оксигену з електронами π-зв'язку.
В результаті зсуву електронної густини подвійного зв'язку до Оксигену атом Карбону набуває надлишкового позитивного заряду. З цієї причини електрони гідроксильного атома Оксигену (неподілені електрони й електрони зв'язку С = О) зміщуються до атома Карбону, а в результаті зниження електронної густини на атомі Оксигену до нього зміщуються електрони зв'язку О—Н. Атом Гідрогену у зв'язку з цим легше відщеплюється у вигляді протона, що й зумовлює кислотні властивості речовини. Зсув електронної густини зв'язків у карбоксильній групі можна виразити такою формулою:
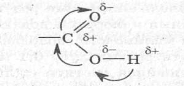
Зсув електронної густини від гідроксильного атома Оксигену до атома Карбону трохи зменшує на ньому позитивний заряд, а отже, і полярність зв'язку С = О , тому варто очікувати зниження реакційної здатності карбонільної групи.
Завдання 1
https://dtek.dp.ua/wp-content/uploads/2018/10/ximiya_10_kl_popel.pdf
Використовуючи електронний навчальний ресурс теми “Карбонові кислоти” на с 109-111:
● визначити поняття: “карбонові кислоти”, “карбоксильна група”, “загальна формула ”;
● дати відповідь на питання:
- Які карбонові кислоти називають одноосновними, двохосновними,
багатоосновними?
- Які карбонові кислоти називають нижчими, вищими?
- Які карбонові кислоти називають насиченими, ненасиченими, ароматичними?
Завдання 2
https://dtek.dp.ua/wp-content/uploads/2018/10/ximiya_10_kl_popel.pdf
За матеріалами інтернет-ресурсу або презентацією проаналізуйте дані таблиці 3 с. 112 «Формули і назви одноосновних насичених карбонових кислот та їх солей» і поясніть як утворюються систематичні назви карбонових кислот.
Таблиця 3 Формули і назви одноосновних насичених карбонових кислот та
їх солей
|
Формула
|
Назва IUPAC |
Традиційна назва |
Назва кислотного залишку |
|
HCOOH |
Метанова |
Мурашина |
Метаноат (форміат) |
|
CH3COOH |
Етанова |
Оцтова |
Етаноат (ацетат) |
|
CH3CH2COOH |
Пропанова |
Пропіонова |
Пропаноат (пропіонат) |
|
CH3 (CH2 )2COOH |
Бутанова |
Масляна |
Бутаноат (бутилат) |
|
CH3 (CH2 )3COOH |
Пентанова |
Валеріанова |
Пентаноат (валерат) |
|
CH3 (CH2 )4COOH |
Гексанова |
Капронова |
Гексаноат (капронат) |
|
CH3 (CH2 )14COOH |
Гексадеканова |
Пальмітинова |
Пальмітат |
|
CH3 (CH2 )16COOH |
Октадеканова |
Стеаринова |
Стеарат |
Завдання 3. Практика… Досвід…
Записати ізомери для пентанової кислоти С4Н9СООН та назвати їх згідно міжнародної систематичної номенклатури:
Очікувана відповідь:
![]()
![]()
![]() 5 4 3 2 1 О 4 3 2 1 О 4 3 2 1 О
5 4 3 2 1 О 4 3 2 1 О 4 3 2 1 О
![]()
![]() СН3- СН2 – СН2 –СН2 -С СН3- СН2 – СН –С СН3 – СН – СН2 –С
СН3- СН2 – СН2 –СН2 -С СН3- СН2 – СН –С СН3 – СН – СН2 –С
![]() пентанова ОН СН3 ОН СН3 ОН
пентанова ОН СН3 ОН СН3 ОН
2-метилбутанова 3-метилбутанова
![]()
![]() СН3 О
СН3 О
![]() СН3- С – С
СН3- С – С
СН3 ОН
2,2-диметилпропанова
V. Узагальнення знань, формування вмінь, навичок, компетенцій
1. Вправа «Хімічний диктант»(вставити пропущені слова)
1. Карбонові кислоти – це … речовин, молекули яких містять … або кілька … груп СООН, сполучених з вуглеводневим радикалом.
2. Основність … кислот залежить від кількості … груп.
3. Карбонові кислоти, що мають одну … групу, називаються ….
4. Група атомів 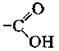 складається з … та … групи.
складається з … та … групи.
5. Загальна формула одноосновних карбонових кислот СnН2n+1СООН або R-COOH.
6. Назви … кислот походять від назви відповідного … з додаванням закінчення - … і слова …
Тест-контроль «Карбонові кислоти»
Освітній портал «На Урок».
https://naurok.com.ua/test/karbonovi-kisloti-2104759.html
VI. Підведення підсумків уроку та повідомлення домашнього завдання
- опрацювати за електронним підручником Попель П.П. Хімія (рівень стандарту): підруч. для 10 кл. закладів загальної середньої освіти/ П.П. Попель, Л.С. Крикля.- Київ: ВЦ “Академія”, 2018,
с. 124-135.
https://dtek.dp.ua/wp-content/uploads/2018/10/ximiya_10_kl_popel.pdf


про публікацію авторської розробки
Додати розробку
















