Уроку. "Узагальнення й систематизація знань з теми «Хімічні реакції»"
Урок № 9. Тема уроку. Узагальнення й систематизація знань з теми «Хімічні реакції»
Мета уроку: узагальнити і систематизувати знання учнів про класифікації хімічних реакцій, кінетику і термодинаміку хімічних реакцій; вдосконалювати вміння писати рівняння хімічних реакцій, вказувати тип реакції за різними ознаками; вдосконалювати вміння розв’язувати тестові завдання, задачі.
Обладнання: мультимедійна презентація уроку, періодична система хімічних елементів, таблиця розчинності, ряд активності металів, картки із завданнями.
Тип уроку: урок узагальнення й систематизації знань.
Девіз уроку. Знання лише тоді стають переконаннями, якщо вони досягнуті зусиллями думки.
Хід уроку
І. Мотивацій навчальної діяльності.
 А.Ф. Лосєв якось сказав: «Будь-який труд є осмисленим, результативним та вільним тільки тоді, коли він усвідомлюється як моя особиста … необхідність». Як ви розумієте ці слова? Як ви думаєте, яка мета нашого уроку? (Слайд 1)
А.Ф. Лосєв якось сказав: «Будь-який труд є осмисленим, результативним та вільним тільки тоді, коли він усвідомлюється як моя особиста … необхідність». Як ви розумієте ці слова? Як ви думаєте, яка мета нашого уроку? (Слайд 1)
Мета уроку: повторити і узагальнити матеріал з теми «Хімічні реакції», підготуватися до контрольної роботи. (Слайд 2)
ІІ. Узагальнення й систематизація знань.
1. Ознаки класифікацій хімічних реакцій . (Слайд 3)
2. Класифікація хімічних реакцій за зміною числа реагентів і продуктів реакції, та їх складом. (Слайд 4)
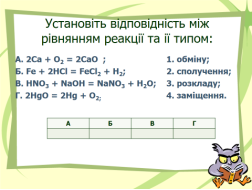 3. Установіть відповідність між рівнянням реакції та ії типом: (Слайд 5)
3. Установіть відповідність між рівнянням реакції та ії типом: (Слайд 5)
-
 Класифікація хімічних реакцій за зміною ступенів окиснення. (Слайд 6)
Класифікація хімічних реакцій за зміною ступенів окиснення. (Слайд 6)
5. Дано схеми двох рівнянь, допишіть рівняння реакцій. (Слайд 7)
6. Класифікація хімічних реакцій за тепловим ефектом. (Слайд 8)
7. Вкажіть, які реакції із даних є екзотермічними: (Слайд 9)

8. Класифікація хімічних реакцій за напрямком протікання. (Слайд 10)
 9. Які з даних реакцій є оборотними: (Слайд 11)
9. Які з даних реакцій є оборотними: (Слайд 11)

10. Чи з однаковою швидкістю відбуваються хімічні реакції?
(Слайд 12)
 11. Аналізуючи причини різної швидкості хімічних реакцій, учень дійшов таких висновків:
11. Аналізуючи причини різної швидкості хімічних реакцій, учень дійшов таких висновків:
(Слайд 13)
12. Якщо сірку, яка горить в повітрі, внести в посудину з киснем, то швидкість реакції горіння збільшиться внаслідок: (Слайд 14) 
13. На шматок заліза діємо розчином хлоридної кислоти. Запропонуйте заходи, якими можна прискорити протікання реакції. (Слайд 15)
14. Порівняйте дію каталізатора і інгібітора на швидкість реакції. (Слайд 16)
15. Класифікуйте запропоновані вам хімічні рівняння за всіма відомими вам класифікаційними ознаками. (Слайд 17)
4NO2 + O2 + 2H2O = 4HNO3 + Q
С2Н4 + Н2 ↔ С2Н6 +Q
Al + Fe2O3 = Al2O3 + 2Fe + Q
16. Напишіть рівняння і назвіть тип реакцій, за допомогою яких можна здійснити перетворення: (Слайд 18)
Al → Al2O3 → AlCl3 → Al(OH)3 → Al2(SO4)3
Для окисно-відновних реакцій складіть електронний баланс, а для реакцій йонного обміну запишіть рівняння в йонному вигляді.

17. (Слайд 19)
 Домашнє завдання. (Слайд 20)
Домашнє завдання. (Слайд 20)


про публікацію авторської розробки
Додати розробку
