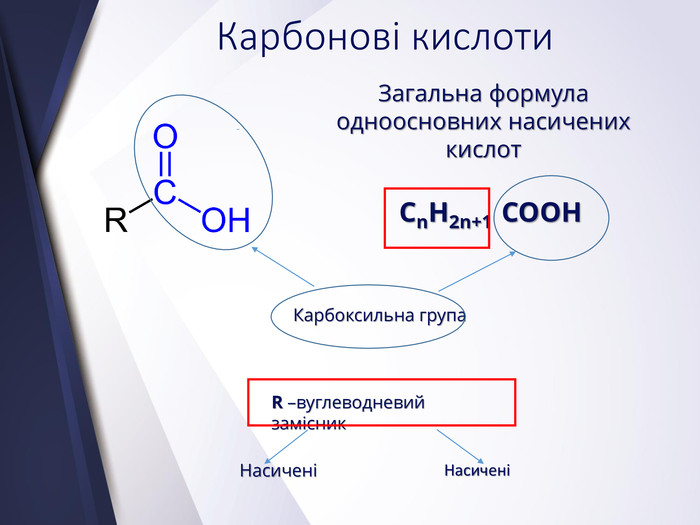
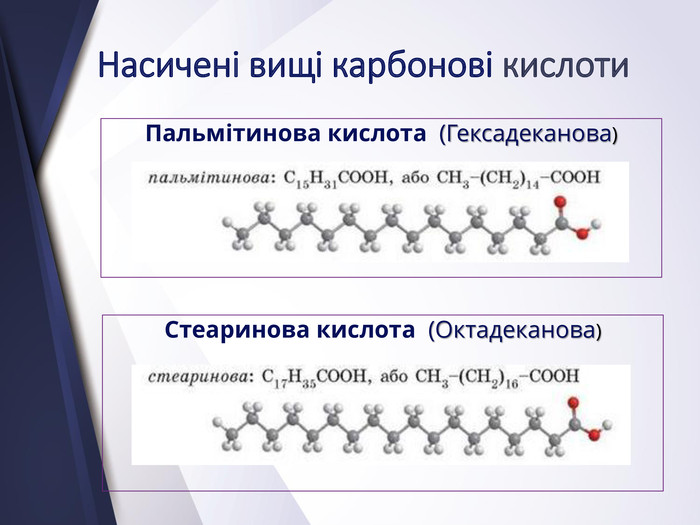
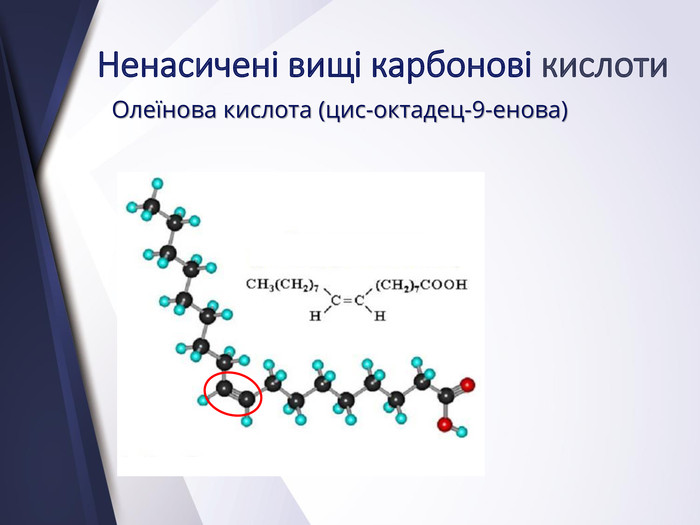
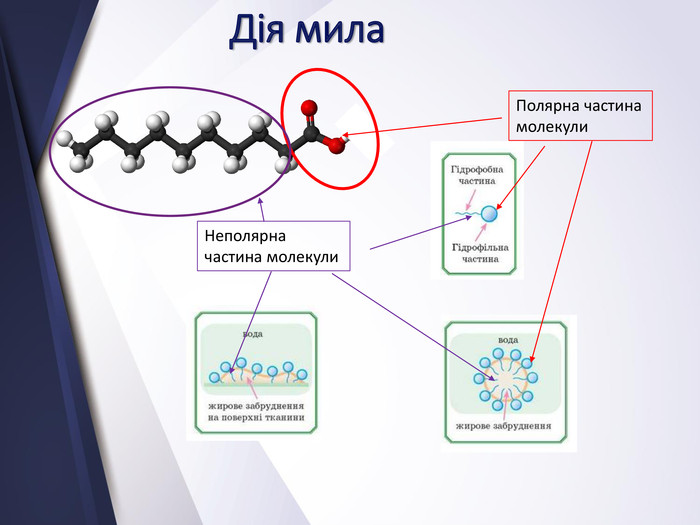
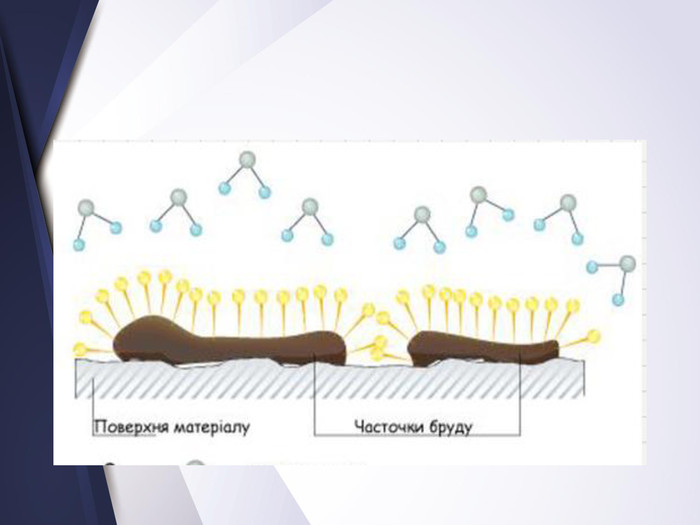
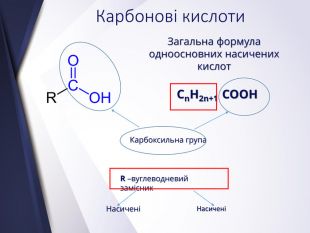
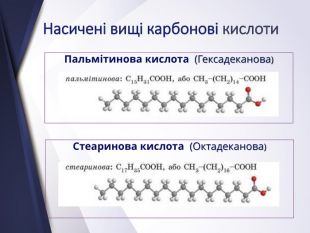
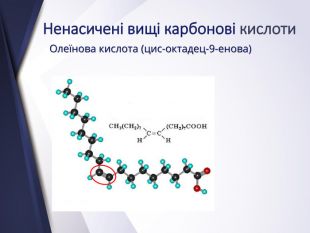
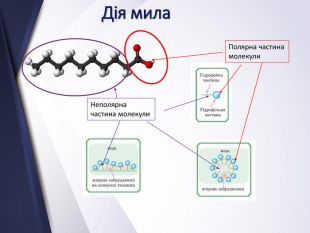
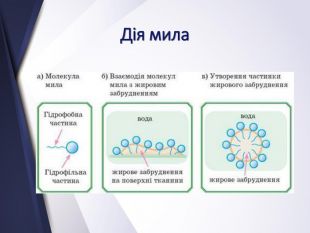
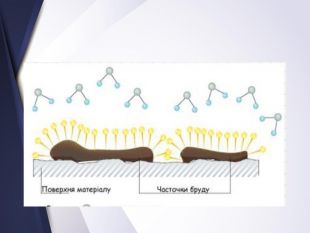
Вищі карбонові вислоти. Мило. Жири
Про матеріал
Матеріал можна викоритати у 9, 10 класах під час вивчення відповідних тем з курсу "Органічна хімія" Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку