Вивчення діаграми стану залізо-вуглецевих сплаві
Про матеріал
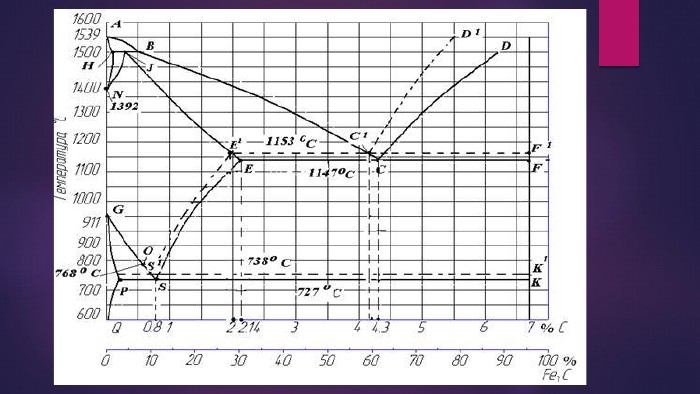
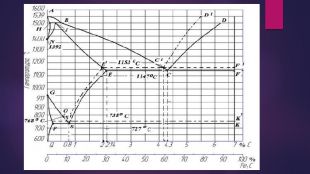
Діаграма стану залізо — цементит та перетворення структурних складових залізовуглецевих сплавів. Діаграму (рис. ) побудовано для системи залізо — цементит (Fe — Ре3С). По осі абсцис відкладено вміст вуглецю у сплаві (у відсотках). Крайня ліва точка відповідає чистому залізу (0 % С), а крайня права точка — чистому цементиту (6,67 % С). Сплави з вмістом вуглецю, більшим за 6,67 %, на діаграмі не позначаються, бо вони не мають практичного значення.
Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку