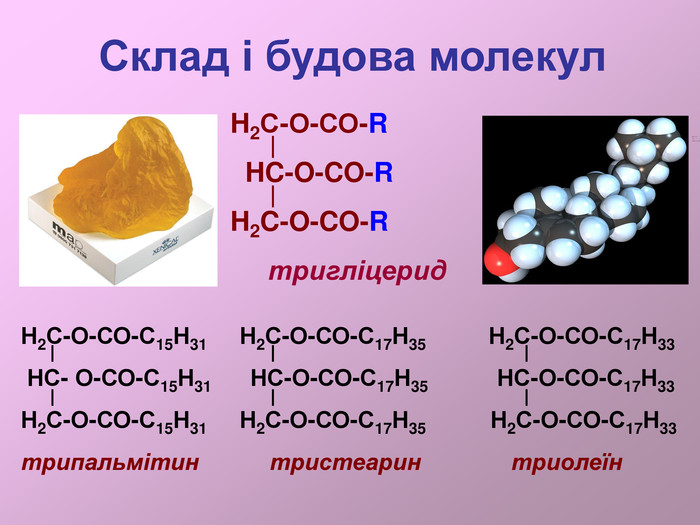
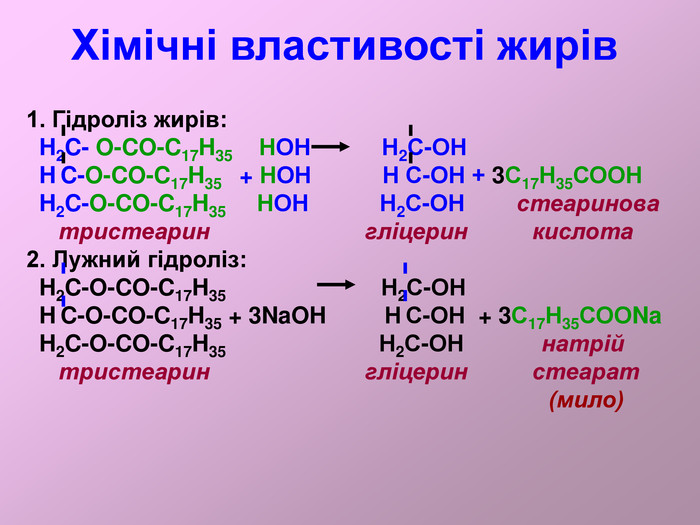
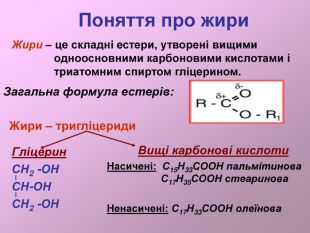
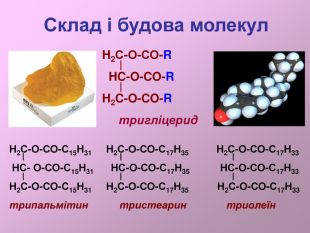
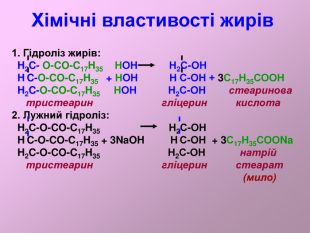
:Жири, склад жирів, фізичні властивості. Природні і штучні жири. Біологічна роль жирів
Про матеріал
Презентація уроку для дистанційного навчання учнів 9 класу надасть можливість учням самостійно опрацювати і засвоїти матеріал із теми Перегляд файлу
Зміст слайдів
ppt
До підручника
Хімія 9 клас (Березан О.В.)
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку