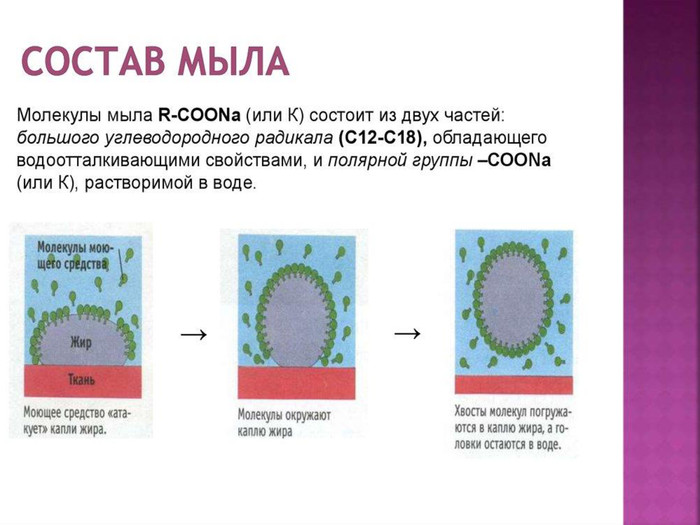
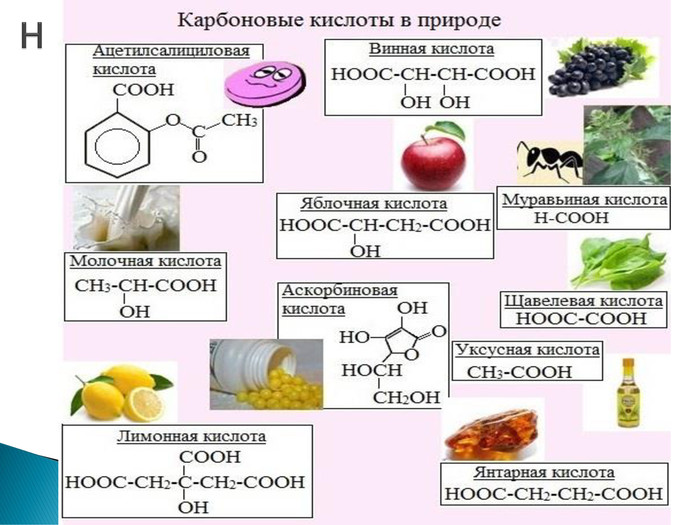
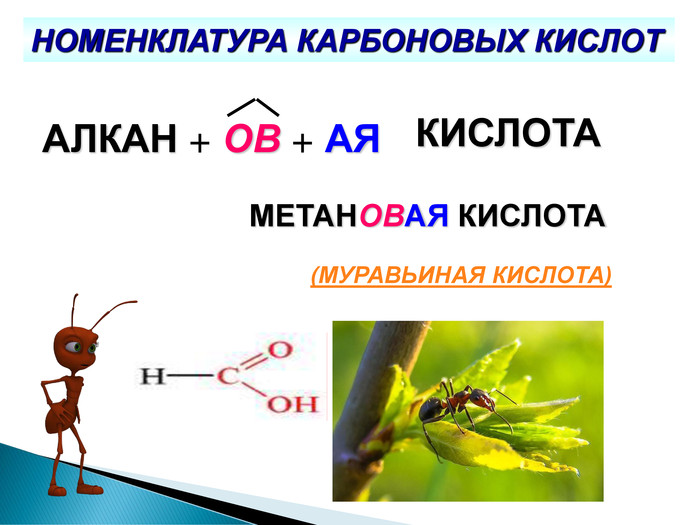
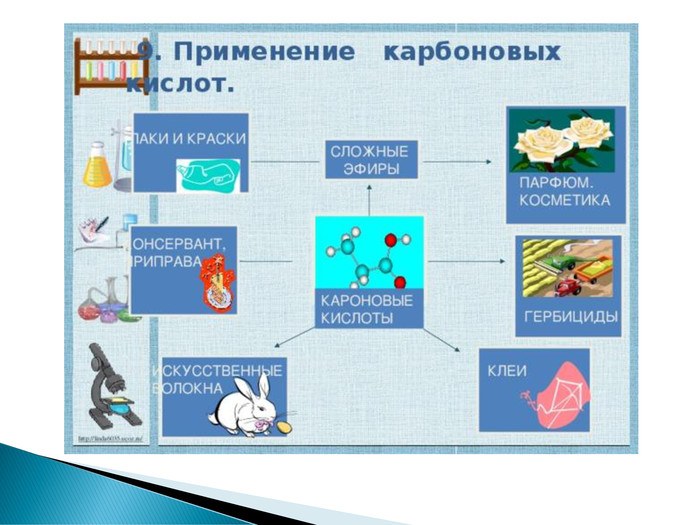
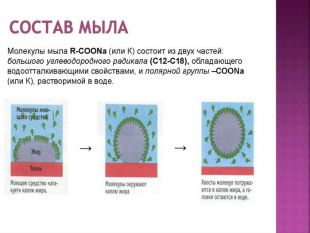
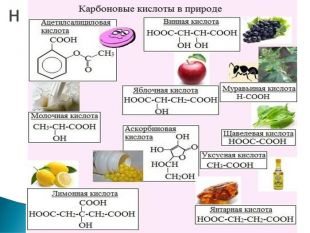
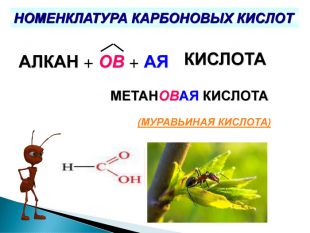
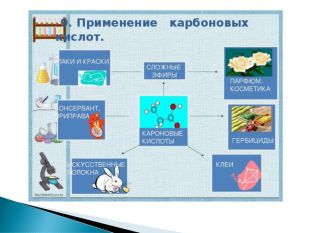
Презентація до уроку хімії у 9 класі на тему "Вищі карбонові кислоти : властивості, застосування і поширення"
Про матеріал
Презентація до уроку хімії у 9 класі на тему "Вищі карбонові кислоти : властивості, застосування і поширення" допоможе краще зрозуміти тему і засвоїти її. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку