8кл . Фізичні властиивості основ .
8 клас
Тема уроку : Фізичні властивості основ.
Опрацювання матеріалу уроку надає можливість учню :
1. усвідомити поняття «основи»
2. ознайомитись з класифікацією основ
2. складати формули основ
3 наводити приклади розчинних і нерозчинних основ,
4. опанувати номенклатуру
5. познайомитись з фізичними властивостями основ
6. відпрацювати навички користування таблицею розчинності
Ключові поняття і терміни: основи, луги , гідроксид.
Хід уроку :
|
1. Подивись навчальне відео «Основи : фізичні властивості» за адресою або QR кодом: |
|
|
|
Теоретичний блок:
Переглянувши відео , з’ясували :
Осно́ви - це складні речовини, утворені металічним елементом та гідроксидними групами (OH).
Основи - електроліти, які у водному розчині дисоціюють з утворенням катіонів металу (або неметалічних катіонів, як NH4+) і аніонів лише одного типу —гідроксиду ОН–.
Наприклад:
- NaOH = Na+ + OH-
- NH4OH = NH4+ + OH-
- Ba(OH)2 = Ba2+ + 2OH-
Тобто основи можна розглядати як гідроксиди основних оксидів - як продукти приєднання води до основних оксидів:
- Na2O + H2O = 2NaOH
- CaO + H2O = Ca(OH)2
- BaO + H2O = Ba(OH)2
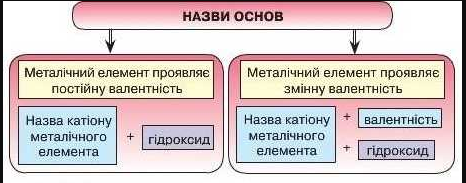
Номенклатура основ :
Основи називають звичайно гідроксидами відповідних металів.
Якщо метал має сталу валентність і утворює тільки один гідроксид, то його називають просто гідроксидом цього металу. Так, NaOH — гідроксид натрію, Ba(OH)2—гідроксид барію.
Якщо ж метал має змінну валентність і утворює кілька гідроксидів, то щоб розрізнити їх, у назвах перед словом гідроксид вказують валентність метала . Наприклад: Cu(OH)2— Купрум (ІІ) гідроксид,
Fe(OH)2—Ферум (ІІ ) гідроксид
Fe(OH)3— Ферум (ІІІ) гідроксид
Перевір себе :
інтерактивна вправа https://learningapps.org/display?v=pqym6frra17
Фізичні властивості основ :
|
2. Перегляньте відео «Зразки основ» за посиланням або за QR кодом : https://www.youtube.com/watch?v=8g3p8YJER0k
|
|
З’ясували :
1. Основи є твердими речовинами.
Деякі з них, зокрема NaOH і KOH, у термічному відношенні досить стійкі: їх можна нагрівати до температури плавлення і вони не розкладаються. Проте більшість основ нестійкі і при нагріванні легко розкладаються з утворенням оксидів і виділенням води.
Наприклад: Ca(OH)2= CaO + H2O або 2Fe(OH)3= Fe2O3+ 3H2O
2. За розчинністю у воді основи поділяють на розчинні та нерозчинні.
Добре розчинними є тільки основи лужних і лужноземельних металів. Розчинні у воді основи називаються лугами.
Серед лугів практично найбільш вживаними є NaOH, KOH, Ca(OH)2 і Ba(OH)2. Водні розчини їдких лугів мають їдкий мильний смак. Вони легко руйнують рослинні і тваринні тканини. Через це їх називають ще їдкими лугами.
Розчини їдких лугів мають здатність змінювати забарвлення індикаторів. Так, у лужному середовищі фіолетовий колір лакмусу змінюється на синій, помаранчевий колір метилоранжу— на ясно-жовтий, а безбарвний розчин фенолфталеїну стає фіолетовим.
Складаємо опорний конспект в зошиті :
Основи – це _________________________________________________________
Основи мають ___________________ будову і складаються з _________________
Загальна формула основ : ________________________________________________
Класифікація основ :_____________________________________________________
Розчинні у воді основи називаються _______________________________________
Фізичні властивості основ : ______________________________________________
Перевір себе ( тренувальні вправи) :
Завдання 1. Визначте валентність металічних елементів за формулами основ :
CsOH, La(OH)3 , Th(OH)3 , Cd(OH)2 , CuOH , Cu(OH)2
Підказка : 
Завдання 2. Виконай завдання :
|
Назвіть наведені формули основ за українською хімічною номенклатурою : |
Складіть хімічні формули основ за їх назвами : |
|
Zn(OH)2 _____________________________________ NaOH _________________________ Cu(OH)2_____________________________________ Al(OH)3_____________________________________ KOH _________________________ Fe(OH)2_______________________ |
Літій гідроксид ____________________ Магній гідроксид __________________ Хром (ІІ) гідроксид__________________ Ферум (ІІІ) гідроксид _______________ Купрум (І) гідроксид ________________
|
Завдання 3. Із запропонованого переліку виберіть формули основ. Користуючись таблицею розчинності основ, кислот і солей розподіліть обрані формули на два стовпчика , а саме : розчинні і нерозчинні основи.
|
Cu(OH)2, Na2O, P2O5, HNO3, Fe(OH)3 , Al2(SO4)3, KOH, Ca(OH)2 Fe(OH)2, CaO, SO3, H3PO4, MgCl2, HCl, H2S , Fe(OH)3, K2O, H2О, Zn3(PO4)2, Ba(OH)2, HNO3 |
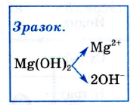
Завдання 4.Запиши йонний склад та співвідношення йонів основ за зразком :
|
|
Ba(OH)2 , Fe(OH)3, , KOH , Ca(OH)2 . Fe(OH)2, NaOH |
Заробляємо оцінку!
Після опрацювання матеріалу пройди Тест онлайн.
Домашнє завдання:
- прочитати § 24 ,
- вивчити фізичні властивості основ


про публікацію авторської розробки
Додати розробку