Хімічні властивості етаналю, його одержання
Про матеріал
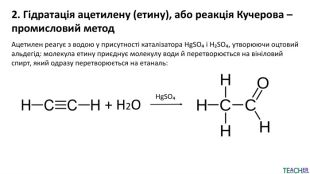
У презентації розглянуто хімічні властивості етаналю (ацетальдегіду) як представника альдегідів. Подано характерні реакції етаналю: окиснення, відновлення, взаємодію з реактивами на альдегідну групу, а також реакції приєднання. Окрему увагу приділено способам одержання етаналю — з етанолу (часткове окиснення, гідратація етину). Матеріал подано у зрозумілій формі з рівняннями реакцій і поясненнями, що сприяє кращому засвоєнню теми учнями. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку



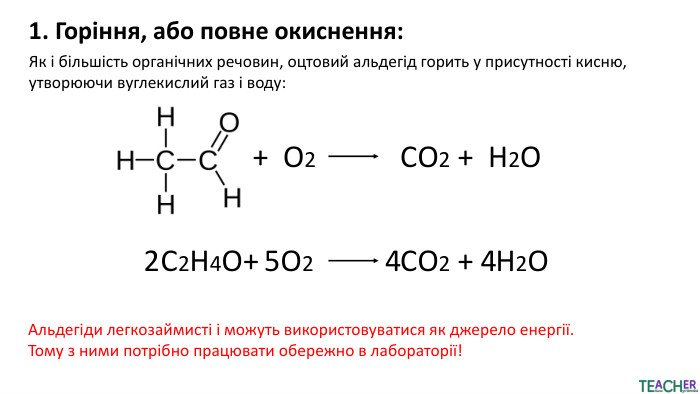
![2. Часткове окиснення:а) реакція “срібного дзеркала”: У чисту пробірку наливають амоніачний розчин аргентум (І) оксиду (у воді цей оксид не розчиняється, але з амоніаком утворює розчинну сполуку [𝐴𝑔(𝑁𝐻3)2]ОН – реактив Толленса. До нього приливають розчин альдегіду і нагрівають. Проба використовується для розрізнення альдегідів від кетонів. При взаємодії з альдегідами реактив відновлюється до металевого срібла, яке осідає на стінках посудини у вигляді дзеркального нальоту. Альдегід окиснюється до оцтової кислоти + Ag2 ОNH3 ⋅ H2 Ot+ 2 Ag 2. Часткове окиснення:а) реакція “срібного дзеркала”: У чисту пробірку наливають амоніачний розчин аргентум (І) оксиду (у воді цей оксид не розчиняється, але з амоніаком утворює розчинну сполуку [𝐴𝑔(𝑁𝐻3)2]ОН – реактив Толленса. До нього приливають розчин альдегіду і нагрівають. Проба використовується для розрізнення альдегідів від кетонів. При взаємодії з альдегідами реактив відновлюється до металевого срібла, яке осідає на стінках посудини у вигляді дзеркального нальоту. Альдегід окиснюється до оцтової кислоти + Ag2 ОNH3 ⋅ H2 Ot+ 2 Ag](/uploads/files/21504/497190/556901_images/4.jpg)
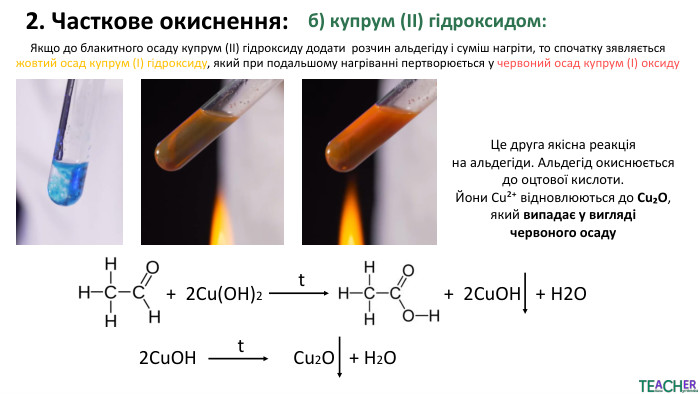
![2. Часткове окиснення: У загальному вигляді:+ [O]Як окисники також застосовуються:калій перманганат KMn. O4, калій дихромат K2 Cr2 O7, селен(IV) оксид Se. O2 2. Часткове окиснення: У загальному вигляді:+ [O]Як окисники також застосовуються:калій перманганат KMn. O4, калій дихромат K2 Cr2 O7, селен(IV) оксид Se. O2](/uploads/files/21504/497190/556901_images/6.jpg)
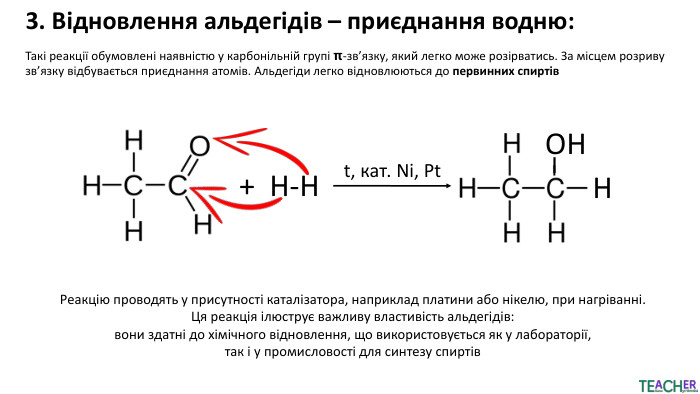

![1. Часткове окиснення етанолу,у результаті чого група -ОН втрачає гідроген, а оксиген з'єднується подвійним зв'язком з атомом карбону. При цьому спирт перетворюється на альдегід: CH3-CH2-OH + [O] + H2OОкиснення має бути частковим, щоб не утворилася оцтова кислота 1. Часткове окиснення етанолу,у результаті чого група -ОН втрачає гідроген, а оксиген з'єднується подвійним зв'язком з атомом карбону. При цьому спирт перетворюється на альдегід: CH3-CH2-OH + [O] + H2OОкиснення має бути частковим, щоб не утворилася оцтова кислота](/uploads/files/21504/497190/556901_images/9.jpg)