Хімічні властивості кисню. Поняття оксиду, реакцій окиснення (горіння, повільне окиснення, дихання). Реакція сполучення.
Урок сформован згідно з календарним плануванням з хімії для 7 класу за новою програмою 2017-2018 р. Використані новітні освітні технології : кейс-технологія, інтерактивна, групова. Створені умови для сприйняття, осмислення і первинного закріплення навчальної інформації.
Тема: Хімічні властивості кисню. Поняття оксиду, реакцій окиснення (горіння, повільне окиснення, дихання). Реакція сполучення.
Мета дидактична: сприяти формуванню знань учнів про кисень, його хімічні властивості; забезпечити умови для засвоєння учнями понять: «реакція сполучення», «реакція горіння», «повільне окислення», «оксиди»; сформувати поняття учнів про оксиди та реакції окиснення речовин; ознайомити учнів із різновидом реакцій окиснення та з умовами виникнення і припинення горіння; сформувати вміння записувати рівняння хімічних реакцій горіння простих і складних речовин в кисні, давати назви отриманим речовинам; сприяти осмисленню учнями ролі кисню на Землі і в житті людини.
Розвиваюча: сприяти формуванню вмінь: виділяти загальні і суттєві ознаки і властивості, бачити проблему і знаходити шляхи її вирішення, застосовувати отримані знання на практиці і оцінювати результатів виконаних дій; продовжувати розвиток самостійності, вміння працювати в парах і групах.
Виховна: сприяти вихованню сумлінного ставлення до праці, позитивного ставлення до знань, ініціативності, наполегливості, здатності долати труднощі для досягнення.
ХІД УРОКУ
I. Організаційний етап
Вчитель вітає учнів, визначає готовність до уроку.
II. Актуалізація знань учнів
Вчитель пропонує виконати завдання для того, щоб згадали ключові поняття минулого уроку. Ці характеристики кисню допоможуть учням більш детально розібратися в темі сьогоднішнього уроку. Вчитель пояснює завдання: на дошці написані формула атома оксигену та формула молекула кисню: на кожній парті знаходяться папірці з текстом (властивості оксигену та кисню) учні повинні вибрати ті визначення, які характерні для кожного (5 хвилин). Потім запрошує двох учнів, які записують на дошці вибрані відповіді. Учні обмінюються зошитами та перевіряють відповідність відповідей, оцінюють повноту знань, виставляють оцінки, обговорюють результати.
Самостійна робота: не має запаху, кольору і смаку; в промисловості отримують з повітря; це - складна речовина; його назва походить від латинського Oxygenium; збирають витісненням повітря; важчий за повітря; складається з одного атома; в зрідженому стані має блакитний колір; входить в склад складних речовин; хімічні властивості; збирають в перевернутий догори дном посудину; в лабораторії отримують з «пероксиду водню»; реакція сполучення; має масу 16; оксиди; при температурі -183 °С перетворюється у рідину; знаходиться в 6 групі, головній підгрупи; має масу 32; входить до складу мінералів, гірських порід, піску, води; утворюється в природі в процесі фотосинтезу.
Актуалізуються опорні знання учнів. Учні готуються до сприйняття нового матеріалу.
Вчитель запитує в учнів усі висловлювання використали чи ні?
На столах залишилось три аркуші паперу з висловами: хімічні властивості, реакція сполучення та оксиди.
Вчитель: Як на вашу думку, чому залишилися ці аркуші. Учні висловлюють думку, що це тема нашого уроку. Вчитель записує тему уроку на дошці (можна написати тему і мету раніше, а потім розкрити дошку), учні записують в зошит. Вчитель розповідає мету уроку.
III. Вивчення нового матеріалу.
Хімічні властивості кисню.
Вчитель пропонує учням роздивитись фото, яке знаходиться у кожного на парті.

Та розповісти, що вони бачать на фото. Учні розповідають, що це багаття, процес горіння дров. Це хімічне явище, яке супроводжується виділенням тепла та світла, яке описується хімічною реакцією.
Вчитель пропонує відкрити підручник на стр.126 (підручник Хімія 7 клас Савчин
2015р.)
Прочитати 3 абзац (горіння….)
Вчитель: Що ж таке реакція горіння? Спалахування скіпки, горіння дров відбувається при взаємодії речовин з киснем.
Вчитель далі звертає увагу на екран та проглянути фільм. https://www.youtube.com/watch?v=iXcu1l2M-Vk Таблица Менделеева. Смешные элементы, кислород. (Короткометражный мультфильм).
Вчитель опитує учнів, про що вони дізнались з фільму. Учні розповідають, що з деякими речовинами кисень не реагує, з іншими дуже бурхливо, з деякими повільно.
Вчитель для підтвердження цього пропонує учням роздивитись малюнки 65 -66 на стр. 126-127 у підручнику и проглянути або фрагмент досліду, або проводить дослід у витяжній шафі.
Після цього пропонує записати рівняння реакції використовуючи алгоритм написання реакції:
А+В =АВ.
Р + О2 =
Mg + O2 =
S + O2 =
Вчитель після кожного досліду звертає увагу учнів на умови , швидкість проведення реакцій та на зміни які відбуваються під час проведення кожного досліду та пропонує одному учню вийти до дошки та закінчити рівняння (інші в цей час перевіряють свої результати).
Вчитель звертає увагу учнів на те що, процес реакція горіння простих речовин відноситься до реакцій сполучення и пропонує учням записати визначення реакції сполучення. Пропонує учням звернутись до підручника (стр. 131) та виписати визначення (або дати визначення на екрані, або на дошці). Для закріплення поняття просить учнів зачитати в слух (повторення допомагає закріпити поняття).
Реакції сполучення - до цього типу відносять реакції, при яких з молекул двох або кількох простих чи складних речовин утворюються молекули одної складної речовини.
Вчитель звертає увагу на хімічні формули утворених речовин та питає «Що, ви, можете сказати про їх склад?»
Учні відповідають, що в складі утворених у результаті реакцій речовин знаходяться два елементи, один з яких оксиген.
Учні вірно визначили склад речовин.
Вчитель підтверджує, що учні вірно визначили склад утвореного речовини, вони дійсно складаються з двох елементів, один з яких оксиген. Такі речовини називають оксидами. Пропанує записати визначення оксидів (стр. 131 підручник).
Оксиди — це складні речовини, утворені двома елементами, одним з яких є Оксиген з валентністю 2.
Учні записуються в зошит визначення поняття «оксиди». Відбувається усвідомлення учнями змісту поняття «оксиди».
Для того, щоб учні ознайомилися з правилом складання назви оксидів, вчитель організовує самостійну діяльність дітей з придбанням необхідних знань використовуючи інтерактивну дошку. На ній приведені формули оксидів та Їх назва.
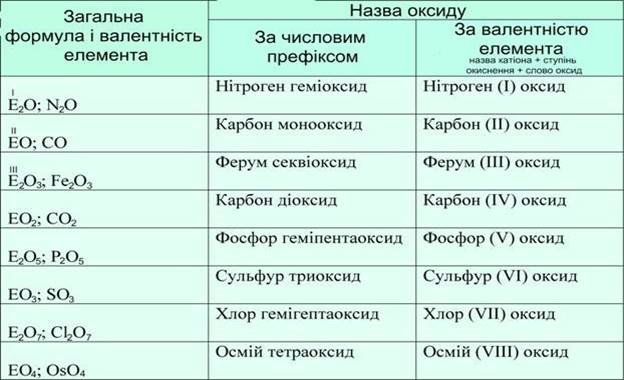
Вчитель пропонує визначити чим схожі назви речовин.
Учні визначають, що в кожній назві є слово «оксид», а перед цим назва кожного елементу, який входить в склад формули.
Вчитель підтверджує вірність відповіді, але звертає увагу, що у деяких назвах є в дужках числа.
Вчитель ставить проблемне питання : «Що це відображають ці числа?»
Як що питання викликає ускладнення, вчитель пропонує повернутись до теми валентність. Учні згадують визначення валентності, як її розраховувати й приходять до висновку, що в дужках вказується валентність елемента (йде повторення раніше вивченого поняття). Вчитель пояснює, коли назвах оксидів вказується валентність: тільки для тих речовин, в яких знаходиться елементи з змінною ступеню окиснення, тобто для елементів 4-8 груп.
Вчитель пропонує учням зробити висновки :
1. Кисень – хімічно активна речовина, яка реагує з простими речовинами.
2. Кисень вступає в реакцію з простими речовинами за різними умовами
(нагрівання).
3. Ознакамиреакцій горіння є виділення тепла та світла.
4. Продуктами горіння є оксиди.
IV. Етап закріплення вивченого матеріалу
1. Групова робота із закріплення отриманих знань.
Вчитель пропонує учням скласти рівняння реакцій за схемами та дати їм назви:
а) Na + O2 = с) C + O2 =
в) Fe + O2 = d) S + O2 =
2. Складіть рівняння хімічних реакцій отримання наступних оксидів і назвіть їх:
MgO, Al2O3, P 2O 5, K2O.
V. Підбиття підсумків уроку, оцінювання учнів.
VI. Домашне завдання
Вчитель записує завдання на дошці та роз'яснює, як слід раціонально організувати свою навчальну роботу при виконанні домашньої задачі.
Задання: §18, відповісти на питання після розділу № 1-3 для середнього рівня; № 56 для достатнього рівня, № 5,6,9 для високого рівня.
Літературні джерела
1. П. Будруджак Задачи по химии - http://www.alleng.ru/d/chem/chem97.htm
2. Дехтяренко С.Г. Моніторинг якості освіти: рівнева загальноосвітня підготовка учнів з хімії. 7 клас.: посібник для вчителів хімії – 3-тє видання, виправлене і доповнене. – Запоріжжя: ТОВ«ЛІПС» ЛТД, 2015. –120 с.
3. Динамічна Періодична Система - http://www.ptable.com/
4. Зламанюк Л. Мотивація до навчання як умова розвитку творчого мислення учнів // Біологія і хімія в сучасній школі. - No 2 – 2013 – С.19-21
5. С.Г. Литвинова Хмарні технологіі як засіб розбудови інноваційної школи http://virtkafedra.ucoz.ua/el_gurnal/pages/vyp14/Litvinova.pdf
6. Савчин Підручник Хімія 7 клас 2015
7. Реакції_сполучення https://uk.wikipedia.org/wiki/
8. Оксиди,_їх_склад,_назви. himiihttp://edufuture.biz/index.php?title


про публікацію авторської розробки
Додати розробку
