Хімічні властивості кисню: взаємодія з вугіллям, сіркою, фосфором. Реакція сполучення.
Урок з предмету «Хімія» на тему «Хімічні властивості кисню: взаємодія з вугіллям, сіркою, фосфором. Реакція сполучення». Розробка уроку у 7 класі з використанням інтерактивних методів навчання, хімічного експерименту, методу проектів.
|
Тема |
Хімічні властивості кисню: взаємодія з вугіллям, сіркою, фосфором. Реакція сполучення. |
|
Очікувані результати |
навчальна:
розвивальна:
виховна:
|
|
Тип заняття: |
комбінований |
|
Форми роботи: |
Індивідуальне опитування, інтерактивні вправи «Спіймай помилку» та «Мікрофон», завдання-малюнок , гра «Влучний стрілець», демонстраційний хімічний експеримент |
|
Обладнання: |
1. Мультимедійна система 2. Відеофрагменти
|
|
Основні поняття та терміни |
Реакція сполучення, оксиди, горіння, окиснення |
|
Міжпредметні зв'язки |
Математика, основи здоров’я |
|
Девіз уроку: |
«Вважай нещасним той день або той час, в який ти не засвоїв нічого нового і нічого не додав до своєї освіти». Я.А. Коменський |
Структура уроку
І. Організаційний момент
ІІ. Перевірка домашнього завдання
ІІІ. Актуалізація опорних знань
IV. Мотивація навчальної діяльності
V. Вивчення нового матеріалу
- Хімічні властивості кисню
- Реакція сполучення
VІ. Узагальнення та систематизація нового матеріалу
VIІ. Домашнє завдання
VІIІ. Підсумок уроку
Хід уроку
І. Організаційний момент
Привітання, перевірка готовності до уроку
ІІ. Перевірка домашнього завдання
- Індивідуальне опитування
А Розв’язування задачі
Знайти масову частку Оксигену у алюміній оксиді.
Б Скласти хімічні рівняння добування кисню в лабораторії
В Перевірка домашніх вправ, творчого завдання
- Інтерактивна вправа «Спіймай помилку»
- Молекула складної речовини кисень утворена двома атомами
Оксигену.
- Кисень – газ без кольору, запаху, смаку, легший за повітря.
- Кисень вперше добув А. Лавуазьє.
- До складу води входить 89% кисню.
- Відносна атомна маса кисню – 8.
- Розчинений у воді Оксиген потрібний для життєдіяльності водних рослин і тварин.
- Кисень добре розчиняється у воді.
- Лабораторні способи добування кисню відносяться до реакцій заміщення.
- Інгібитори – речовини, які прискорюють хімічну реакцію.
- Кисень збирають способом витиснення повітря.
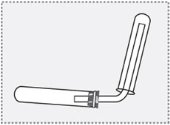
- Завдання-малюнок
Яких помилок припустився учень?
- Учень 7 класу приготував обладнання для одержання кисню. Він налив у пробірку розчин калій перманганату. Пробірку закрив пробкою з прямою газовідвідною трубкою, на яку надів догори дном порожню пробірку, і почав чекати. Закінчився урок, але тліюча скіпка, яку він підносив до пробірки-приймача, так і не спахнула.
ІІІ. Актуалізація опорних знань
Інтерактивна вправа «Мікрофон»
Бесіда з учнями
- Що таке хімічна реакція?
- За яких умов відбуваються хімічні реакції?
- За якими ознаками можна визначити, що хімічна реакція відбувається?
IV. Мотивація навчальної діяльності
Проблема: Як ви вважаєте, що ми будемо вивчати на уроці?
Демонстрація відео фрагмента: «Спалювання заліза»
Повідомлення теми та завдань уроку
V. Вивчення нового матеріалу
- Хімічні властивості кисню
І. Горіння простих речовин
А горіння вуглецю
С + О2 = СО2 (карбон(IV) оксид)
Демонстрація: Спалювання вуглецю
Б горіння сірки
S + О2 = SО2 (сульфур(IV) оксид)
Демонстрація: Спалювання сірки
В горіння фосфору
4Р + 5О2 = 2Р2О5 (фосфор(V) оксид)
Демонстрація: Спалювання фосфору
Г горіння магнію
2Мg + O2 = 2МgO (магній оксид)
Демонстрація: Спалювання магнію
- Первинне закріплення знань
Запитання:
- Яка речовина підтримує горіння?
- Так які ж речовини утворюються при взаємодії кисню з простими речовинами?
- Які речовини на вашу думку можуть утворюватись при горіння складних речовин?
ІІ. Горіння складних речовин
А горіння метану
СН4 + 2О2 = СО2 + 2Н2О
Б горіння спирту
С2Н5ОН + 3О2 = 2СО2 + 3Н2О
- За 20 останніх років в незалежній Україні відбулося більше 900 підземних пожеж та майже 50 вибухів. Україна втратила приблизно 4 тисячі гірників. Рівень травматизму у вугільній галузі України вважається одним з найвищих у світі. На 1 млн. тонн вугілля в нашій країні доводиться 2,5 шахтарської смерті. Це про них горить свіча.
- Фізкультхвилинка (1 хв.)
Встаньте, діти, посміхніться,
Землі нашій поклоніться,
За щасливий день вчорашній,
Ви до сонця потягніться,
Веретеном обкрутіться,
Раз присядьте, два присядьте,
І за парти тихо сядьте.
- Реакція сполучення
Реакціями сполучення називаються реакції, під час яких із кількох речовин утворюється одна.
Оксидом називається сполука, утворена двома елементами, одним із яких є Оксиген.
VI. Узагальнення та систематизація знань
- Напишіть рівняння реакцій:
AL + О2 →
Mg + О2 →
C2H4 + О2 →
H2S + О2 →
PH3 + О2 →
- Гра: «Влучний стрілець»
Вибрати з переліку формул оксиди: CH4, CO2, H2CO3, Na2O, SO2, NH3, AL2O3, HCL, BaO, H3PO4
VIІ. Домашнє завдання
- Опрацювати § 21
- виконати вправи: 18, 19
Повторити правила ТБ
VIІI. Підсумок уроку
- З якою хімічною властивістю кисню ви ознайомились на уроці?
- Як ви вважаєте з практичної точки зору навіщо вивчаються властивості речовин?


про публікацію авторської розробки
Додати розробку
