Кольорові реакції білків
План-конспект лабораторно-практичного заняття
Тема: Кольорові реакції білків
Мета заняття:
- експериментально підтвердити наявність пептидних зв’язків та специфічних амінокислотних радикалів у структурі білків;
- вдосконалити навички роботи з хімічним посудом та агресивними реактивами (луги, концентровані кислоти);
- виховувати культуру безпечної праці та аналітичне мислення.
Обладнання та реактиви: штатив з пробірками, спиртівка, пробіркотримач, розчин білка, розчин натрій гідроксиду, нітратної кислоти, плюмбум ацетату, купрум(ІІ) сульфату, нінгідрин.
Хід проведення заняття
І. Організаційний момент.
ІІ. Актуалізація знань (бліц-опитування)
Перед початком роботи варто обговорити:
- Рівні організації білкової молекули та хімічні зв'язки
- Який зв'язок називається пептидним і між якими групами амінокислот він виникає?
(Це амідний зв’язок ( -CO-NH-), що виникає в результаті взаємодії α-карбоксильної групи однієї амінокислоти та α-аміногрупи іншої).
Акцент: варто зазначити, що саме цей зв’язок ми будемо виявляти у біуретовій реакції. Важливо підкреслити, що для позитивної реакції необхідно мати мінімум два такі зв'язки (тобто сполука має бути мінімум трипептидом).
2. Різноманітність амінокислотних радикалів
- Чи всі білки складаються з однакового набору амінокислот? Які специфічні угруповання можуть міститися в радикалах (бічних ланцюгах)?
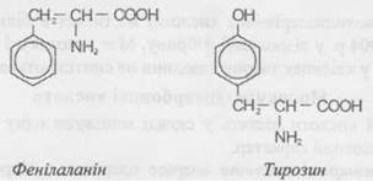
(Ароматичні радикали: наявність бензольного кільця (тирозин, фенілаланін, триптофан).
Акцент: це теоретична основа ксантопротеїнової реакції.
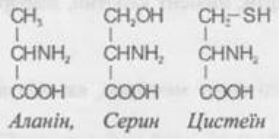
(Сірковмісні радикали: наявність атомів Сульфуру (цистеїн, метіонін).
Акцент: це основа реакції Фоля.
Проблемне питання: Якщо білок складається переважно з аліфатичних амінокислот (гліцин чи аланін), чи дасть він позитивну ксантопротеїнову реакцію? (Відповідь: ні).
3. Хімічні властивості та денатурація
- Що відбувається з білком під дією сильних кислот, лугів або високої температури?
(Відбувається денатурація – руйнування вторинної, третинної та четвертинної структур при збереженні первинної).
- Акцент: оскільки багато кольорових реакцій вимагають кип’ятіння або використання концентрованих кислот, учні повинні розуміти, що вони спостерігатимуть не лише зміну кольору, а й, можливо, випадання осаду (коагуляцію білка).
4. Мотиваційний блок: де це використовується в житті?
- Медицина: як перевірити наявність білка в біологічних рідинах (наприклад, у сечі при підозрі на захворювання нирок)?
- Харчова промисловість: як переконатися, що продукт (наприклад, спортивне харчування чи молоко) дійсно містить білок, а не дешеві замінники?
- Косметологія: чому деякі креми жовтіють при контакті з певними реагентами?
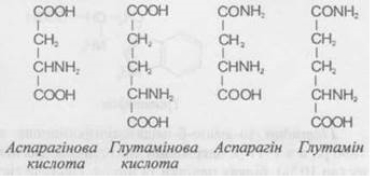
На цьому етапі можна використати короткий інтерактив — показати картки з формулами амінокислот (гліцин, тирозин, цистеїн) і попросити учнів спрогнозувати, яку саме реакцію (із запланованих сьогодні) дасть кожна з них.
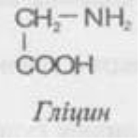
ІІ. Інструктаж з техніки безпеки
Важливо: у роботі використовуються концентрована нітратна кислота (HNO3) та луг (NaOH).
- Працювати виключно в халатах та захисних окулярах.
- При потраплянні кислоти на шкіру – промити великою кількістю води та обробити розчином соди.
- При потраплянні лугу – промити водою та обробити розчином борної кислоти.
ІІІ. Практична частина
Дослід 1. Біуретова реакція (на пептидний зв'язок)
Це універсальна реакція на всі білки. Вона дозволяє виявити наявність у розчині зв'язків -CO-NH-.
- Реактиви: розчин білка (яєчний альбумін), 10% розчин NaOH, 1% розчин CuSO4.
- Хід роботи: до 2 мл розчину білка додайте 2 мл лугу, а потім кілька крапель розчину купрум(ІІ) сульфату.
- Ознака реакції: поява інтенсивного фіолетового або синьо-фіолетового забарвлення.
Дослід 2. Ксантопротеїнова реакція (на ароматичні амінокислоти)
Виявляє амінокислоти, що містять бензольне кільце (фенілаланін, тирозин, триптофан).
- Реактиви: розчин білка, концентрована HNO3, розчин аміаку або лугу.
- Хід роботи: до 1 мл білка обережно додайте 5-6 крапель концентрованої нітратної кислоти. Нагрійте суміш.
- Ознака реакції: утворення жовтого осаду або забарвлення. При додаванні надлишку лугу колір змінюється на оранжевий.
Дослід 3. Реакція Фоля (на сірковмісні амінокислоти)
Виявляє цистеїн та метіонін, які містять слабозв'язану сірку.
- Реактиви: розчин білка, 20% розчин NaOH, 5% розчин Pb(CH3COO)2 (плюмбум ацетату).
- Хід роботи: до розчину білка додайте рівний об'єм лугу та 2-3 краплі плюмбум ацетату. Тривало прокип'ятіть (1 – 2 хвилини).
- Ознака реакції: поява чорного або темно-сірого осаду (PbS).
Дослід 4. Нінгідринова реакція (на α-аміногрупи)
Виявляє вільні аміногрупи. Дуже чутлива реакція.
- Реактиви: розчин білка, 0,1% розчин нінгідрину в спирті.
- Хід роботи: до розчину білка додайте кілька крапель нінгідрину і нагрійте.
- Ознака реакції: поява синьо-фіолетового забарвлення.
IV. Оформлення результатів
Учні заповнюють підсумкову таблицю:
|
Назва реакції |
Що виявляє (зв'язок/група) |
Спостереження (колір) |
Висновок |
|
Біуретова |
Пептидний зв'язок |
Фіолетовий |
Білок є поліпептидом |
|
Ксантопротеїнова |
Ароматичне кільце |
Жовтий Оранжевий |
Наявність тирозину/фенілаланіну |
|
Реакція Фоля |
Сульфгідрильні групи (-SH) |
Чорний осад |
Наявність сірки (цистеїну) |
V. Підсумок заняття
Вікторина: https://wordwall.net/resource/104756719
Перейти за покликанням або сканувати QR-код та пройти коротеньку вікторину за вивченим матеріалом.

Контрольні запитання для дискусії:
- Чому при попаданні нітратної кислоти на шкіру з’являються жовті плями? (Зв'язок з ксантопротеїновою реакцією).
- Чи дасть біуретову реакцію окрема амінокислота, наприклад, гліцин? (Ні, бо немає пептидного зв'язку).
- Яке значення мають ці реакції в аналітичній хімії та медицині? (Виявлення патологій за аналізом сечі, вивчення білкового складу крові і т.п.)


про публікацію авторської розробки
Додати розробку
