Конспект уроку хімії в 9 класі на тему "Ацетилен,будова, властивості, застосування"
Мета: формувати знання про гомологічний ряд алкінів на прикладі ацетилену, ознайомити з природою потрійного зв'язку, фізичними та хімічними властивостями, розвивати вміння і навички складати рівняння реакцій, формувати вміння пояснювати механізм реакцій приєднання, розглянути способи добування і застосування ацетилену; розвивати логічне мислення і формувати життєві компетенції.
Загальноосвітня школа І-ІІІ ст. с. Великий Курінь
Ацетилен,будова,
властивості, застосування
(хімія, 9 клас)
З досвіду роботи
вчителя хімії Семенюк Н.Т.
Мета: формувати знання про гомологічний ряд алкінів на прикладі ацетилену, ознайомити з природою потрійного зв’язку, фізичними та хімічними властивостями, розвивати вміння і навички складати рівняння реакцій, формувати вміння пояснювати механізм реакцій приєднання, розглянути способи добування і застосування ацетилену; розвивати логічне мислення і формувати життєві компетенції.
Тип уроку: отримання нових знань.
Обладнання: слайди презентації, комп’ютер, ППЗ «Органічна хімія», проектор.
Форми роботи: фронтальна, індивідуальна, групова.
Структура уроку
І. Організаційний етап (1хв.)
ІІ. Актуалізація опорних знань (5хв.)
ІІІ. Мотивація навчальної діяльності (2хв.)
ІV. Визначення теми, мети і завдань уроку (2хв.)
V. Вивчення нового матеріалу (20хв.)
VІ. Закріплення вивченого матеріалу( 6хв.)
VІІ. Рефлексія.(підсумок уроку, оцінювання (3хв.)
VІІІ. Домашнє завдання, його коментар (1хв.)
Хід уроку
Девіз уроку:
«Не бійся відповідати: неправильна відповідь – теж відповідь,
адже це свідчить про те, що ти розмірковуєш.»
І. Організація класу
Привітання. Створення позитивного емоційного настрою, вступ до уроку
Побажання вчителя: «Пам’ятайте, що немає нічого неможливого для наполегливих».
Тож хай вас не лякають труднощі. Вірте в себе – ви зможете їх подолати.
ІІ. Актуалізація опорних знань
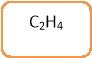 Завдання 1. Гра «Снігова куля» - слайд
Завдання 1. Гра «Снігова куля» - слайд

![]()
![]()
![]()
![]()
![]()
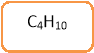
![]()

![]()
![]()

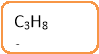
![]()

Бесіда.- слайд
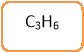
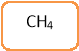
- Що об’єднує ці сполуки?
- Які вуглеводні ми вже вивчили?
- Які з цих речовин є алканами?
- Яка загальна формула алканів?
- Назвіть алкани снігової кулі.
- Які з них належать до ненасичених вуглеводнів?
- Яка загальна формула вуглеводнів ряду етилену?
- Який суфікс присутній у насичених вуглеводнів?
- Який суфікс присутній в етиленових вуглеводнів?
10.Які зв’язки можуть виникати між атомами Карбону в органічних речовинах?
11.Що є доказом наявності атомів Карбону?
12.Що є доказом наявності атомів Гідрогену?
13.На слайді перелік реакцій: гідрування, заміщення, горіння, приєднання, окиснення.
Які з цих реакцій характерні для насичених вуглеводнів?
14.Які хімічні властивості ненасичених вуглеводнів?
Отже, знебарвленням розчинів бромної води та марганцівки можна відрізнити алкени від алканів. Завдання 2. Скласти назву нової речовини - слайд
Із букв, що відповідають правильним відповідям, складіть назву нової речовини, яку будемо вивчати на уроці.
|
1) Метан має тетраедричну будову |
А |
|
2) Молекулярна формула етану – С2Н4 |
Ц |
|
3) Метан та його гомологи розчинні у воді |
О |
|
4) Реакція повного окиснення метану — екзотермічна |
Е |
|
5) Одинарний зв'язок - π-зв’язок |
І |
|
6) Етилен має подвійний зв’язок |
Т |
|
7) Хімічна активність метану висока |
М |
|
8) Під час горіння етилену виділяється вуглекислий газ і вода |
И |
|
9) Метан — стійкий до дії кислот, лугів та окисників |
Л |
|
10) Приєднання водню до етилену – це реакція гідрування |
Е |
|
11) Гомологи метану і етилену не горять |
Д |
|
12) Етилен знебарвлює розчин калій перманганату |
Н |
Назва речовини складена, але про цю речовину ми нічого не знаємо, нам вона не відома. Отже виникла проблема, яку ми маємо розв’язати на уроці.
III. МОТИВАЦІЯ НАВЧАЛЬНОЇ ДІЯЛЬНОСТІ
Учитель. Учений Б. М. Кедров говорив: «Будь-яка речовина — від найпростішої до найскладнішої — має три відмінні, але взаємопов'язані сторони...» Як ви гадаєте, діти, про які сторони говорив учений? (Склад, будова і властивості)
Оголошення теми й мети уроку. – слайди
За ключовими словами: що? які? як? де? визначити питання, які слід розглянути на уроці.
Складаємо план вивчення нового матеріалу.(учні називають питання)
Отже, ми в ході уроку дамо відповіді на такі питання: - слайд
1.Ацетилен – найпростіший представник алкінів.
2. Склад і будова молекули ацетилену.
3. Фізичні властивості.
4. Хімічні властивості.
5. Добування ацетилену.
6. Застосування ацетилену.
IV. ФОРМУВАННЯ НОВИХ ЗНАНЬ, УМІНЬ І НАВИЧОК
1.Склад і будова молекули ацетилену
Складання комплексної характеристики ацетилену
Робота з класом
Учні встановлюють молекулярну формулу ацетилену, розв'язуючи задачу. – слайд
Про яку речовину йдеться мова, якщо відомо, що вона належить до вуглеводнів, масова частка Карбону в ній становить 92,3%, відносна густина за воднем – 13.
Відповідь: молекулярна формула ацетилену — С2Н2.
Встановлення структурної та електронної формули ацетилену відбувається в процесі лабораторного досліду (виготовлення на основі кулестрижневої моделі етану, етилену і ацетилену)
Обговорення результатів роботи
- Як сполучені між собою два атоми Карбону?
- Чи можливе вільне обертання атомів навколо потрійного зв'язку?( атоми Карбону можуть обертатися тоді, коли вони сполучені σ - зв’язком; виникнення – π-зв’язку позбавляє їх можливості вільно обертатися.)
Перегляд «Склад і будова молекули ацетилену» (пояснення з мультимедійним супроводом)
1.Який валентний кут між атомами Карбону в молекулі ацетилену?
2. Яку будову має молекула ацетилену?(лінійну. Дослідження будови молекули ацетилену показує, що всі атоми в ній розміщені на одній прямій)
3.Як виникає потрійний зв'язок?
4.Скільки всього ковалентних зв'язків у молекулі ацетилену?
Отже, ацетилен належить до ненасичених вуглеводнів – алкінів із суфіксом –ин,
-ін, молекули яких мають відкритий карбоновий ланцюг з потрійним зв’язком: одним – σ і двома – π-зв’язками.
Цей потрійний зв'язок міцніший, ніж подвійний. Кут між лініями, що з’єднують центри атомів у молекулі, становить 180 градусів. Відстань між центрами атомів Карбону, що утворюють потрійний зв'язок, становить 0,120 нм (довжина потрійного зв’язку менша, ніж подвійного).
- Дослідження фізичних властивостей ацетилену
Робота в групах - слайд
Задача. Обчислити відносну густину ацетилену за такою речовиною:
1 — воднем, 2 — киснем, 3 — повітрям.
Розв'язання
1.Густина ацетилену за воднем дорівнює:13
DH2= 26/2=13
- Густина ацетилену за киснем дорівнює:0,81
DO2 = 26/32=0,81
3.Густина ацетилену за повітрям дорівнює:0,9
Dпов.=26/29=0,9
Висновок: ацетилен у 14 разів легший за водень, трохи легший за кисень, молярна маса ацетилену близька до маси повітря.
Робота з класом
Встановити залежність між складом, будовою та властивостями ацетилену.- слайд
С2Н2
ꜜ
ковалентний зв'язок
ꜜ
молекулярна ґратка
ꜜ
Fпритяг. слабкі
Ацетилен — газ, малорозчинний у воді, Тплавл і Ткип. — низькі.
Порівняємо фізичні властивості алканів, алкенів і алкінів – слайд
(Температура плавлення і кипіння підвищується зі збільшенням числа атомів Карбону.)
Перш, ніж досліджувати хімічні властивості ацетилену, пригадаємо хімічні властивості етилену. Скласти рівняння реакцій (замість крапок вставити формули)- слайд
Ненасичені вуглеводні, будучи подібними до насичених вуглеводнів за елементним складом, відрізняються від них будовою – наявністю кратних зв’язків –подвійного і потрійного. Чи це позначається на їхніх хімічних властивостях?
(думки дітей про реакції окиснення, приєднання)
3.Досліджуємо хімічні властивості ацетилену. –пояснення з мультимедійним супроводом, складання учнями опорного конспекту.
1.Горіння (повне окиснення) ацетилену.
- Порівняйте, яким полум'ям горять метан, етилен? А яким полум’ям горить ацетилен.
- Як пояснити цю відмінність?
Горіння (повне окиснення):
2С2Н2 + 5О2 -> 4СО2 + 2Н2О
Горить кіптявим полум’ям. Під час горіння в середовищі кисню температура полум’я досягає 3200 С . Цю властивість використовують під час зварювання металів.
Правила техніки безпеки
Суміш ацетилену з киснем і повітрям вибухонебезпечні.
2.Часткове окиснення (КМп04): знебарвлення розчину марганцівки.
3.Реакції приєднання: відбуваються за місцем розриву π-зв’язків у дві стадії.
а) Якісна реакція на ацетилен — це реакції приєднання Брому за місцем потрійного зв'язку (реакція галогенування).
СН ≡ СН + Вч2 СНВч ═ СHВч
СНВч ═ СHВч + Вч2 СНВч2 - СНВч2
Під час реакції бромна вода (розчин брому у воді) знебарвлюється, червоно-буре забарвлення зникає.
б) приєднання водню – реакція гідрування –каталітична.
СН ≡ СН+Н2 СН2=СН2
СН2 =СН2 +Н2 СН3– СН3
4.Застосування ацетилену.- слайд
Знання про властивості різних речовин, а в нашому випадку ацетилену, дозволяють зрозуміти, як ці речовини можна використати.
5. Добування ацетилену.
а) піроліз метану;
б) карбідний спосіб: (потребує великих затрат електроенергії)
СаС2 +Н2ОС2Н2+ Са(ОН)2
V. Закріплення вивченого матеріалу
Вправа «Закінчи речення»
- Алкіни – це вуглеводні із…
- Потрійний зв'язок складається з …
- Найпростіший вуглеводень із потрійним зв’язком…
- Продукти горіння ацетилену…
- Для ацетилену характерні реакції…
- Якісна реакція на потрійний зв'язок…
Вправа «Здійсни перетворення»
С СН4 С2Н2 А С2Н6 В
Б
VІ. Рефлексія
-Чи виконали ми те, що планували на початку уроку?
-Чи на всі питання отримали відповіді?
Чи потрібні нам знання про ацетилен?
Оцінювання учнів (оцініть свою роботу на уроці)
VІІ.Домашнє завдання
Опрацювати § 22
Вправа «Попрацюй творчо». Складіть ланцюжок перетворень за участю алканів, алкенів і алкінів.
Запам’ятайте найголовніше – слайди


про публікацію авторської розробки
Додати розробку
