Практична робота №2Виведення молекулярної формули речовини за загальною формулою гомологічного ряду та густиною або відносною густиною. Виведення молекулярної формули речовини за
Практична робота №2
Тема: Виведення молекулярної формули речовини за загальною формулою гомологічного ряду та густиною або відносною густиною.
Виведення молекулярної формули речовини за масою, об’ємом або кількістю речовини реагентів або продуктів реакції.
Теоретична частина
Виведення молекулярної формули речовини за загальною формулою гомологічного ряду та густиною або відносною густиною.
В органічні хімії існує таке поняття, як загальна формула гомологічного ряду. Використовуючи її та знаючи молярну масу, можна легко визначити молекулярну формулу будь-якого членна гомологічного ряду
|
Алкани |
Алкени |
Алкіни |
Арени |
|
CnH2n+2 |
CnH2n |
CnH2n-2 |
CnH2n-6 |
|
Загальні формули для обчислення молярної моаси: |
|||
|
М(CnH2n+2) = 14n +2 |
М(CnH2n) = 14n |
М(CnH2n-2) = 14n -2 |
М(CnH2n-6) = 14n-6 |
Алгоритм розв'язування задач
1. Скласти загальну формулу класу сполук.
2. За формулою відносної густини обчислити відносну молекулярну масу.
3. За формулою відносної молекулярної маси визначити кількість атомів елементів у сполуці.
Задача 1. Відносна густина алкану за повітрям становить 3,93. Визначте формулу алкану.
Дано:
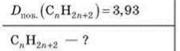
Розв’язання
1. Яка відносна молекулярна маса алкану?
![]()
2. Яка формула сполуки?
![]()
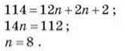
Відповідь: C8H18.
Задача 2. Маса 1 л алкену за н. у. дорівнює 1,875 г. Визначте формулу алкену.
Дано:
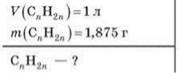
Розв’язання
1. Яка відносна молекулярна маса алкену?
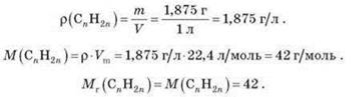
2. Яка формула сполуки?
![]()
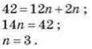
Відповідь: C3H6.
Задача 3. Визначить формулу алкану, відносна молекулярна маса якого – 100 а.о.
|
Дано: |
|
|
|
Мr (алкану) = 100 |
Мr (CnH2n + 2) = n • Аr(С) + 2•n•Аr(Н) + 2 |
Аr(С) = 12 |
|
|
|
Аr(Н) = 1 |
|
CnH2n + 2 - ? |
|
|
|
|
||
|
Алгоритм розв’язання |
||
|
1. За загальною формулою відносна молекулярна маса дорівнює: |
||
|
Мr (CnH2n + 2) = n • Аr(С) + 2•n • Аr(Н) + 2 |
||
|
Мr (CnH2n + 2) = 12n + 2n + 2 |
||
|
2. Обчислюємо n: |
||
|
100 = 14n + 2 |
||
|
100 – 2 = 14n |
||
|
98 = 14n |
||
|
n = 7 |
||
|
3. Підставляємо n у формулу С7Н16 |
||
|
|
||
|
Відповідь: формула алкану - С7Н16 |
||
Виведення молекулярної формули речовини за масою, об’ємом або кількістю речовини реагентів або продуктів реакції.
Коли згоряють органічні речовини, у складі яких містяться Карбрн, Гідроген, а також Оксиген, завжди утворюються одні і ті самі продукти - вуглекислий газ і вода.
Задача Спалили вуглеводень масою 8,6г. Утворився карбон (ІV) оксид масою 26,4 г і вода масою 12,6 г. Густина пари вуглеводню за метаном – 5,375.
Знайдіть молекулярну формулу сполуки
|
Дано: |
|
|
||||||||||||||||
|
m( CxHy) = 8.6 г |
Мr (CnH2n + 2) = n • Аr(С) + 2•n•Аr(Н) + 2 |
Аr(С) = 12 |
||||||||||||||||
|
m(СО2) = 26,4 г |
|
Аr(Н) = 1 |
||||||||||||||||
|
m(Н2О) = 12,6 г |
|
D |
= |
Мr1 |
|
Мr(СН4)= 16 |
||||||||||||
|
D(СН4) = 5,375 |
|
Мr2 |
|
|
||||||||||||||
|
|
Мr1 = D • Мr2 |
|
||||||||||||||||
|
CxHy - ? |
|
|
||||||||||||||||
|
|
||||||||||||||||||
|
І спосіб |
||||||||||||||||||
|
1. Пам’ятаючи, що маса речовини до реакції дорівнює масі речовини після |
||||||||||||||||||
|
реакції , обчислюємо масу вуглецю і водню в певній масі продуктів реакції: |
||||||||||||||||||
|
Мr(СО2) = 44; m( 1 моль СО2) = 44 г |
||||||||||||||||||
|
44 г (СО2) - 12 г (С) |
||||||||||||||||||
|
26,4 г - х г |
||||||||||||||||||
|
|
х |
= |
26,4 г • 12 г |
= |
7,2 г (С) |
|
||||||||||||
|
|
44 г |
|
||||||||||||||||
|
2. Аналогічно обчислюємо масу водню |
||||||||||||||||||
|
Мr(Н2О) = 18; m( 1 моль Н2О) = 18 г |
||||||||||||||||||
|
18 г (Н2О) - 2 г (Н) |
||||||||||||||||||
|
12,6 г - у г |
||||||||||||||||||
|
|
у |
= |
12,6 г • 2 г |
= |
1,4 г (Н) |
|
|
26,4 г * 12 г |
= |
7,2 7 (С) |
|
|||||||
|
|
18 г |
|
44 г |
|
|
|
||||||||||||
|
3. Знаходимо атомів у молекулі. Для цього маси вуглецю і водню ділимо |
|
|
|
|
||||||||||||||
|
на їх відносні атомні маси:
|
|
|
|
|
||||||||||||||
|
|
7,2 |
= |
0,6 |
|
1,4 |
= |
1,4 |
|
|
|
|
|
||||||
|
|
12 |
1 |
У цілих числах: 6 : 14 |
|
|
|
|
|||||||||||
|
4. Зі відносною густиною обчислюємо відносну молекулярну масу: |
|
|
|
|
||||||||||||||
|
Мr(речовини) = D • Мr(СН4) |
|
|
|
|
||||||||||||||
|
Мr(речовини) = 5,375 • 16 = 86 |
|
|
|
|
||||||||||||||
|
5. Формула - С6Н14; Мr (С6Н14) = 12•6 + 1 • 14 = 86 |
|
|
|
|
||||||||||||||
|
|
|
|
|
|
||||||||||||||
|
Відповідь: формула вуглеводню - С6Н14 |
|
|
|
|
||||||||||||||
ІІ спосіб
|
1. СхНу + О2 = СО2 + Н2О |
||||||||||
|
2. |
ʋ (СО2) |
= |
26,4 |
= |
0,6моль; |
ʋ (Н2О) |
= |
12,6 |
= 0,7моль |
|
|
44 |
18 |
|||||||||
|
3. ʋ (С) = ʋ (СО2) = 0,6моль ʋ(Н) = 2 ʋ(Н2О) = 2•0,7 = 1,4моль |
||||||||||
|
4. ʋ (С) : ʋ(Н) = 0,6:1,4 у цілих 6 :14 |
||||||||||
|
5. Мr(речовини) = D • Мr(СН4) = 5,375 • 16 = 86 |
||||||||||
|
6. Мr(С6Н14) = 86 ; 86=86 |
||||||||||
|
Відповідь: формула С6Н14 - гексан |
||||||||||
ІІІ спосіб
|
1. Мr(СхНу) = D • Мr(СН4) = 5,375 • 16 = 86 |
|||||||||
|
8,6 26,4 12,6 |
|||||||||
|
2. 2 СхНу + О2 → 2х СО2 + уН2О |
|||||||||
|
2•86 2х•44 у•18 3. |
|||||||||
|
8,6 |
= |
26,4 |
|
|
8,6 |
= |
12,6
|
|
|
|
2• 86 |
2х•44 |
|
|
2• 86 |
у•18
|
|
|||
|
х = 6 у = 14 |
|||||||||
|
4. ʋ (С) : ʋ(Н) = 6 : 14 |
|||||||||
Відповідь: формула С6Н14 - гексан
Завдання вхідного контролю
1. Відносна атомна маса позначається...
2. Відносна молекулярна маса позначається...
3. Відносна молекулярна маса речовини обчислюється за формулою...
4. Густина позначається...
5. Густина речовини обчислюється за формулою...
6. Масову часку елемента в складній речовині обчислюють за формулою...
7. Відносна густина газів позначається...
8. Відносна густина газів обчислюється за формулою...
9. Відносна густина газу за воднем обчислюється за формулою...
10. Відносна густина газу за повітрям обчислюється за формулою...
ХІД РОБОТИ
ВАРІАНТ 1
1. Складіть молекулярну формулу вуглеводню гомологічного ряду метану, що містить 16 атомів Гідрогену.
Напишіть скорочені структурні формули двох ізомерів.
Обчисліть відносну густину за воднем і за повітрям.
2.Відносна густина алкану за воднем дорівнює 22. Який це алкан?
3. Під час спалювання органічної речовини масою 3г утворився вуглекислий газ масою 8,8г і вода масою 5,4г. Відносна густина випарів цієї речовини за воднем дорівнює 15. Визначте молекулярну формулу цієї органічної речовини.
ВАРІАНТ 2
1. Складіть молекулярну формулу вуглеводню гомологічного ряду етену, що містить 12 атомів Гідрогену.
Напишіть скорочені структурні формули двох ізомерів.
Обчисліть відносну густину за киснем і за повітрям.
2.Відносна густина алкену за повітрям дорівнює 1,44. Який це алкен?
3. Під час спалювання органічної речовини масою 10г утворився вуглекислий газ масою 27,5г і вода масою 22,5г. Відносна густина випарів цієї речовини за киснем дорівнює 0,5. Визначте молекулярну формулу речовини.
ВАРІАНТ 3
1. Складіть молекулярну формулу вуглеводню гомологічного ряду етину, що містить 12 атомів Гідрогену.
Напишіть скорочені структурні формули двох ізомерів.
Обчисліть відносну густину за воднем і за азотом.
2.Відносна густина алкіну за киснем дорівнює 1,25. Який це алкін?
3. Після згоряння речовини масою 4,25г утворився оксид Карбону (IV) масою 13,2 і вода масою 5,85г. Відносна густина парів цієї речовини за повітрям дорівнює 5,862. Визначте формулу речовини.
ВАРІАНТ 4
1. Складіть молекулярну формулу вуглеводню гомологічного ряду алкенів, що містить 14 атомів Гідрогену.
Напишіть скорочені структурні формули двох ізомерів.
Обчисліть відносну густину за воднем і за повітрям.
2. Відносна густина ароматичного вуглеводню за воднем дорівнює 39. Який це вуглеводень?
3. Визначте істину формулу вуглеводню, під час спалювання якого масою 4,4г одержали карбон (IV) оксид масою 13,2г і воду масою 7,2г. Відносна густина його випарів за воднем дорівнює 22.
Практична робота №2
ВАРІАНТ 1
Завдання вхідного контролю
І
1. Відносна атомна маса позначається...
2. Відносна молекулярна маса позначається...
3. Відносна молекулярна маса речовини обчислюється за формулою...
4. Густина позначається...
5. Густина речовини обчислюється за формулою...
6. Масову часку елемента в складній речовині обчислюють за формулою...
7. Відносна густина газів позначається...
8. Відносна густина газів обчислюється за формулою...
9. Відносна густина газу за воднем обчислюється за формулою...
10. Відносна густина газу за повітрям обчислюється за формулою...
ІІ
1. Складіть молекулярну формулу вуглеводню гомологічного ряду метану, що містить 16 атомів Гідрогену.
Напишіть скорочені структурні формули двох ізомерів.
Обчисліть відносну густину за воднем і за повітрям.
2.Відносна густина алкану за воднем дорівнює 22. Який це алкан?
3. Під час спалювання органічної речовини масою 3г утворився вуглекислий газ масою 8,8г і вода масою 5,4г. Відносна густина випарів цієї речовини за воднем дорівнює 15. Визначте молекулярну формулу цієї органічної речовини.
_____________________________________________________________________________________
Практична робота №2
ВАРІАНТ 2
Завдання вхідного контролю
І
1. Масову часку елемента в складній речовині обчислюють за формулою...
2. Відносна густина газів позначається...
3. Відносна густина газів обчислюється за формулою...
4. Відносна густина газу за воднем обчислюється за формулою...
5. Відносна густина газу за повітрям обчислюється за формулою...
6. Відносна атомна маса позначається...
7. Відносна молекулярна маса позначається...
8. Відносна молекулярна маса речовини обчислюється за формулою...
9. Густина позначається...
10. Густина речовини обчислюється за формулою...
ІІ
1. Складіть молекулярну формулу вуглеводню гомологічного ряду етену, що містить 12 атомів Гідрогену.
Напишіть скорочені структурні формули двох ізомерів.
Обчисліть відносну густину за киснем і за повітрям.
2.Відносна густина алкену за повітрям дорівнює 1,44. Який це алкен?
3. Під час спалювання органічної речовини масою 10г утворився вуглекислий газ масою 27,5г і вода масою 22,5г. Відносна густина випарів цієї речовини за киснем дорівнює 0,5. Визначте молекулярну формулу речовини.
Практична робота №2
ВАРІАНТ 3
Завдання вхідного контролю
І
1. Відносна молекулярна маса позначається...
2. Відносна атомна маса позначається...
3. Густина позначається...
4. Відносна молекулярна маса речовини обчислюється за формулою...
5. Масову часку елемента в складній речовині обчислюють за формулою...
6. Густина речовини обчислюється за формулою...
7. Відносна густина газів обчислюється за формулою...
8. Відносна густина газів позначається...
9. Відносна густина газу за повітрям обчислюється за формулою...
10. Відносна густина газу за воднем обчислюється за формулою...
ІІ
1. Складіть молекулярну формулу вуглеводню гомологічного ряду етину, що містить 12 атомів Гідрогену.
Напишіть скорочені структурні формули двох ізомерів.
Обчисліть відносну густину за воднем і за азотом.
2.Відносна густина алкіну за киснем дорівнює 1,25. Який це алкін?
3. Після згоряння речовини масою 4,25г утворився оксид Карбону (IV) масою 13,2 і вода масою 5,85г. Відносна густина парів цієї речовини за повітрям дорівнює 5,862. Визначте формулу речовини.
___________________________________________________________________________________
Практична робота №2
ВАРІАНТ 4
Завдання вхідного контролю
І
1. Відносна молекулярна маса речовини обчислюється за формулою...
2. Відносна атомна маса позначається...
3. Відносна густина газів позначається...
4. Відносна густина газу за воднем обчислюється за формулою...
5. Густина речовини обчислюється за формулою...
6. Відносна молекулярна маса позначається...
7. Густина позначається...
8. Масову часку елемента в складній речовині обчислюють за формулою...
9. Відносна густина газів обчислюється за формулою...
10. Відносна густина газу за повітрям обчислюється за формулою...
ІІ
1. Складіть молекулярну формулу вуглеводню гомологічного ряду алкенів, що містить 14 атомів Гідрогену.
Напишіть скорочені структурні формули двох ізомерів.
Обчисліть відносну густину за воднем і за повітрям.
2. Відносна густина ароматичного вуглеводню за воднем дорівнює 39. Який це вуглеводень?
3. Визначте істину формулу вуглеводню, під час спалювання якого масою 4,4г одержали карбон (IV) оксид масою 13,2г і воду масою 7,2г. Відносна густина його випарів за воднем дорівнює 22.
-
-
-
Дякую


про публікацію авторської розробки
Додати розробку
