Презентація "Алкіни"
Про матеріал
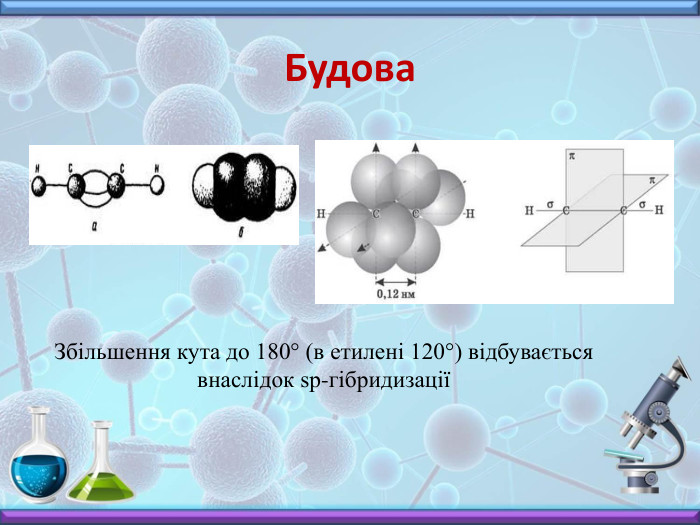
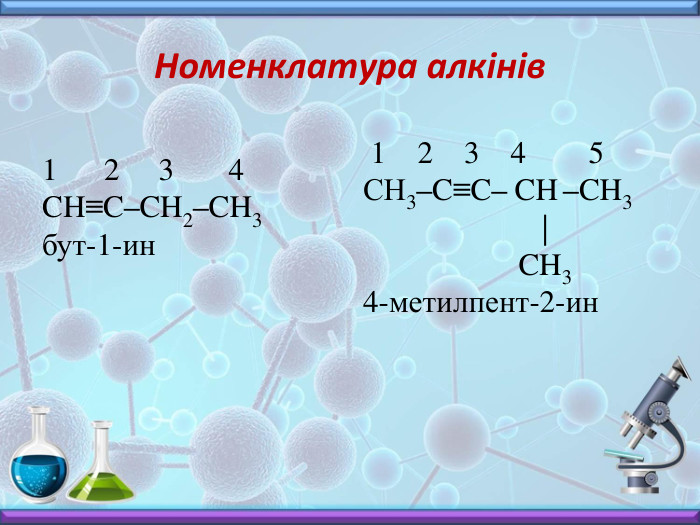
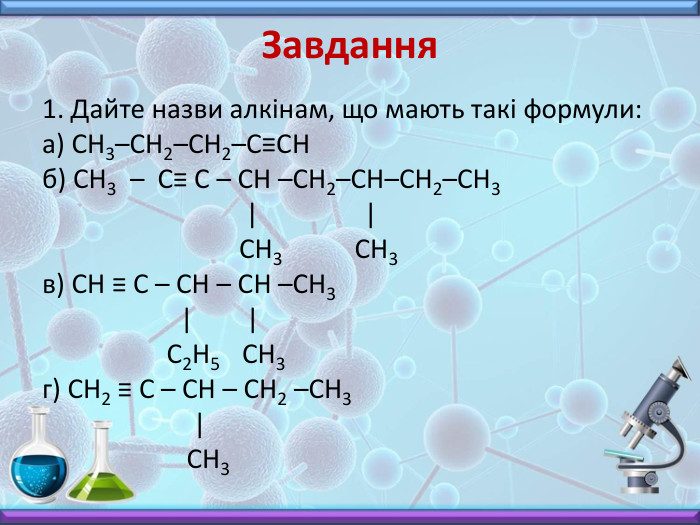
Презентація з хімії до вивчення теми "Алкіни" у 10 класі. Містить інформацію про будову, номенклатуру, фізичні властивості, хімічні взаємодії та застосування алкінів. Включає завдання до цієї теми, необхідні для закріплення матеріалу. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку