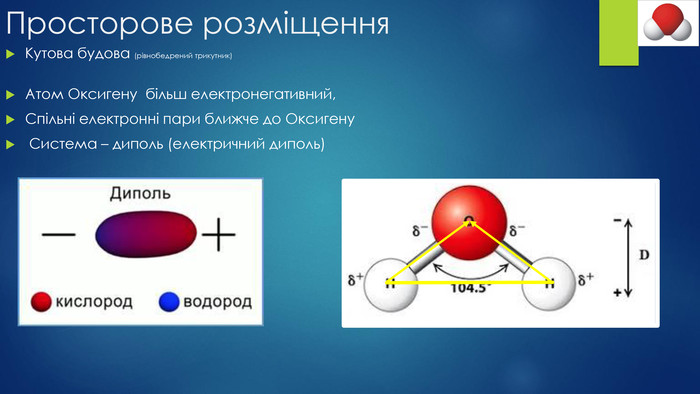
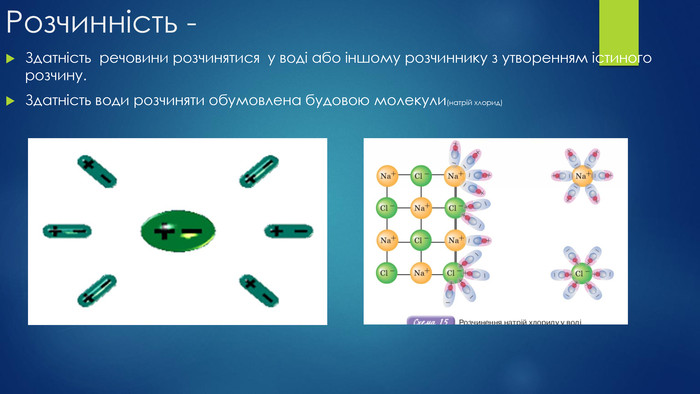
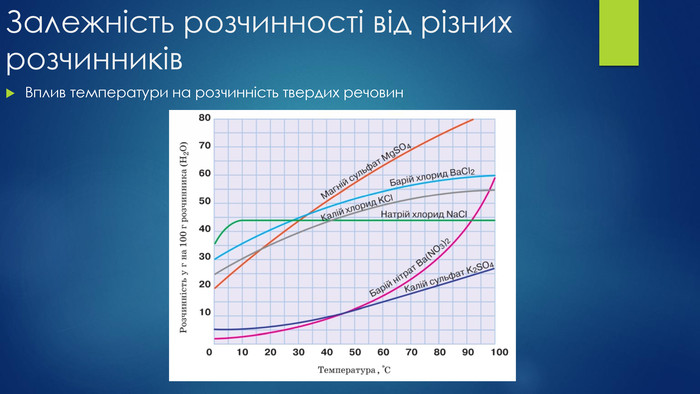
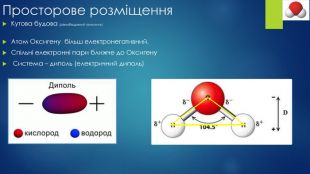
Презентація "Будова молекули води, поняття про водневий зв’язок"
Про матеріал
Презентація "Будова молекули води, поняття про водневий зв’язок", за Підручником Ярошенко О.Г., 9 клас, 2017 року Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
-
Дякую!
-
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку