Презентація до уроку, 10 клас."Анілін"
Про матеріал
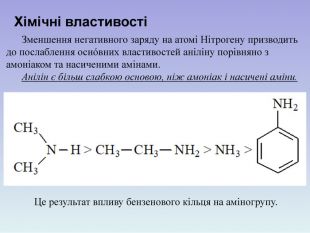
Презентація містить завдання для актуалізації опорних знань з теми «Аміни», в ній розглянуто будову молекули аніліну, фізичні, хімічні властивості, добування та застосування аніліну. Презентацію можна викостовувати під час вивчення теми «Анілін» в 10 класі. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
ppt
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку




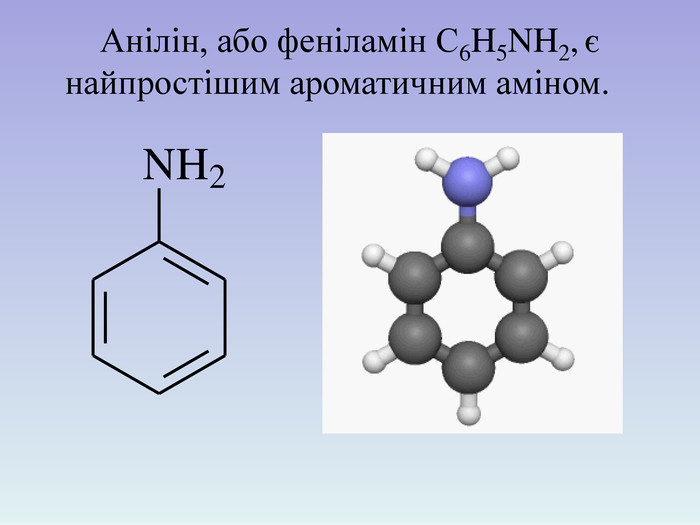
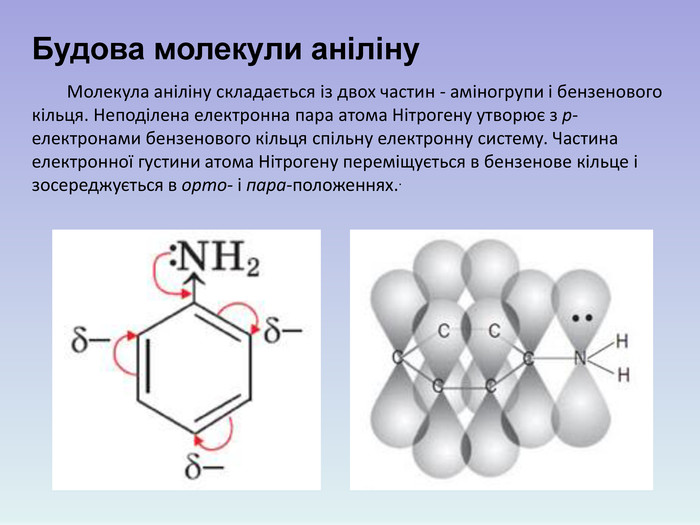

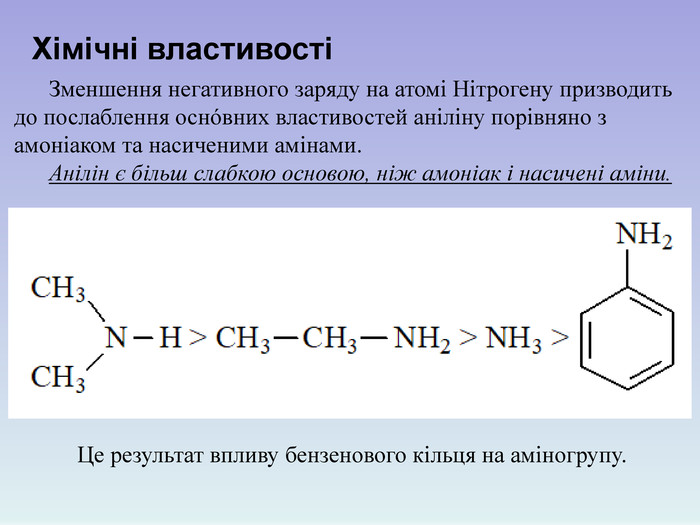
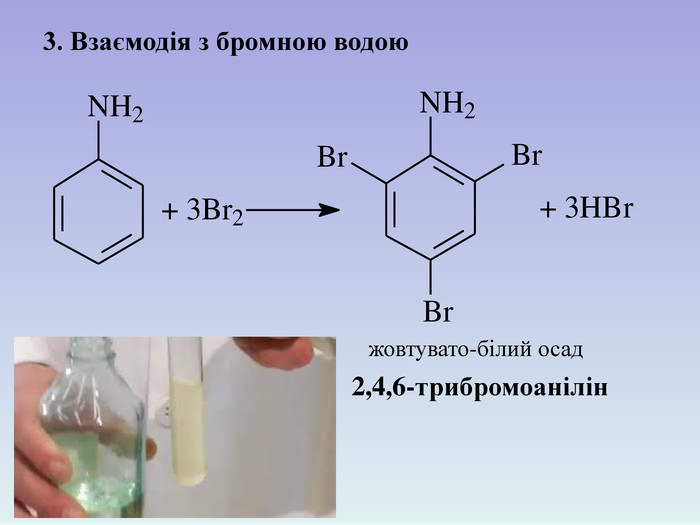
![C6H5NH2 + H+ → [C6H5NH3]+. йон феніламонію Розчинність аніліну в воді незначна. У водному розчині аніліну майже немає йонів ОН–; індикатори в ньому не змінюють свого забарвлення: 1. Взаємодія з водою C6H5NH2 + H+ → [C6H5NH3]+. йон феніламонію Розчинність аніліну в воді незначна. У водному розчині аніліну майже немає йонів ОН–; індикатори в ньому не змінюють свого забарвлення: 1. Взаємодія з водою](/uploads/files/895803/240469/259933_images/10.jpg)
![2. Взаємодія з кислотами Анілін взаємодіє лише із сильними кислотами: C6H5NH2 + HC1 → [C6H5NH3]Cl, анілін феніламоній хлорид C6H5NH2 + Н2SO4 → [C6H5NH3]HSO4. анілін феніламоній гідрогенсульфат 2. Взаємодія з кислотами Анілін взаємодіє лише із сильними кислотами: C6H5NH2 + HC1 → [C6H5NH3]Cl, анілін феніламоній хлорид C6H5NH2 + Н2SO4 → [C6H5NH3]HSO4. анілін феніламоній гідрогенсульфат](/uploads/files/895803/240469/259933_images/11.jpg)