Презентація до уроку: "Фізичні та хімічні властивості гомологів метану"



























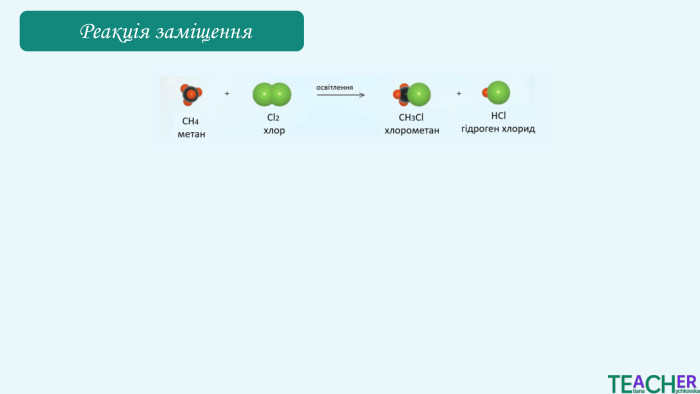
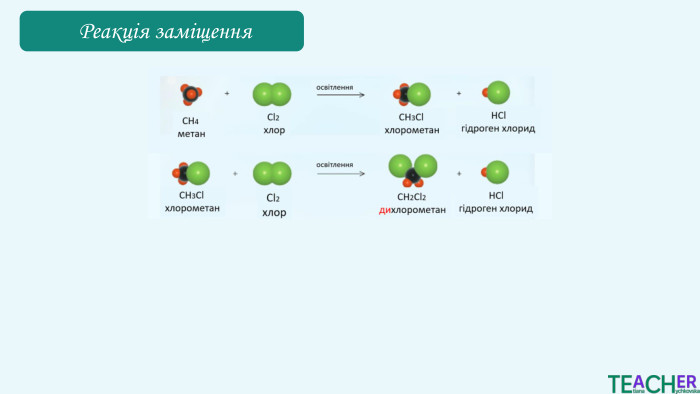
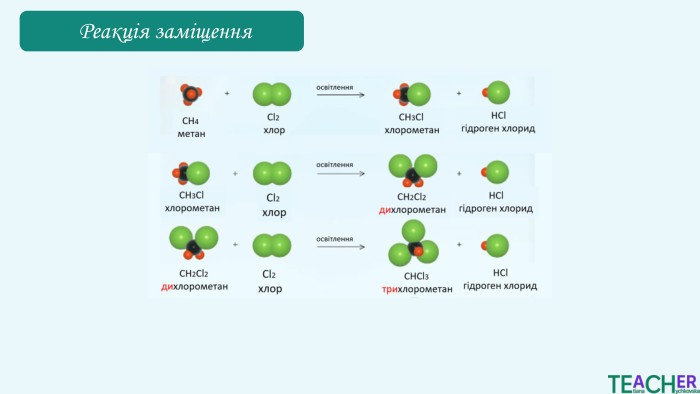
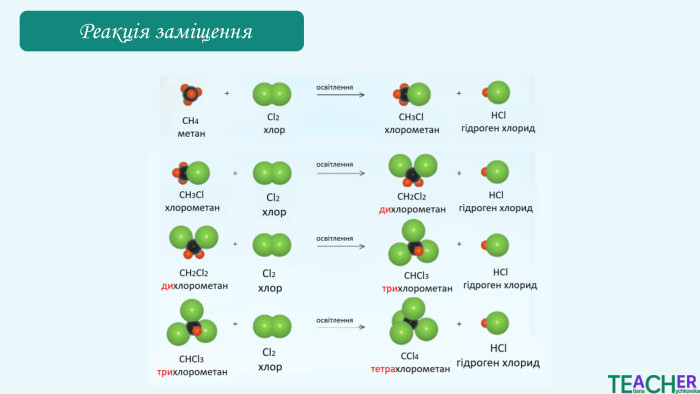
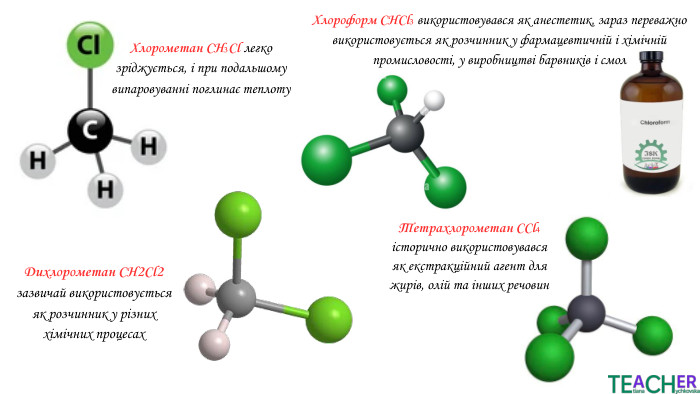


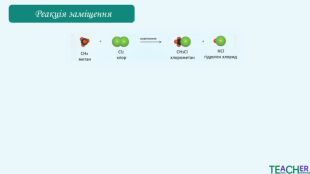
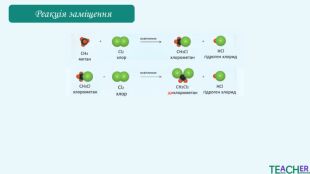
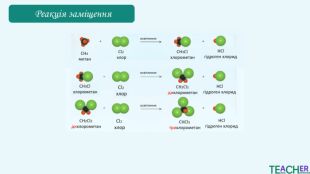
Хлорометан CH₃Cl легко зріджується, і при подальшому випаровуванні поглинає теплоту. Дихлорометан СН2 Сl2 зазвичай використовується як розчинник у різних хімічних процесах. Хлороформ CHCl₃ використовувався як анестетик, зараз переважно використовується як розчинник у фармацевтичній і хімічній промисловості, у виробництві барвників і смол. Тетрахлорометан CCl₄ історично використовувався як екстракційний агент для жирів, олій та інших речовин
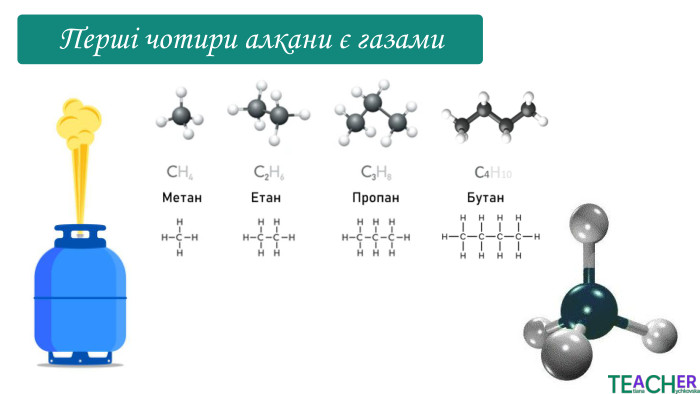
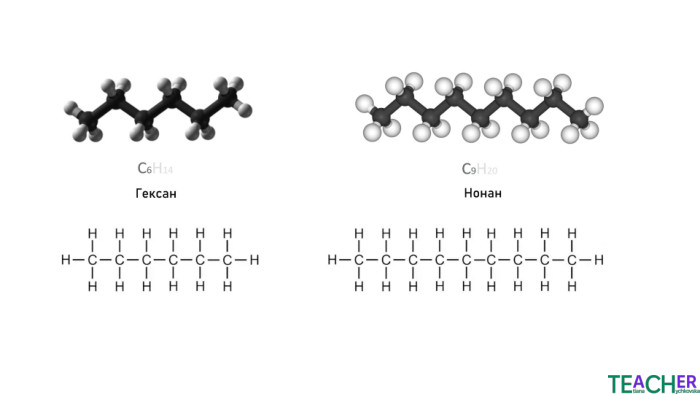
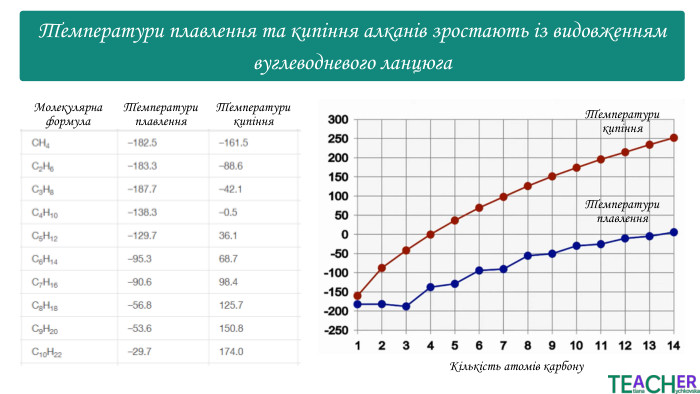
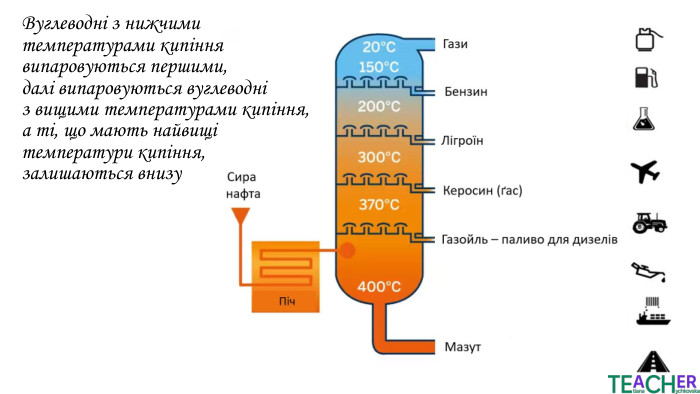
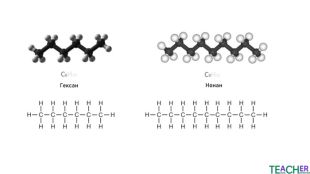
Коротко про головне. Перші чотири алкани є газами, від 5 до 17 - рідинами, при більшій кількості атомів карбону вуглеводні є твердими речовинами. Газоподібні і тверді алкани не мають запаху, а рідкі – характерний «бензиновий» запах. Температури плавлення та кипіння зростають із видовженням вуглеводневого ланцюга. Для алканів характерна реакція горіння. При надлишку кисню утворюються вуглекислий газ і вода, при нестачі – чадний газ або вуглець і вода. Для алканів характерна реакція заміщення. В результаті утворюються галогенопохідні сполуки


про публікацію авторської розробки
Додати розробку

































-

Alla Alla
17.01.2026 в 14:17
Дякую
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Шкідченко Надія Миколаївна
08.04.2025 в 15:46
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Теплова teplova-m
03.02.2025 в 07:47
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Процюк Лариса Вікторівна
12.02.2024 в 21:51
Всі презентації просто чудові ! Натхнення , бажання, сили.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Школьник Олександр Григорович
12.02.2024 в 10:04
Дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Пашаєва Тетяна Миколаївна
21.01.2024 в 23:05
Дуже вдячна!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 3 відгука