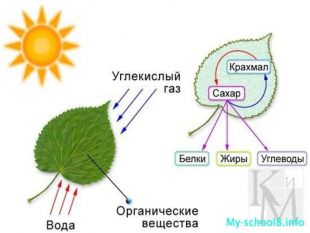
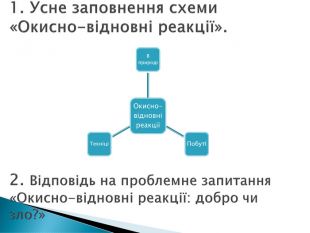
Презентація до уроку хімії "Окисно-відновні реакції" 9 клас
Про матеріал
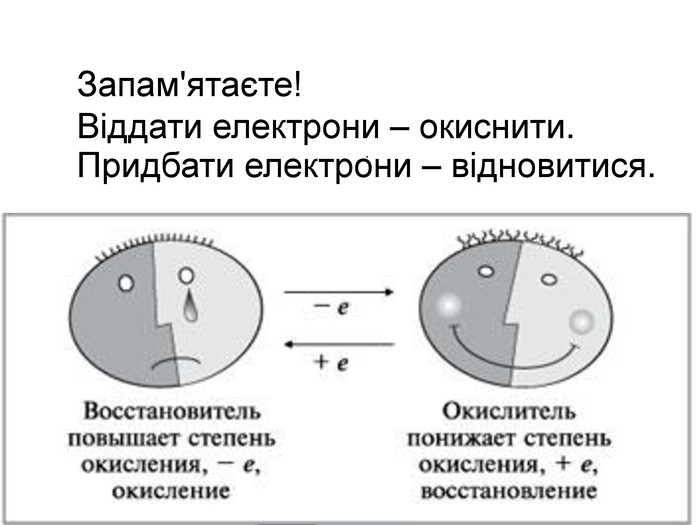
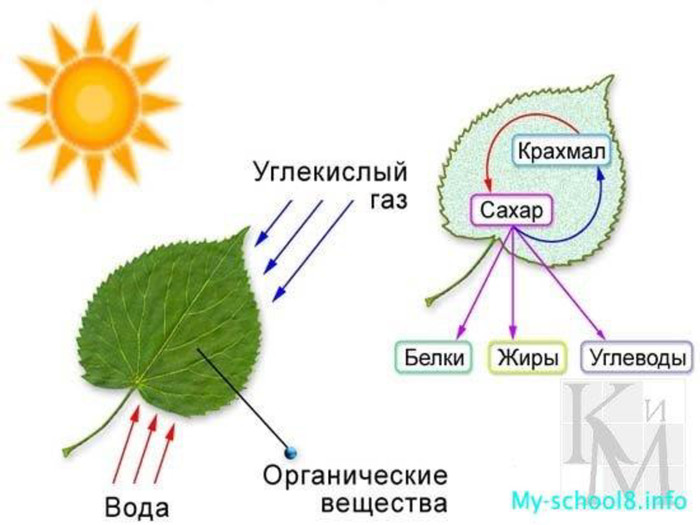
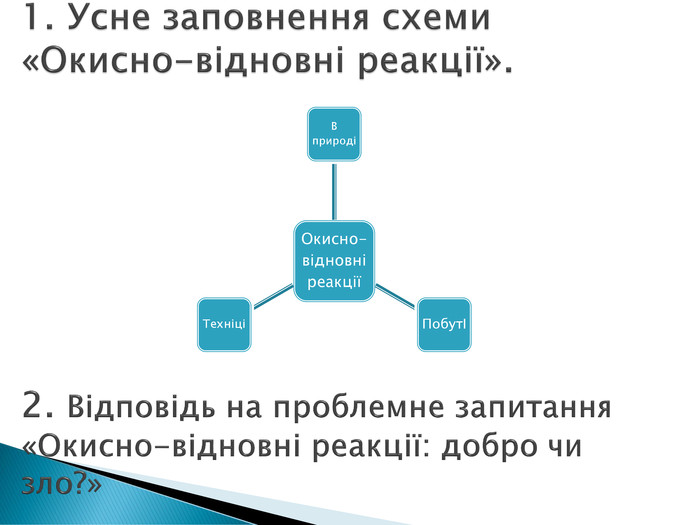
Мета: Розкрити роль окисно-відновних реакцій в природі, техніці та житті людини; продовжити відпрацювання навичок визначати ступені окиснення елементів, окисник і відновник в рівняннях реакції, урівнювати реакції методом електронного балансу, розвивати пізнавальну активність учнів, хімічну мову, мислення, сприяти розширенню їх світогляду, формувати життєві компетенції; виховувати творче ставлення до практичного використання знань з хімії. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку