Презентація до уроку хімії в 9 класі «Мило, його склад, мийна дія»






















Історія мила. За існуючими даними, мило виготовлялося ще в стародавньому Шумері та Вавилоні (приблизно 2800 років до н. е.), а Єгипетський папірус свідчить про те, що єгиптяни регулярно милися за допомогою мила. Одна з легенд пов’язує появу мила і навіть слова "soap" з горою Sapo, на якій в Стародавньому Римі спалювали туші принесених в жертву тварин. Жир тварин, який виділявся під час спалювання такої жертви, накопичувався та змішувався з попелом вогнищ (як природний луг), а потім змивався дощами в річку, в результаті чого вода починала пінитися і добре змивати весь бруд з тканини. Саме тоді помітили той факт, що завдяки цій суміші, одяг почав пратися набагато легше.
Одна з перших публікацій про мило зустрічається у «Природній історії» Плінія Старшого. Він пише, що мило виготовляють з букової золи і козиного сала, а добули його гали для фарбування волосся в червоний колір. З тексту не зрозуміло, чи використовувалось мило з для інших цілей. У відомому папірусі Еберса – медичний древньогрецький рукопис, знайдений в 1872 р, до ХІ ст. до н.е. мило згадується як лікарський препарат. Миловаріння як ремесло виникло в Європі у XIV ст. В секрети виробництва мила перейняли від Візантії. Майстри миловаріння появились лише у XV ст. Перші синтетичні мийні засоби зявились в 1916 р. Винахід німецького хіміка Фріца Понтера мав лише промислове застосування. Побутові синтетичні мийні засоби не шкідливі для рук стали випускати у 1933р.
Лише на рубежі 18-19 століть була виявлена хімічна природа жирів і внесена ясність у реакцію їхнього омилення. 1779 року шведський хімік Шеєле показав ,що під час взаємодії оливкової олії з плюмбум оксидом і водою утворюється солодка і розчинна у воді речовина. Вирішальний крок на шляху вивчення хімічної природи жирів зробив французький хімік Шеврель. Він відкрив стеаринову, пальмітинову і олеїнову кислоти, як продукти розкладу жирів під час їхнього омилення водою і лугами. Солодку речовину, яку одержав Шеєле, Шеврель назвав гліцерином.
Вчений Леблан розробив порівняно простий і дешевий спосіб виробництва каустичної соди (Na2 CO3), потрібної для приготування із цих жирів мила. У перших миловарнях усі складники змішували і варили у величезних відкритих котлах. Досвідчений миловар помішував цю суміш спеціальною лопаткою. Залежно від того, як мило стікало по ній, він знав який складник слід додати або скільки і як ще треба варити мило.
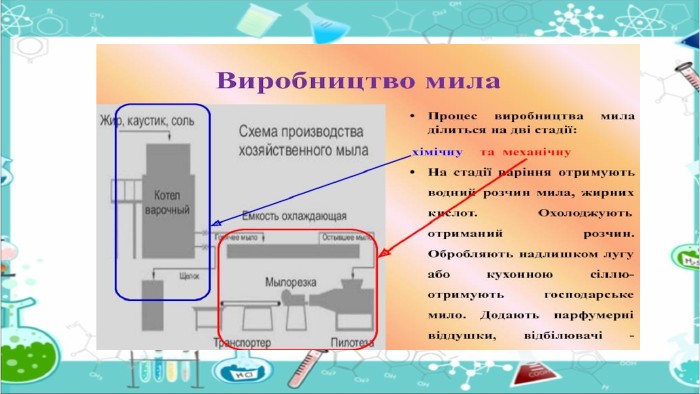
Сьогодні технологічний процес виготовлення мила складається з трьох основних етапів. Перший етап — це омилення. До різних олій та жирів додають луг, внаслідок чого утворюється суміш з чистого мила, гліцерину та 30 відсотків води. Іноді для того, аби отримати цю суміш, мило, як і раніше, варять у котлах, але в більш сучасних миловарнях цим процесом керує комп’ютеризована система. Другий етап — сушка. Очищене мило подають в розпилювальну сушку, де у вакуумі та при високій температурі воно перетворюється на маленькі гранули з вмістом води лише 12 відсотків. На третьому, завершальному етапі мильні гранули змішують з різними ароматизаторами, барвниками та іншими додатками. Наприкінці мило нарізають кусочками або ж заливають у відповідні форми.
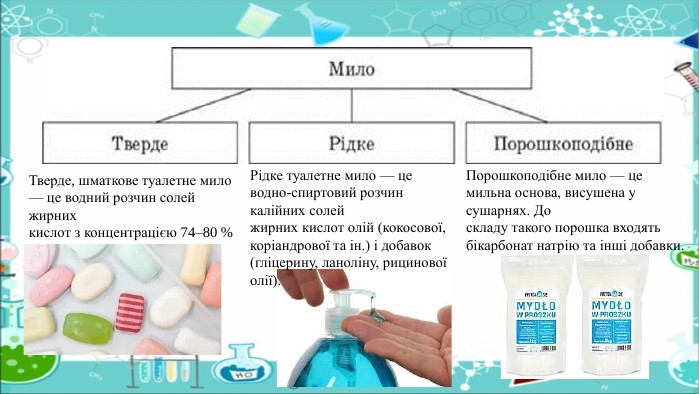
Порошкоподібне мило — це мильна основа, висушена у сушарнях. Доскладу такого порошка входять бікарбонат натрію та інші добавки. Рідке туалетне мило — це водно-спиртовий розчин калійних солейжирних кислот олій (кокосової, коріандрової та ін.) і добавок (гліцерину, ланоліну, рицинової олії). Тверде, шматкове туалетне мило — це водний розчин солей жирнихкислот з концентрацією 74–80 %
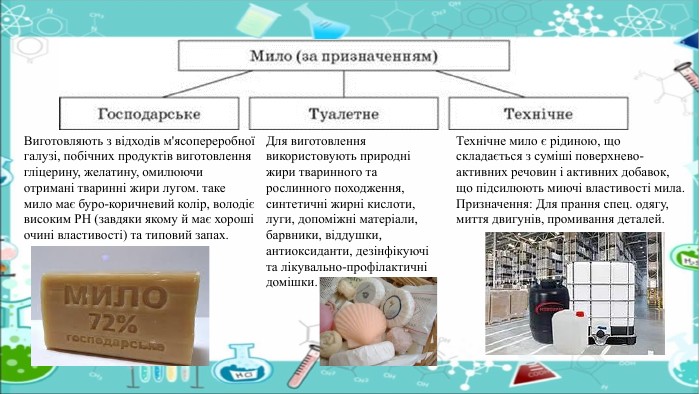
Виготовляють з відходів м'ясопереробної галузі, побічних продуктів виготовлення гліцерину, желатину, омилюючи отримані тваринні жири лугом. таке мило має буро-коричневий колір, володіє високим РН (завдяки якому й має хороші очині властивості) та типовий запах. Для виготовлення використовують природні жири тваринного та рослинного походження, синтетичні жирні кислоти, луги, допоміжні матеріали, барвники, віддушки, антиоксиданти, дезінфікуючі та лікувально-профілактичні домішки. Технічне мило є рідиною, що складається з суміші поверхнево-активних речовин і активних добавок, що підсилюють миючі властивості мила. Призначення: Для прання спец. одягу, миття двигунів, промивання деталей.
Мила – це солі лужних елементів і вищих карбонових кислот, переважно стеаринової та пальмітинової з добавками барвників, запашних речовин, антисептиків, тощо. Властивості мила залежать не лише від природи жирної кислоти, яка входить до її складу, але й від катіона: натрієві солі є твердими речовинами, калієві – рідкими. Більшість властивостей мила, наприклад, твердість, розчиненість у воді залежить від його жирового складу. Так пальмітинова кислота надає милу твердості і гарні піноутворюючі якості, а олеїнова кислота – розчинність у холодній воді і миючу здатність. Стеаринова кислота посилює миючу здатність мила у гарячій воді. Якщо атомів Карбону в аніоні солі менше 10, то сполука не виявляє мийної дії, а якщо більше 20, то сіль практично нерозчинна у воді.
Процес миловаріння полягає в нагріванні жирів з лугами (омилення жирів): Процес миловаріння. До утвореної в’язкої рідини добавляють насичений розчин кухонної солі, для зменшення розчинності мила. Мило виділяється з розчину і спливає на поверхню. Цей процес називають висолюванням. Мило збирають і заповнюють ним форми, де воно твердне.
При горінні мила утворюються вуглекислий газ ,вода та мінеральна сіль, що ускладнює подальший хід процесу. Так, якщо повністю окиснити натрій стеарат , то утворюється СО2, Н2 О і Na2 CO3. Однак, у реальних умовах не весь Карбон ,що міститься в милі,прореагує з киснем, і спостерігається виділення вуглецю у вигляді сажі.2 C17 H35 COONa + 52 02 → 35 С02 + 35 Н20 + Na2 CO3
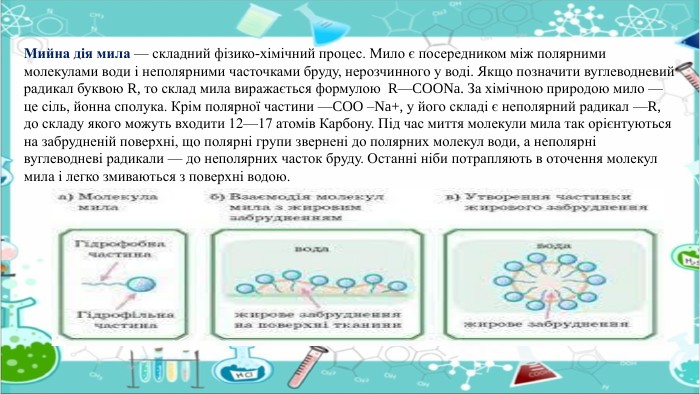
Мийна дія мила — складний фізико-хімічний процес. Мило є посередником між полярними молекулами води і неполярними часточками бруду, нерозчинного у воді. Якщо позначити вуглеводневий радикал буквою R, то склад мила виражається формулою R—COONa. За хімічною природою мило — це сіль, йонна сполука. Крім полярної частини —COO –Na+, у його складі є неполярний радикал —R, до складу якого можуть входити 12—17 атомів Карбону. Під час миття молекули мила так орієнтуються на забрудненій поверхні, що полярні групи звернені до полярних молекул води, а неполярні вуглеводневі радикали — до неполярних часток бруду. Останні ніби потрапляють в оточення молекул мила і легко змиваються з поверхні водою.
Чому мило не милиться у твердій воді?У твердій воді утворюються нерозчинні магнієві та кальцієві солі карбонових кислот, через це мило втрачає свою мийну дію, а солі осідають на поверхні виробу:2 C17 H35 COONa + Mg. CO3 → (C17 H35 COO)2 Mg↓ + Na2 CO3 Синтетичні мийні засоби, за всієї різноманітності їх хімічного складу, мають подібну до мила будову молекул, в яких є розчинна у воді полярна частина і нерозчинний неполярний вуглеводневий радикал. Але вони, на відміну від мила, є солями іншої хімічної природи і у твердій воді не утворюють нерозчинних сполук. У цьому полягає перевага синтетичних мийних засобів над натуральним милом.
Синтетичні мийні засоби (СМЗ) – складні суміші, які крім мийної основи, містять різні добавки Синтетичні мийні засоби є солями іншої хімічної природи й у твердій воді не утворюють нерозчинних сполук. Це і рідке мило, шампуні, гелі для душу, піна для ванн, пральні порошки, пасти та інші. До складу СМЗ крім мийної основи входять ензими, відбілювачі, стабілізатори піни, пом’якшувачі та ін.
Порівняння мила й СМЗ Ознаки. Мила. Синтетичні миючі засоби. Сировина. Жири, у т. ч. харчові, що є дефіцитними (в рік до 300 тис. тонн жиру для одної країни). Вищі жирні спирти, які добувають з нафти. Температура миття. Гаряча вода, або кип’ятіння. У будь-якій воді, краще при температурі +25-35°С. Вплив на тканину. Не корисно для деяких тканин: синтетичні при кип’ятінні плавляться, у шовкових погіршується міцність. Якість тканини і колір, не змінюється. Твердість води. У твердій воді миє погано, тому що з йонами Са2+, Мg2+ утворює нерозчинні солі. На осадження солей кальцію і магнію витрачається багато мила. Нерозчинні солі осідають на тканині (особливо на шерстяних), плавають у воді. Успішно миють у твердій і морській воді, тому що не взаємодіють з солями магнію і кальцію, нерозчинних солей не утворюють. Дія на шкіру рук. Мило легко гідролізується водою з утворенням лугу, який шкідливий для шкіри рук. На шкіру не діють (за невеликим винятком). Вплив на оточуюче середовище. Легко розкладаються, не шкідливі. Багато СМЗ повільно або майже не руйнуються біологічним способом за допомогою мікроорганізмів. Шкідливі для оточуючого середовища. Витрати на миття. Залежать від твердості води: чим більша твердість, тим більші витрати. Добре миють в розбавлених розчинах. У концентрованих розчинах утворюють міцели – мийні властивості спадають. Необхідно дотримуватись норм на упаковках.
Вплив мила на організм людини та навколишнє середовище. Мило добре піниться і гарно очищає, дезінфікує, бо має в своєму складі луги, є гіпоалергенним за умови якщо в ньому натуральні компоненти. В навколишньому середовищі мило легко нейтралізується, утворює осади з Мg2+ та Са2+ і тому не шкодить живим організмам. Але мило також має і деякі побічні ефекти, такі як: - луг пошкоджує шкірний жир – захисну оболонку шкіри, одне і те ж мило не завжди підходить для різних типів шкіря;- мило «змиває» позитивний заряд з шкіри, тому мікроби до неї буквально просто «липнуть»;- під дією лугу руйнуються натуральні тканини, барвники, якими пофарбована тканина.
Вплив СМЗ на організм людини та навколишнє середовище. Синтетичні миючі засоби мають перевагу перед милами унаслідок величезної здатності до знежирення, відмінних змочуючих і піноутворюючих властивостей незалежно від жорсткості води, СМЗ проявляють мийну дію не тільки в гарячій воді, витрата CMC приблизно в 15 рази менше, ніж мила. Але: Основні активні речовини СМЗ – це так звані поверхнево активні речовини (ПАР). Маючи певну спорідненість з окремими компонентами мембран клітин, точніше, їх ліпідним шаром, вони здатні нагромаджуватися на цих мембранах, покриваючи поверхню клітини тонким шаром, а за певної одноразової концентрації або тривалого впливу мінідоз – руйнуючи її. Установлено, що ПАР здатні викликати суттєві порушення імунітету, викликати алергію, негативним чином впливати на функцію головного мозку, печінки, нирок.
Вплив СМЗ на організм людини та навколишнє середовище. Недоліком їх є важка біозасвоюваність в стічних водах мікроорганізмами, так як фактично для них це отрути. Тому стічні води, що містять синтетичні миючі засоби, сильно забруднюють водойми (ріки, озера). Попадання пар у водойми несприятливо впливає на органолептичні (колір, запах, смак) і бактеріологічні показники води. До мийних засобів додають фосфати, які у водоймах перетворюються на речовини, що живлять мікроорганізми. Вони починають швидко розмножуватись, а це спричиняє до так званого «цвітіння води» - евтрофікації, що в свою чергу призводить до зменшення кисню у воді, утворення мулу, заболочення водойм. СМЗ не утворюють нерозчинних солей на відміну від мила, тому, щоб стічні води очистити від СМЗ, їх треба піддавати тривалому біологічному і хімічному руйнуванню, а це на водоочисних спорудах не виконується, таким чином все, що не розклалось потрапляє нам у водопровід.
Людина, що називає себе Bubbleman, займається тим, що створює величезні мильні бульбашки (насправді його звати Сем Хіт і йому 38 років). Сем навіть встановив кілька світових рекордів. У тому числі надувши міхур, в який помістилося 50 чоловік. Зовсім недавно Bubbleman оновив свій рекорд, надувши 56 маленьких бульбашок усередині одного гігантського. Таким чином він побив свій же рекорд 2006 року, коли число маленьких бульбашок становило 49. Сему також належать рекорди по надуванню найбільшої, найдовшої, а також найстійкішої мильної бульбашки у світі.
Винахід британських вчених може спричинити революцію в індустрії мийних засобів. До складу мила вони зуміли додати солі, багаті на залізо. Засіб розчиняє бруд, а тоді його можна зібрати - притягуючи магнітами. За допомогою нової розробки сподіваються очищувати води стічних труб. Та найголовніше - винахід допоможе запобігти екологічним катастрофам. Після розливу нафти магнітне мило зможе очистити не тільки водойми, а й їхніх мешканців. Джуліан Істоу, професор хімії Брістольського університету повідомив:-Морські птахи часто страждають від розливів нафти. Їхнє пір'я забруднюється і відчистити його дуже складно. А з допомогою магнітного мила ми з легкістю знімемо увесь бруд з пташиного пір'я. Мило може стати початком серії екологічних чистячих засобів. Крім усього іншого, у магнітного мила є ще один приємний бонус - його можна прикріпити до магнітної мильниці просто так, без всяких залізних вставок.
-
 Мельник Тетянa Юріївна 04.04.2023 в 20:23Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0
Мельник Тетянa Юріївна 04.04.2023 в 20:23Загальна:5.0Структурованість5.0Оригінальність викладу5.0Відповідність темі5.0


про публікацію авторської розробки
Додати розробку


























