Презентація на тему: "Поняття про спирти, карбонові кислоти, жири, вуглеводи. Метанол, етанол, гліцерол: молекулярні і структурні формули, фізичні властивості. Горіння етанолу. Які
Про матеріал
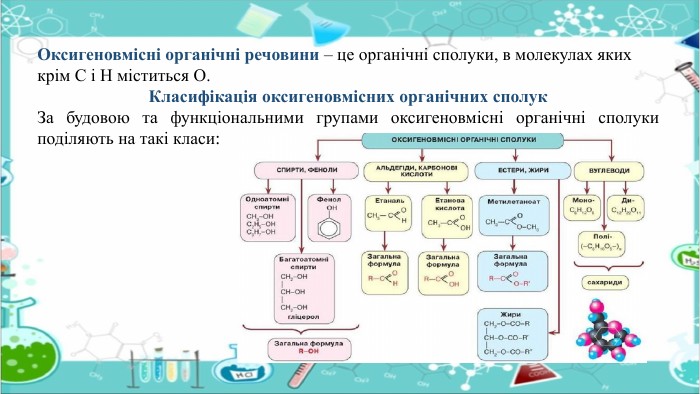
Презентація на тему: "Поняття про спирти, карбонові кислоти, жири, вуглеводи. Метанол, етанол, гліцерол: молекулярні і структурні формули, фізичні властивості. Горіння етанолу. Якісна реакція на гліцерол. Лабораторний дослід №11 «Взаємодія гліцеролу з купрум (ІІ) гідроксидом»" допоможе сформувати знання учнів про склад та властивості насичених одноатомних спиртів та для порівняння гліцеролу, як представника багатоатомних спиртів, поглибити знання учнів про спирти, як оксигеновмісні сполуки, розкрити поняття функціональної групи (на прикладі групи - ОН) її значення. Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку