Презентація до уроку: "Оксиген. Кисень. Фізичні властивості кисню"
Про матеріал
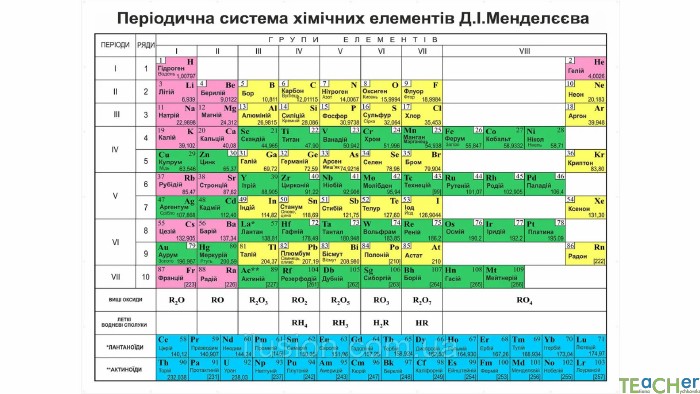
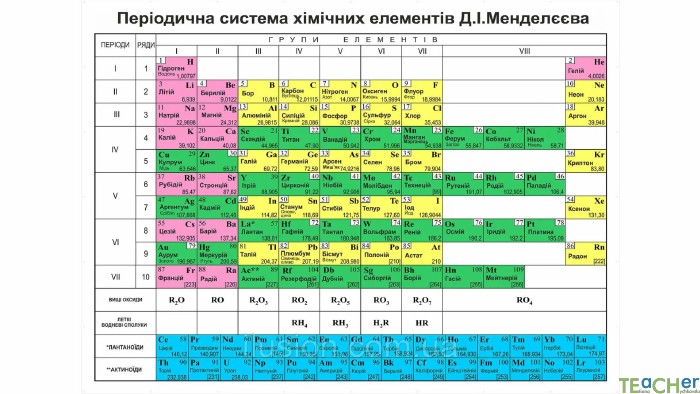
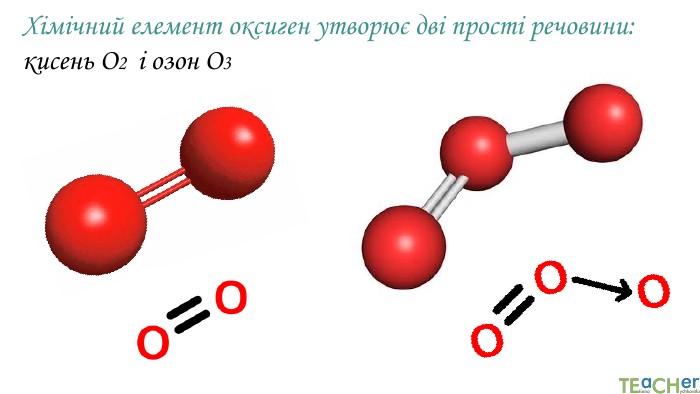
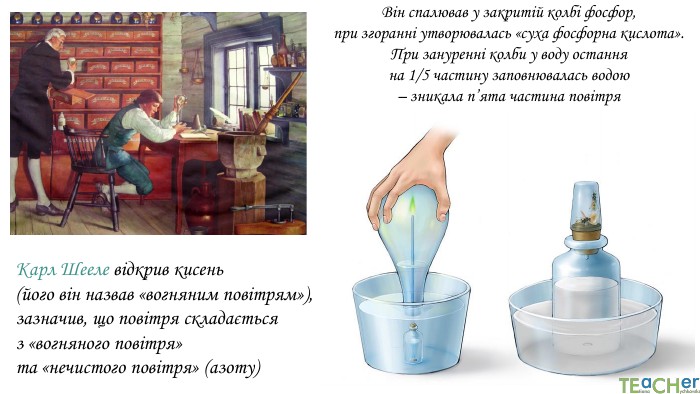
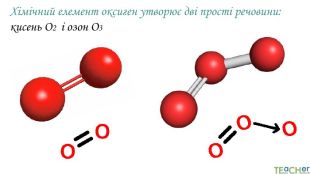
У презентації подано матеріал про значення оксигену, основні відомості про цей елемент, кисень як просту речовину, склад і будову його молекули, фізичні властивості та історію відкриття кисню.
Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
-
-
Дуже дякую!


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку