Презентація до уроку з хімії для 8 класу "Значення періодичного закону. Життя і діяльність Д.І. Менделєєва.


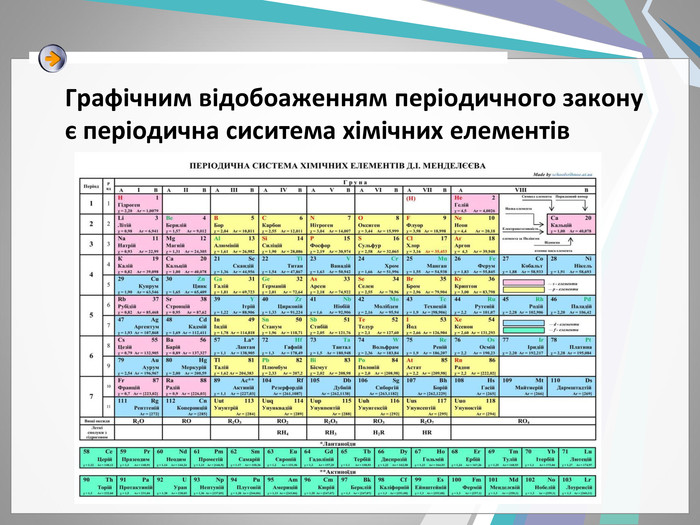













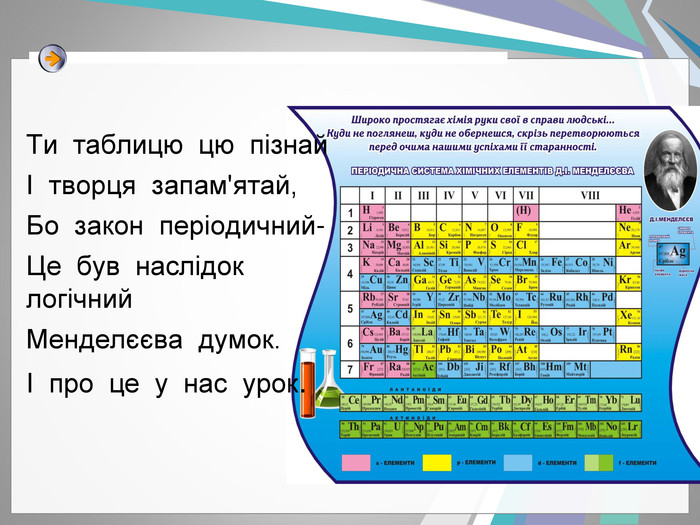



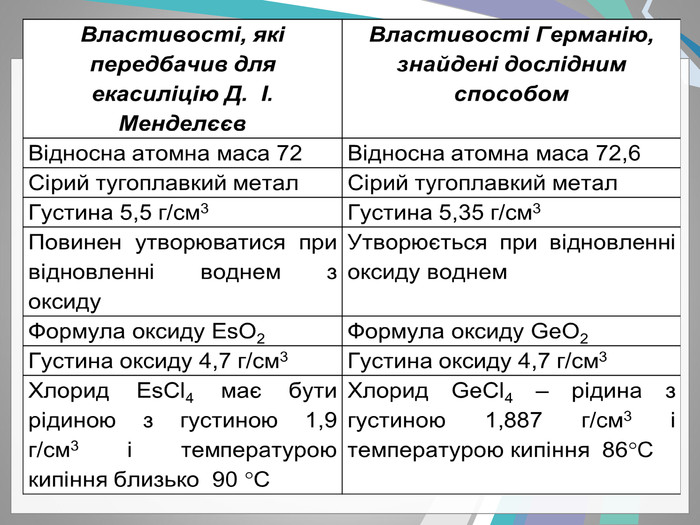

















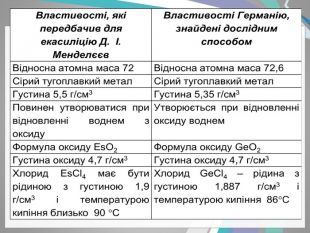
- Д. І. Менделєєв дуже докладно описав властивості трьох ще не відкритих елементів і назвав їх екабором, екаалюмінієм і екасиліцієм. Протягом 15 років ці елементи були відкриті. Першим був відкритий екаалюміній (Лекок-де-Буабодран , француз, 1875). Цей елемент був названий галієм . Другим був відкритий екабор (скандій) (Л. Ф. Нільсон , швед, 1880), потім екасіліцій, названий германієм (К. А. Вінклер, німець,1886). Періодичний закон Д.І. Менделєєва дав можливість передбачити існування на той час ще невідомих хімічних елементів
На основі періодичного закону і періодичної системи вбуло виправлено відносні атомні маси багатьох елементів ( берилію, титану, ітрію, лантану, церію, талію , урану) Наприклад, в той час відносна атомна маса Берилію мала значення 13,5. в такому випадку Берилій мав би знаходитися між Карбоном і Нітрогеном. А це, в свою чергу, порушило би періодичність у зміні властивостей елементів, оскільки метал Берилій розмістився би між двома неметалами. Звідси Менделєєв зробив висновок, що Берилій повинен мати відносну атомну масу проміжну між 7 (Літій) і 11 (Бор). Подальші дослідження це підтвердили.
Д.І.Менделєєв був найбільш визнаним у світі російським ученим – він мав понад ста почесних звань, зокрема був почесним членом майже усіх російських та закордонних академій наук і університетів. Відомий хімік Л.О.Чугаєв так охарактеризував творчість Дмитра Івановича: «Геніальний хімік, першокласний фізик, плодотворний дослідник у галузі гідродинаміки, метеорології, в геології, в різноманітних галузях хімічної технології (вибухові речовини, нафта, вчення про паливо та ін.) й інших дисциплінах, які межують з хімією і фізикою, глибокий знавець хімічної промисловості , оригінальний мислитель»
Перевірте свої знання: 1. Виберіть сучасне формулювання Періодичного закону А Властивості хімічних елементів і утворених ними сполук перебувають у періодичній залежності від атомної маси Б Властивості хімічних елементів і утворених ними сполук перебувають у періодичній залежності від атомної ваги В Властивості хімічних елементів і утворених ними сполук перебувають у періодичній залежності від заряду ядра атома Г Властивості хімічних елементів і утворених ними сполук перебувають у періодичній залежності від електронегативності.
7. Як змінюється склад електронної оболонки атомів хімічних елементів 3-го періоду періодичної системи Д.І. Менделєєва зі зростанням протонного числа? А збільшується число енергетичних рівнів Б зменшується число енергетичних рівнів В зменшується число електронів на зовнішньому енергетичному рівні Г збільшується число електронів на зовнішньому енергетичному рівні
10. Чому Сульфур і Хром розташовано в одній групі періодичної системи елементів Д.І. Менделєєва А атоми Сульфуру і Хрому мають однакове число валентних орбіталей Б атоми Сульфуру і Хрому мають однакове число валентних електронів В атоми Сульфуру і Хрому мають однакове число енергетичних рівнів Г Сульфур і Хром мають однакову валентність за Гідрогеном


про публікацію авторської розробки
Додати розробку




































-

Чоп Наталя
07.11.2023 в 08:47
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Крамар Світлана
12.10.2023 в 20:31
дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Ivanenko Olena
09.10.2022 в 12:58
Все чудово.
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Тодоров Леонід
04.11.2021 в 18:23
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Сороквашина Тетяна
28.09.2021 в 23:05
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 2 відгука