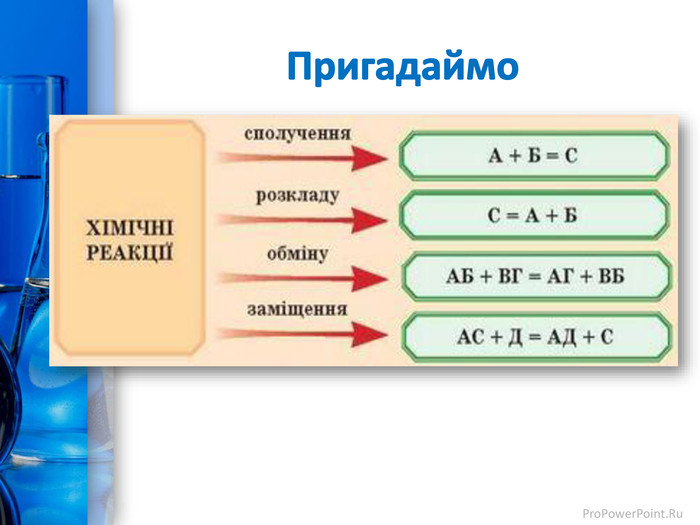
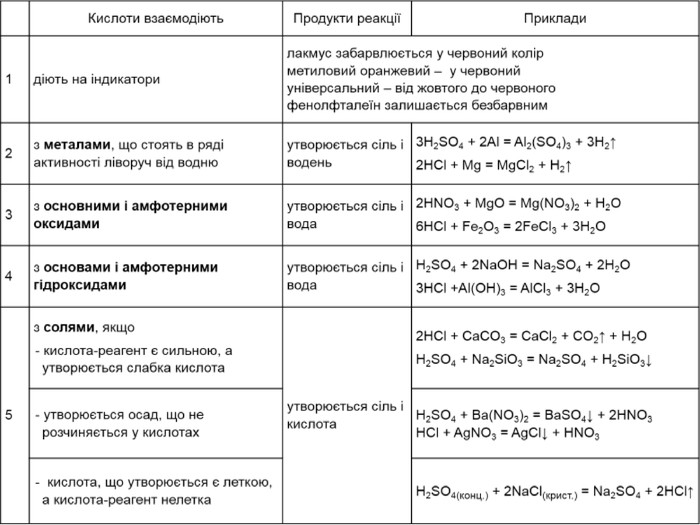
Презентація "Фізичні та хімічні властивості кислот"
Про матеріал
Формування ключових компетентностей:
а) саморозвитку й самоосвіти – створення проблемних ситуацій, уміння знаходити нові рішення;
б) інформаційної – розуміння та усвідомлення отриманої інформації, вміння робити висновки та узагальнення, складання опорних схем;
в) здоров’язбережувальної – вміння поводитися з хімічними речовинами, піклуватися про своє життя і здоров'я. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Гарна робота! Дякую!
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку