Презентація "Хімічні властивості лугів та основ"
Про матеріал
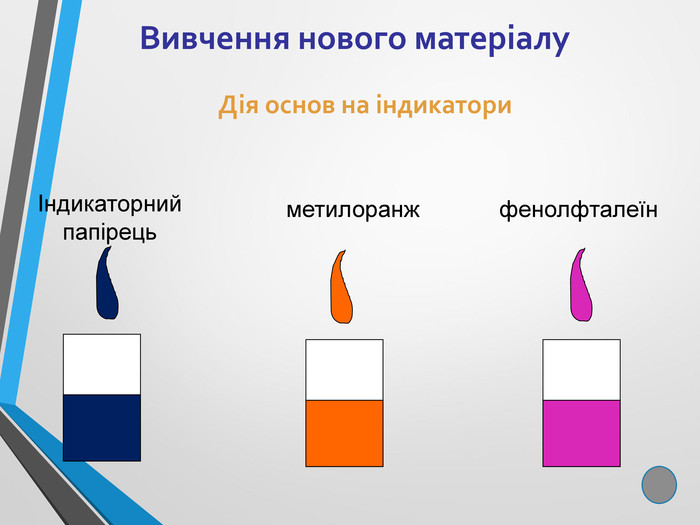
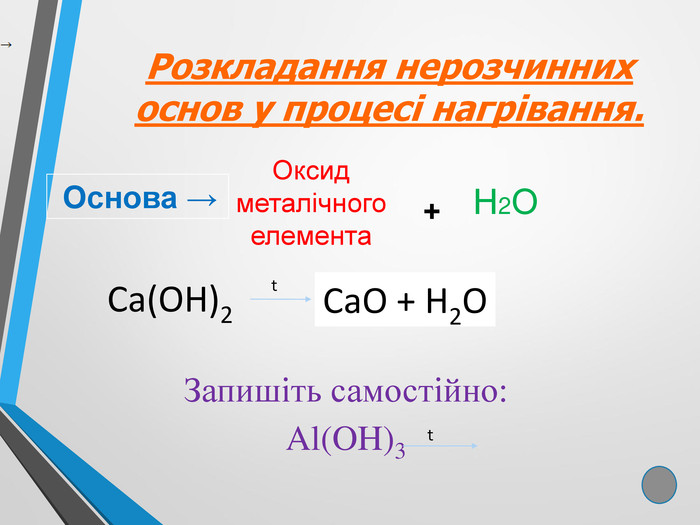
Презентація до уроку хімії у 8 класі "Хімічні властивості основ і лугів" Осно́ви - це складні речовини, утворені металічним елементом та гідроксидними групами (OH). Хімічні властивості основ визначаються їх відношенням до кислот, амфотерних оксидів і солей. Найбільш характерною властивістю основ є їх здатність вступати в хімічні реакції з кислотами. Причому з кислотами взаємодіють як розчинні, так і нерозчинні основи. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку























-

Чоп Наталя
17.05.2023 в 10:09
Дякую!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Фельді Віталій Йожефович
01.03.2023 в 17:21
Молодчинка!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Озірна Інна Миколаївна
23.02.2023 в 11:45
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Міщенко Галина Миколаївна
19.02.2023 в 12:38
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Проценко Ніна Іванівна
17.03.2022 в 16:38
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 2 відгука