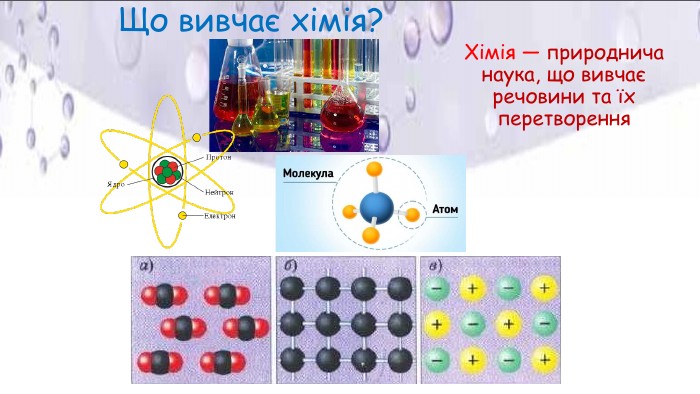
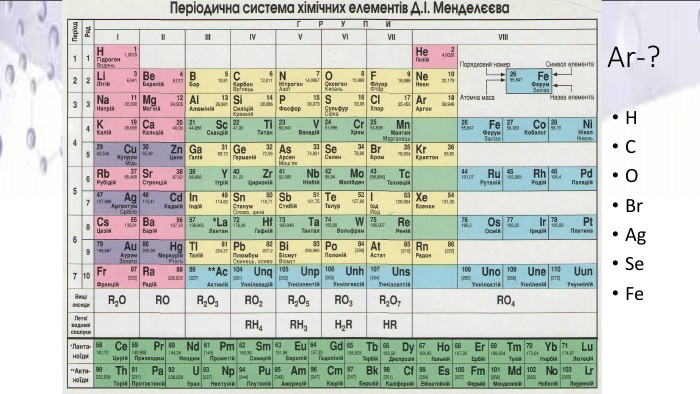
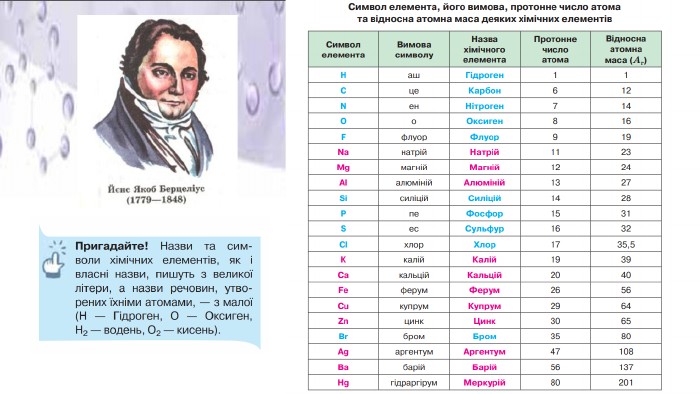
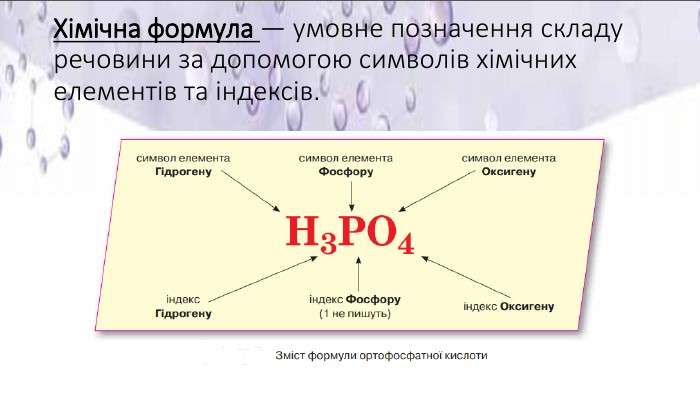
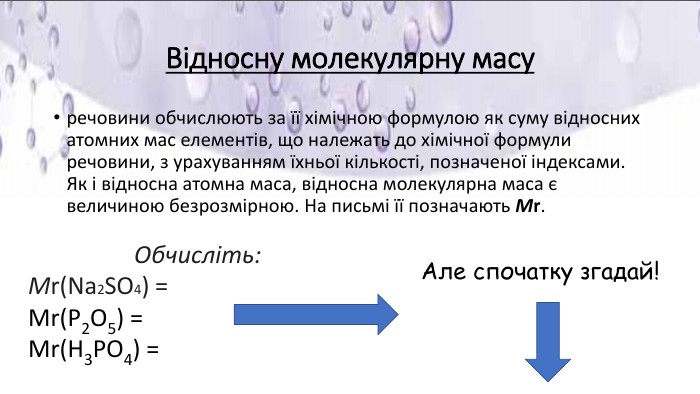
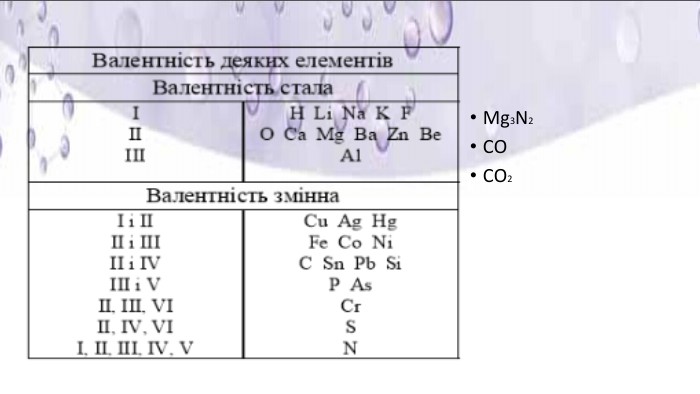
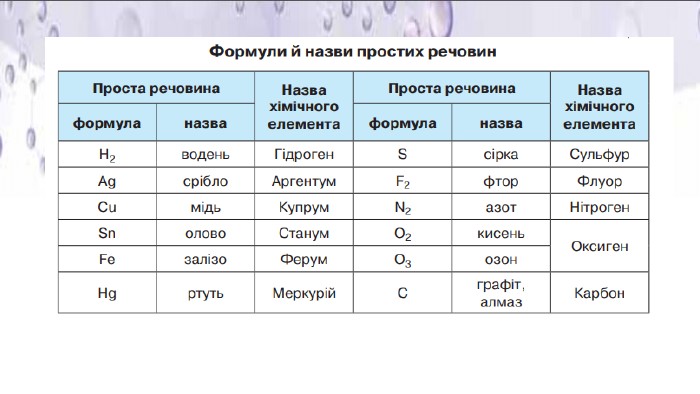
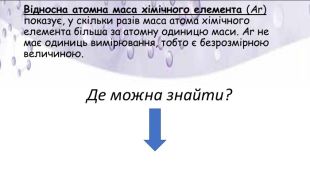
Презентація "Хімічний елемент, речовина. Хімічна формула"
Про матеріал
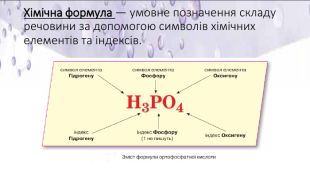
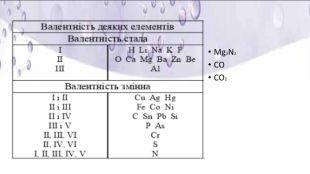
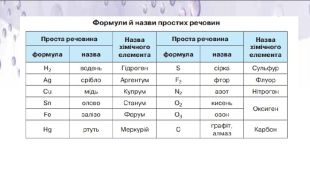
Презентація "Хімічний елемент, речовина. Хімічна формула" складена для супроводу дистанційного уроку з Хімії 8 клас за підручником О.Г. Ярошенко (2021р.). Перегляд файлу
Зміст слайдів

Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку