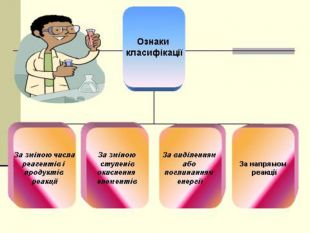
Презентація "Класифікація хімічних реакцій за різними ознаками"
Про матеріал
закріпити і поглибити одержані раніше знання про типи хімічних реакцій;
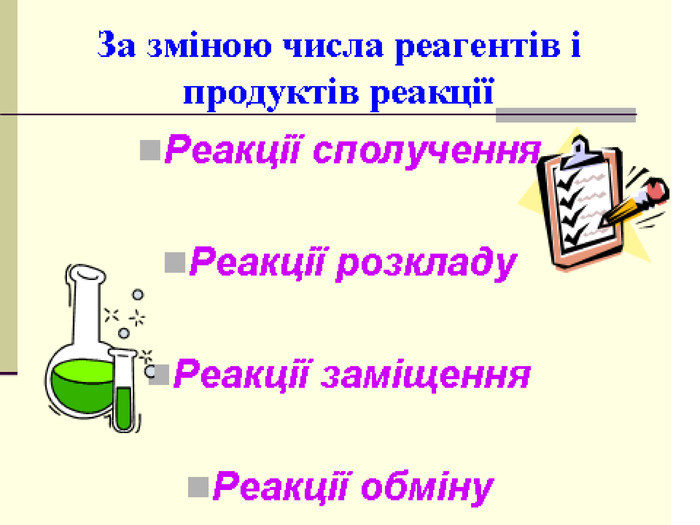
► Навчитись розрізняти реакції сполучення, розкладу, заміщення, обміну;
►продовжити формувати уміння класифікувати хімічні реакції за кількістю і складом речовин, що взаємодіють, чи утворюються в результаті реакції, та складати реакції різних типів;
►комплексно розвивати всі компоненти мислення, уміння застосовувати набуті знання і навички на практиці;
►виховувати ціннісне ставлення до власного здоров’я, культуру мовлення, ініціативність,патріотизм, екологічну культуру.
завдання уроку:Складання хімічних реакцій за схемою перетворень:
визначення типу хімічної реакції;
вказати окисник і відновник у ОВР;
методом електронного балансу розставити коефіцієнти;
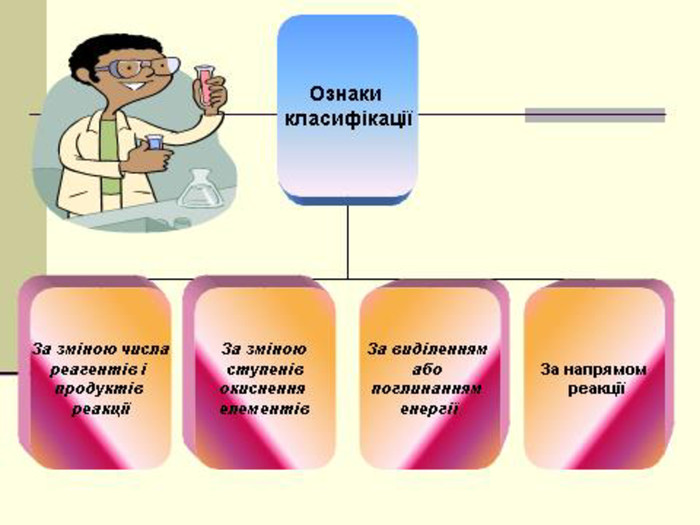
складання схеми “ Класифікація хімічних реакцій за різними ознаками;
Розв’язування задач;
Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку