Презентація до уроку з хімії 9 кл. Реакції йонного обміну
Про матеріал
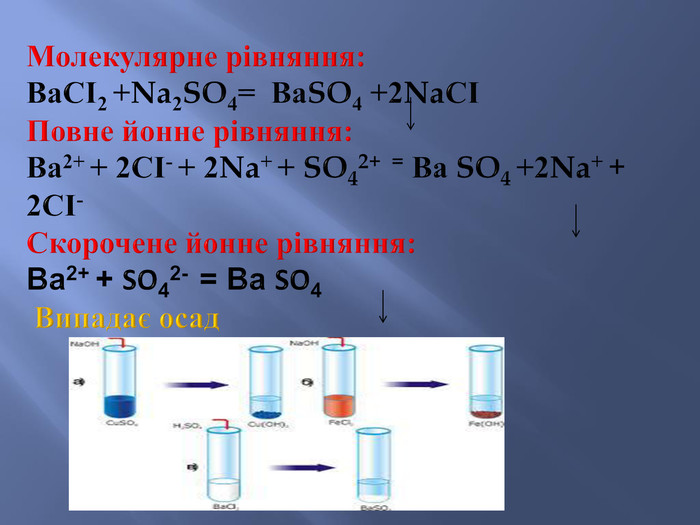
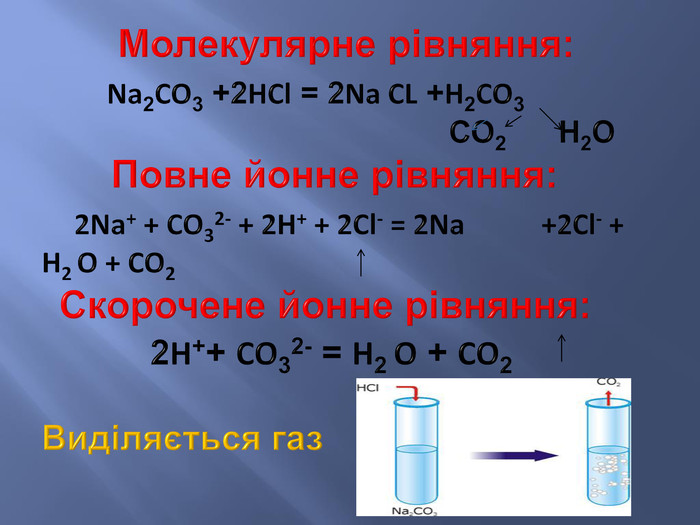
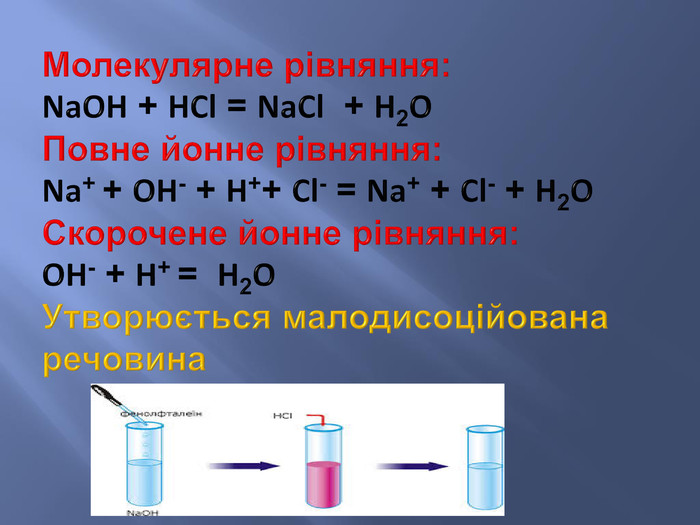
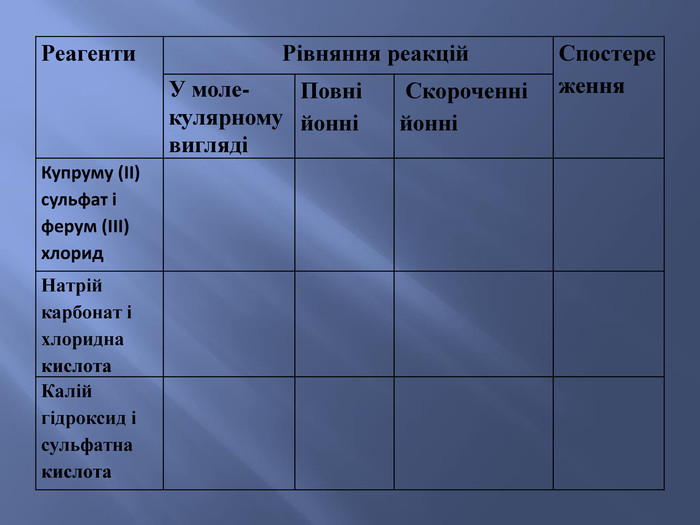
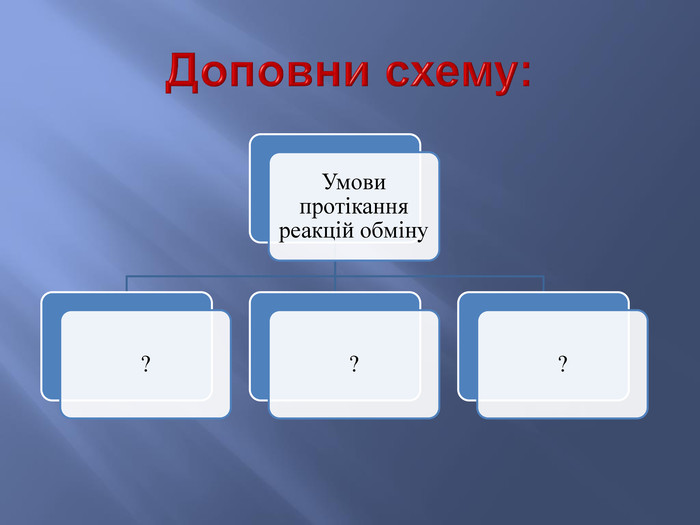
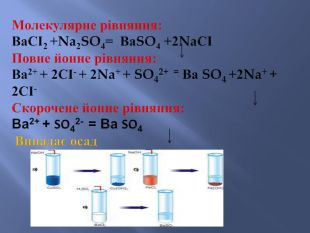
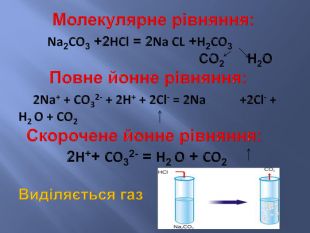
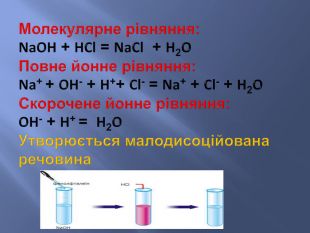
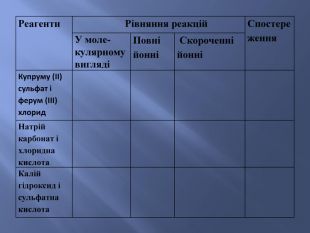
Презентація до уроку з хімії у 9 класі на тему: "Реакції йонного обміну". Після ознайомлення з темою учні вмітимуть: складати рівняння реакції обміну у повній та скороченій йонній формах; розрізняти катіони і аніони; -пояснювати суть реакцій йонного обміну з позиції електролітної дисоціації.
Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку