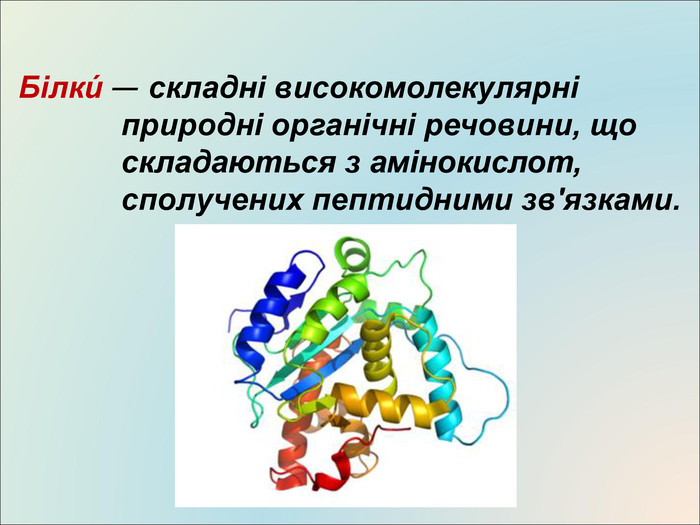
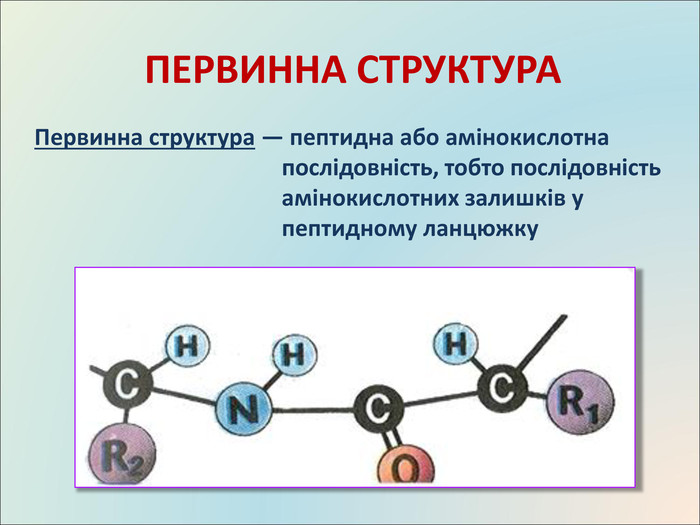
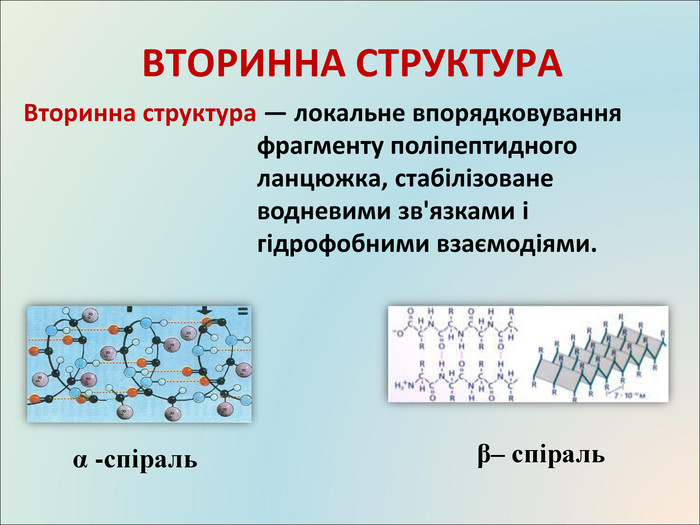
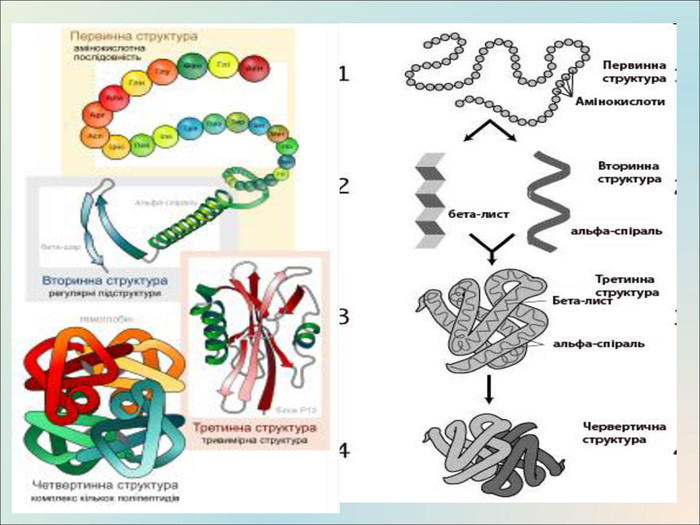
Презентація на тему "Білки: склад і властивості"
Про матеріал
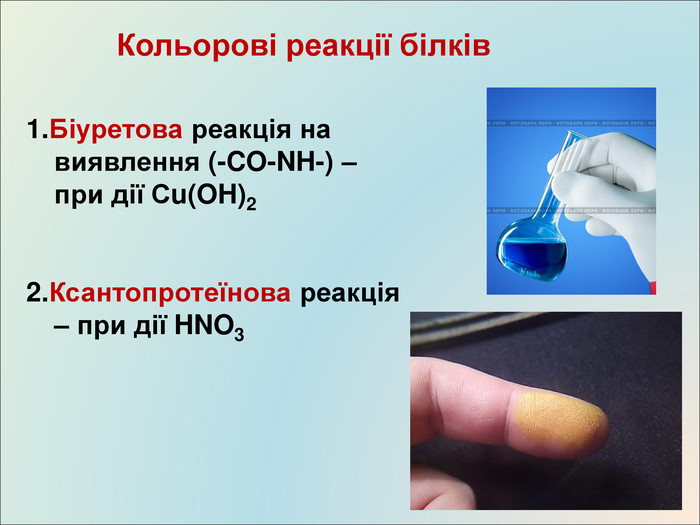
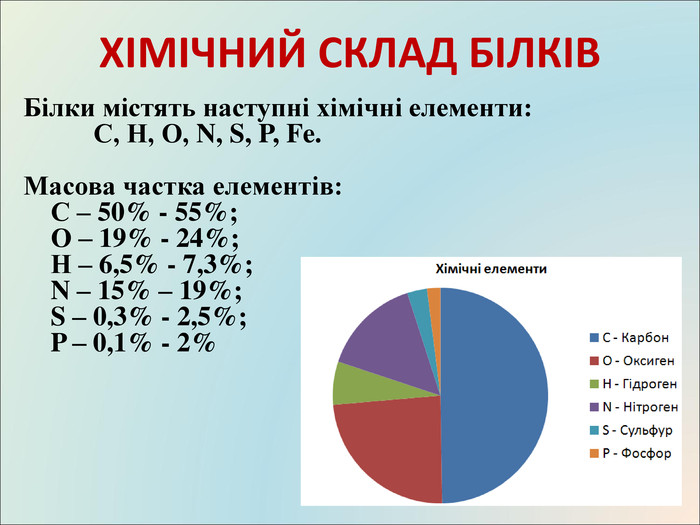
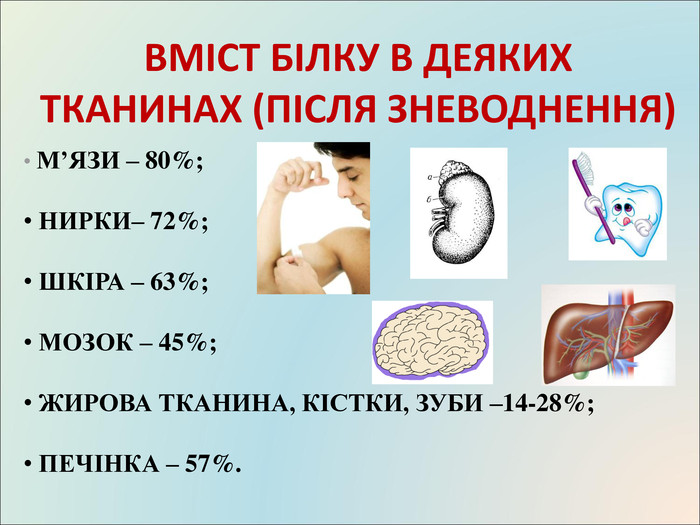
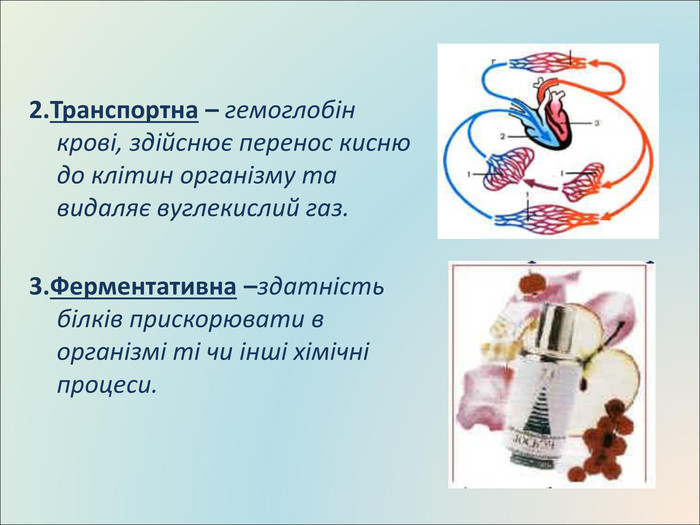
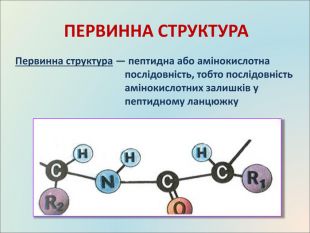
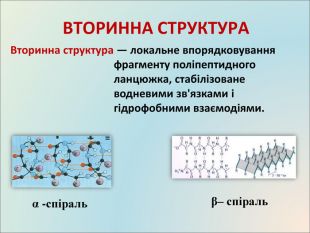
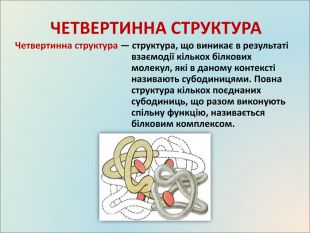
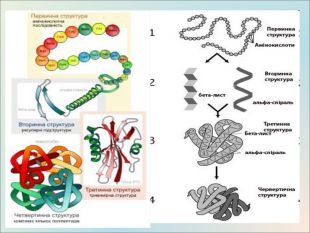
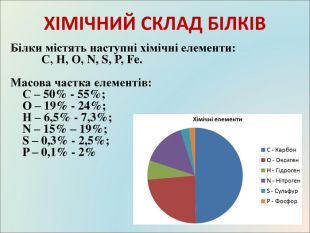
Презентація до уроку, містить матеріали про білки, склад, структуру, якісні реакції Перегляд файлу
Зміст слайдів


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку