Презентація "Солі жирних кислот. Мило."
Про матеріал
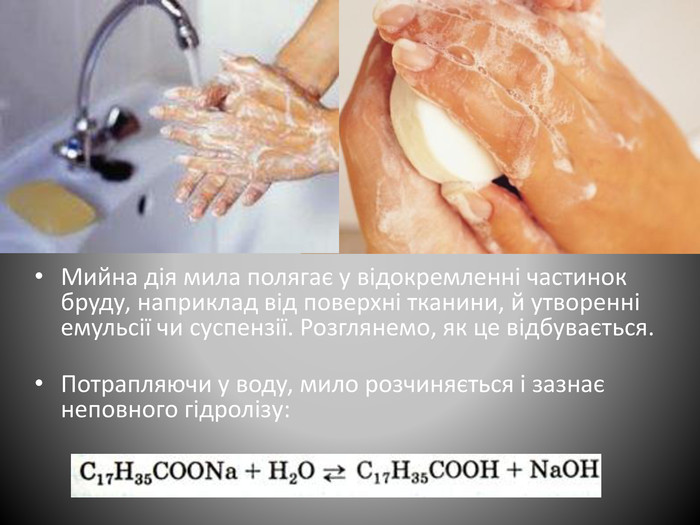
Презентація "Солі жирних кислот. Мило."
Процес виготовлення і застосування мила .
Синтетичні мийні засоби.
Перегляд файлу
Зміст слайдів
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку