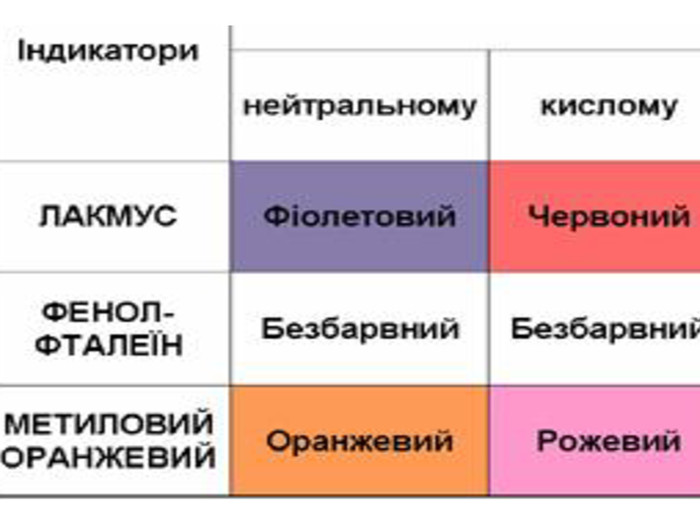
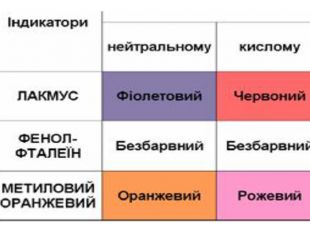
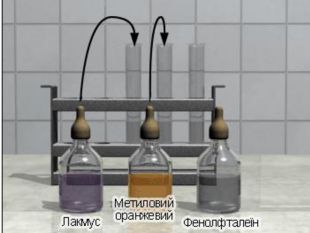
Презентація Тема " Хлоридна кислота : властивості, добування і застосування"
Про матеріал
познайомити учнів з хімічними властивостями кислот на прикладі хлоридної кислоти Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку