Презентація «Валентність та ступінь окиснення» 9 клас
| Презентація допоможе провести урок на тему «Ступінь окиснення. Визначення ступеня окиснення елемента за хімічною формулою сполуки. Складання формули сполуки за відомими ступенями окиснення елементів». |














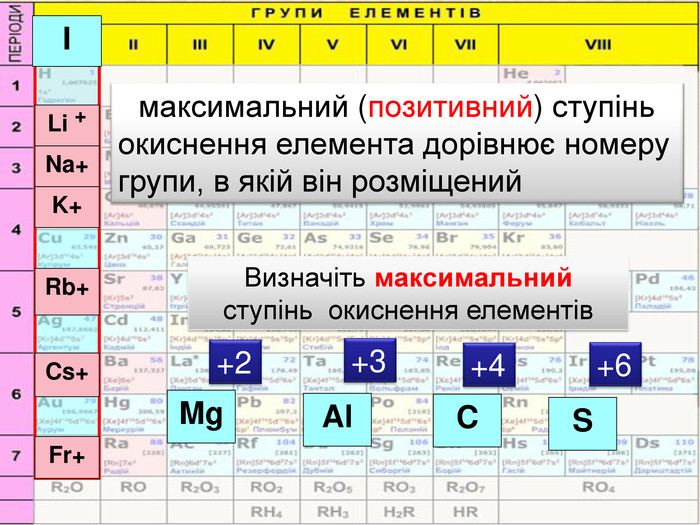
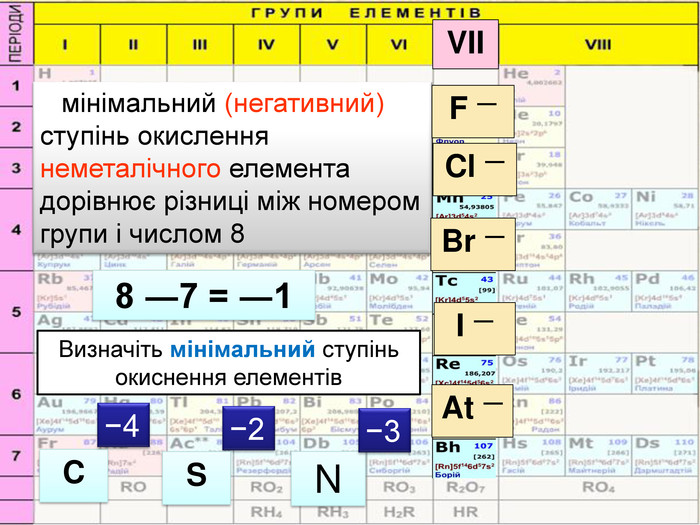








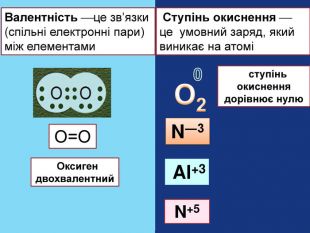
Валентність. Ступіньокиснення Визначається числом спільних електронних пар, що утворюють хімічний звязок Визначається числом відданих або приєднаних електронів Числове вираження не має знака Може мати нульове значення. Не має значення 0 (нуль) Числове значення може бути позитивним або негативним
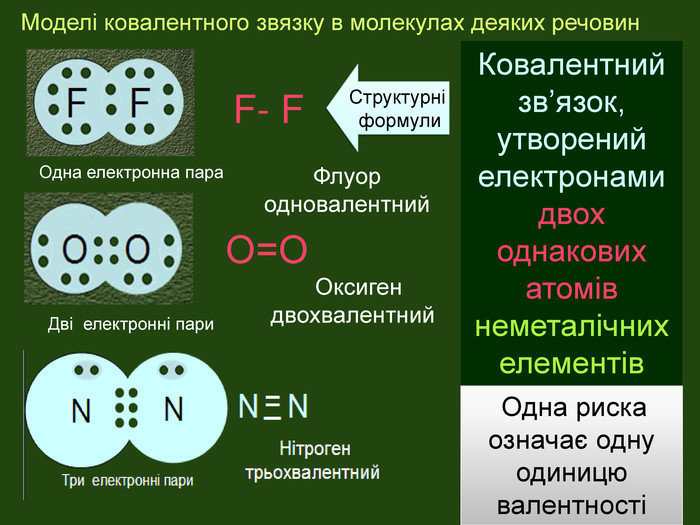
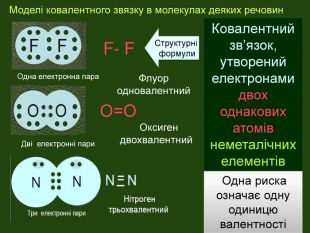
Моделі ковалентного звязку в молекулах деяких речовин. F- FО=ООдна електронна пара. Дві електронні пари. Структурні формули Оксиген двохвалентний. Флуор одновалентний. Ковалентний зв’язок, утворений електронами двох однакових атомів неметалічних елементів Одна риска означає одну одиницю валентності
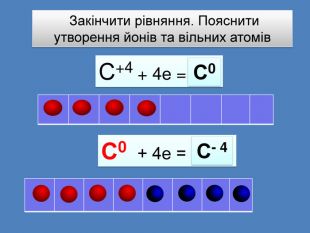
Cтупінь окиснення Карбону С+4 (плюс чотири); Приклад: Яку валентність та ступені окиснення мають атоми в сполуці СCl4 ?Сl↑ Cl←С+4→Cl↓Cl. Напрям стілочок показує, що атом Карбону віддав свої електрони атомам Хлору, набувши позитивного ступеня окиснення плюс 4. Валентність Карбону 4 (чотири спільні електронні пари з атомом Хлору). ССl4+4 ─
Cтупінь окиснення Карбону С-4 (мінус чотири); Приклад: Яку валентність та ступені окиснення мають атоми в сполуці СН4 ?Н↓ Н→С ─4←Н↑ННапрям стілочок показує, що атом Карбону прийняв 4 електрони, набувши негативного ступеня окиснення мінус 4. Валентність Карбону 4 (чотири спільні електронні пари з атомом Гідрогену). СН4-4 +
Nа0 Число над знаком хімічного елемента називається ступінь окиснення. ступінь окиснення вказує на кількість відданих чи приєднаних електронів В даному випадку ступінь окиснення― ноль. Це означає, що атом електронейтральній, тобто в наявності всі електрони. Nа+ В цьому випадку ступінь окиснення ― плюс один (одиниця не пишеться) Це означає, що атом “віддав” один електрон, перетворившись на позитивно заряджений йон катіон
Li0 Як називається число над знаком? На що вказує ступінь окиснення ? в даному випадку ступінь окиснення― ноль. Що це означає? Li+ Прокоментуйте цей випадок. Що це означає ?Число над знаком хімічного елемента називається ступінь окиснення. ступінь окиснення вказує на кількість відданих чи приєднаних електронів Це означає, що атом електронейтральній, тобто в наявності всі електрони. В цьому випадку ступінь окиснення ― плюс один (одиниця не пишеться) Це означає, що атом “віддав” один електрон, перетворившись на позитивно заряджений йон катіон
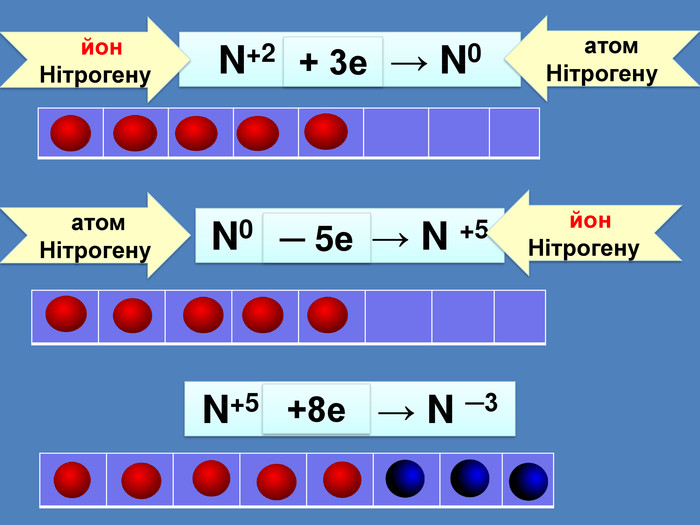
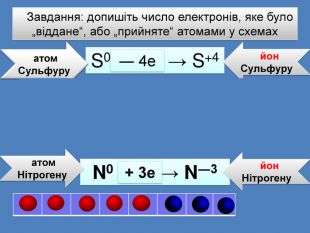
Йони ― це електрично заряджені частинки речовини, що утворилися з атомів або атомних груп внаслідок втрати або приєднання до них електронів S+6 К+ Al+3 катіони Атоми, які втратили електрони та перетворилися на позитивно заряджені йони S ―2 C―4 N―3 аніони Атоми, які приєднали електрони та перетворилися на негативно заряджені йони
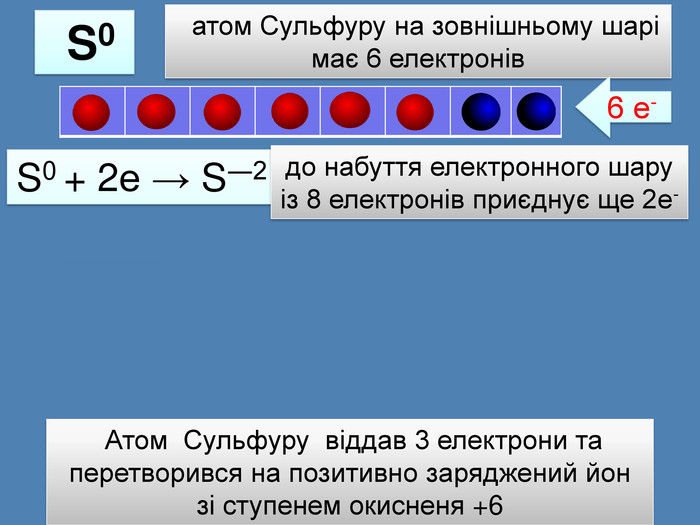
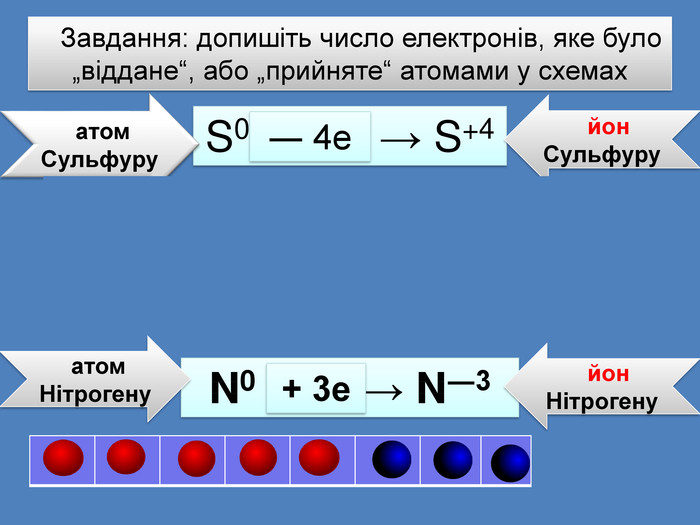
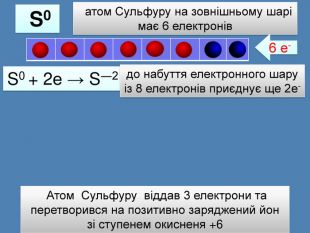
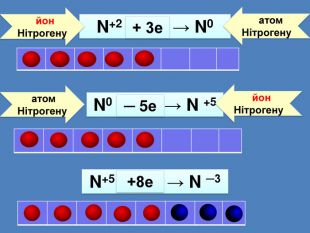
атом Сульфуру на зовнішньому шарі має 6 електронів S0 {21 E4 AEA4-8 DFA-4 A89-87 EB-49 C32662 AFE0}S0 + 2е → S―2 S0 {21 E4 AEA4-8 DFA-4 A89-87 EB-49 C32662 AFE0}++++++S0 ― 6е → S+6 Атом Сульфуру віддав 3 електрони та перетворився на позитивно заряджений йон зі ступенем окисненя +66 е-до набуття електронного шару із 8 електронів приєднує ще 2е-
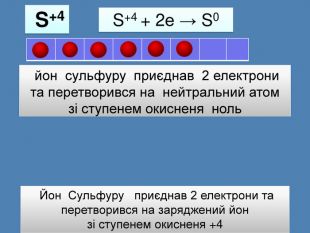
S+4 {21 E4 AEA4-8 DFA-4 A89-87 EB-49 C32662 AFE0}++S+4 + 2е → S0 йон сульфуру приєднав 2 електрони та перетворився на нейтральний атомзі ступенем окисненя ноль S+6 {21 E4 AEA4-8 DFA-4 A89-87 EB-49 C32662 AFE0}++++++S+6 + 2е = S+4 Йон Сульфуру приєднав 2 електрони та перетворився на заряджений йон зі ступенем окисненя +4
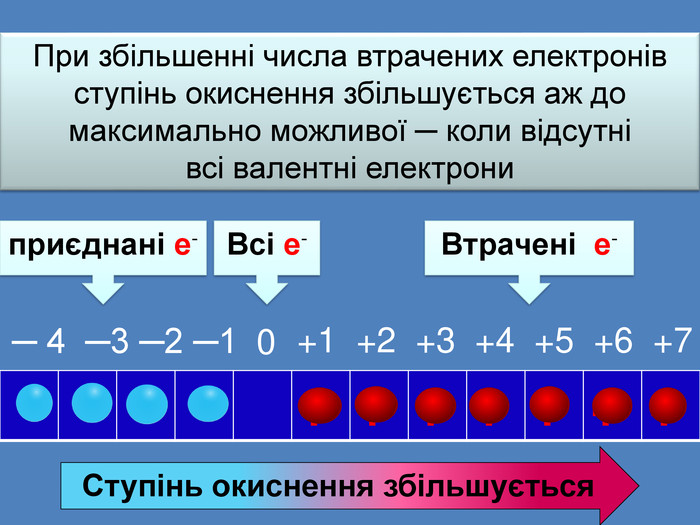
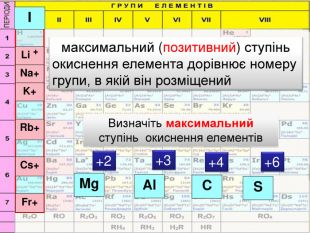
При збільшенні числа втрачених електронів ступінь окиснення збільшується аж до максимально можливої ─ коли відсутні всі валентні електрони {5 C22544 A-7 EE6-4342-B048-85 BDC9 FD1 C3 A}+++++++Всі е-+1 +2 +3 +4 +5 +6 +7 Втрачені е-приєднані е-─ 4 ─3 ─2 ─1 0 Ступінь окиснення збільшується
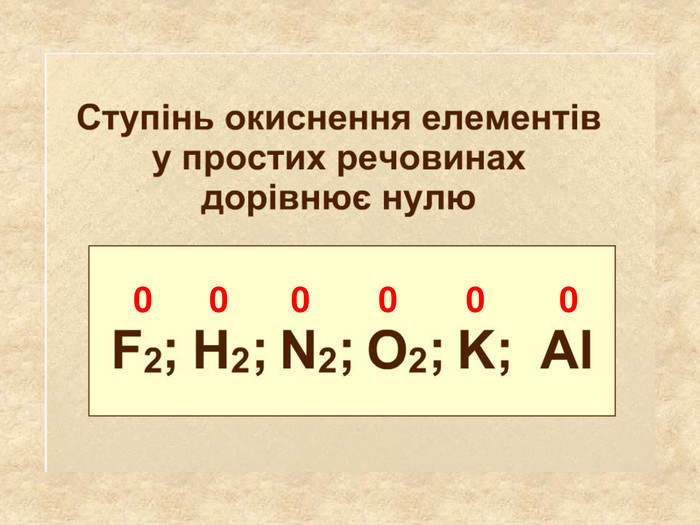
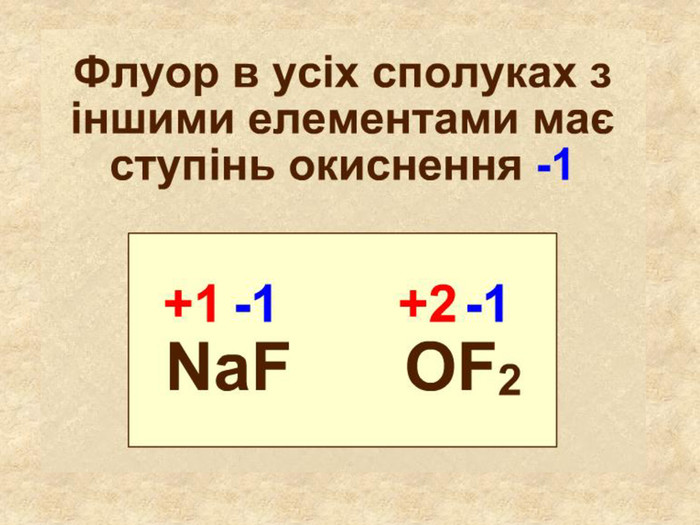
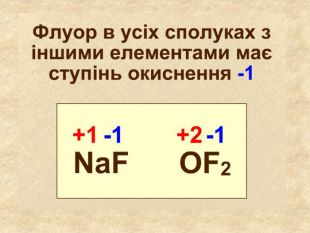
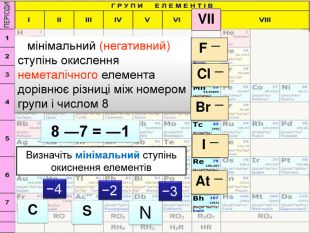
Визначення ступенями окисненя Елементи в сполуках мають такий ступінь окиснення: Оксиген має характерний ступінь окиснення -2 Наприклад: О–2 Флуор, Хлор має характерний ступінь окиснення -1. Наприклад: Сl Йони мають ступінь окиснення OH— Cl— NO—3 SO4 — 2 CO3 — 2 Si. O3 — 2 PO4 — 3 Атоми простих речовин електронейтральні. Їх ступінь окиснення дорівнює нулю. Наприклад: Сl02 ; О02; Н02
Елементи в сполуках мають такий ступінь окиснення: Металічні елементи у сполуках з неметалічними завжди мають позитивний ступінь окиснення. Наприклад: Na+; Ba+ 2; Ca + 2; Al3+; Неметалічні елементи у сполуках з металічними завжди мають негативний ступінь окиснення. Наприклад: C–4 ; Сl ; S 2; N 3 Гідроген у сполуках з металічними елементами має негативний ступінь окиснення H– (мінус один), а з неметалічними— позитивний +1 Наприклад: Н+Сl
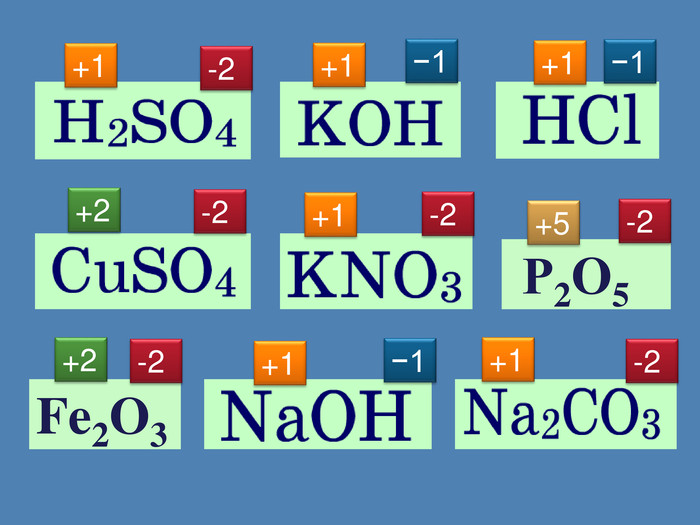
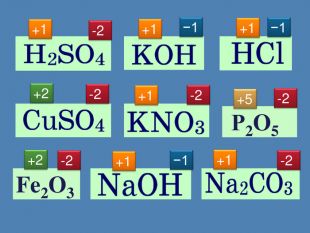
Визначення ступеня окиснення. H2 SO42·4 = 81· 2 = 2-2 +6 ? Завдання: Визначити ступінь окиснення атомів у споуках. HNO3 Mg. SO4 H3 PO4 Na2 SO4-2 +5 -2 -2 + +7 +6 +5 + КСl. O3 HPO3 KСl. O4 КMn. O4+ + +5 +7 -2 -2 -2 + ─8 +2 +6 +8 2+6 = 8ступінь окиснення всіх атомів Оксигену ─8 (мінус вісім)ступінь окиснення всіх атомів Гідрогену+2 (плюс два) +8─8 =0+ + +2-2 +6 -2 + +5
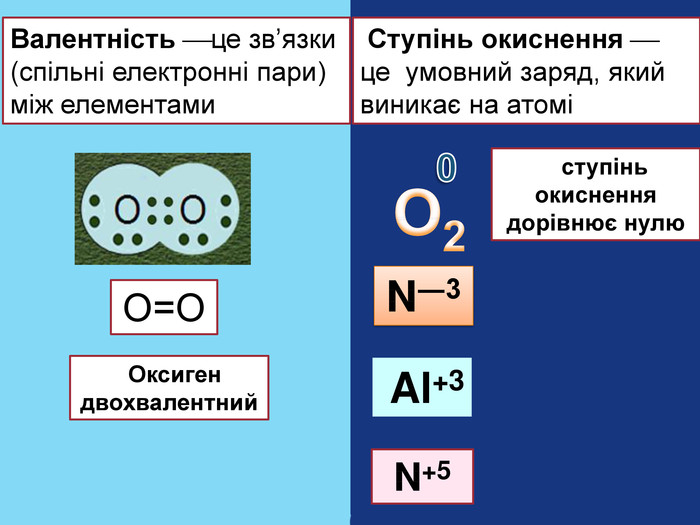
Валентність це зв’язки (спільні електронні пари) між елементами Таким чином, за однакових значень валентності елемент може мати різний ступінь окислення як за знаком так і за значенням. Ступінь окиснення і валентність — родинні поняття. У багатьох сполуках абсолютна величина ступеня окиснення елементів співпадає з їх валентністю. Однак існує багато випадків, коли валентність відрізняється від ступеня окиснення. Ступінь окиснення це умовний заряд, що виникає на атомі в результаті приєднання чи віддачі електронів. Підсумки
Складання формул за ступенями окисненя. NON2 O5 3. Поділимо його на ступінь окиснення кожного атома та знайдемо індекси: для Нітрогену 10 : 5 =2 для Оксигену 10 : 2 = 5 1. Записати ступені окиснення над символами елементів+5 -2 2. Знайти найменше спільне кратне модулів ступенів окиснення НСК =10 105102 Na CO3 Zn SO4 Mg (NO3) Al (SO4) Завдання: Скласти формули сполук. Ca. Cl Н S С Н SO+2 +2 +2 +3 + + + -2 -2 -2 -2 -2 ─ 2 2 2 2 2 2 ─ 4 3 4 + 4 ─
Григорович О. В. Хімія: підруч. для 9 класу загальноосвіт. навч.закл./ О. В. Григорович .̶ Харків: Вид-во «Ранок», 2017 Шаповалов С. А. Хімія. Довідник старшокласника та абітурієнта. Харків. Торсінг, 2005. Строойтова І. Ю. Усі уроки імії. 9 клас ̶ Х.: вид. група «Основа», 2009 Абрамович С.І. Левитська О. В. Хімія. Розвязування задач, відповіді на питання, підказки до практичних робіт до підручника Н. М. Буринської Харків: Веста 2002 Джерела


про публікацію авторської розробки
Додати розробку























-

Димарєва Лілія
11.09.2023 в 12:48
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Теребіленко Людмила Володимирівна
04.06.2023 в 13:53
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Попова Валентина
28.11.2022 в 13:35
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Шепета Людмила Юріівна
08.11.2021 в 09:20
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 1 відгук