Презентація «Відносна молекулярна маса» (виправлена та доповнена) 7 клас
Про матеріал
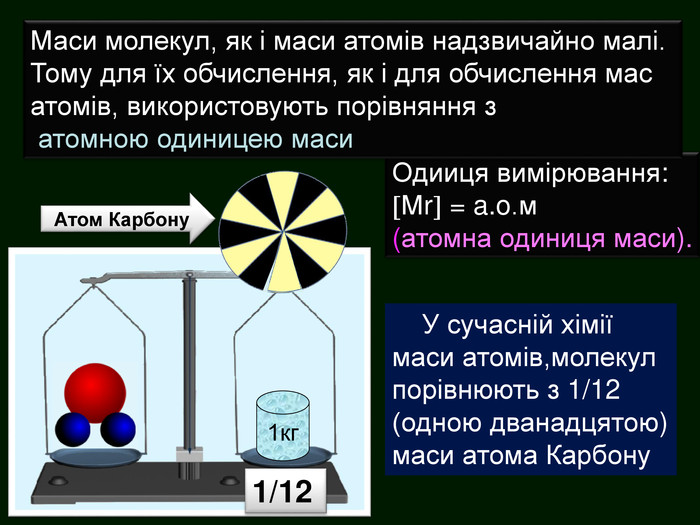
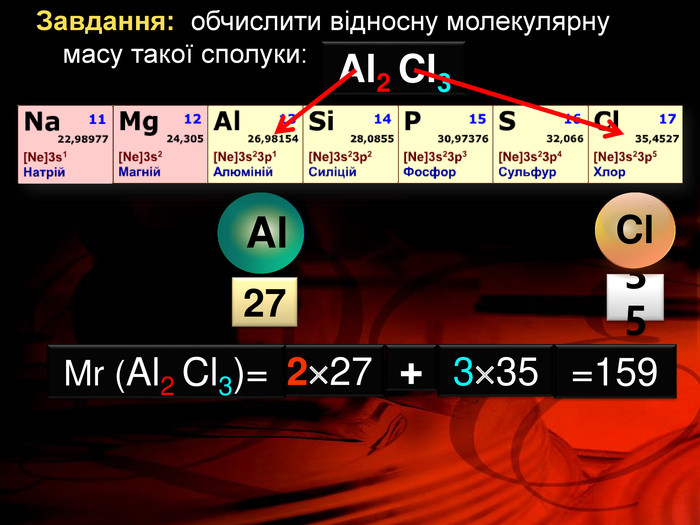
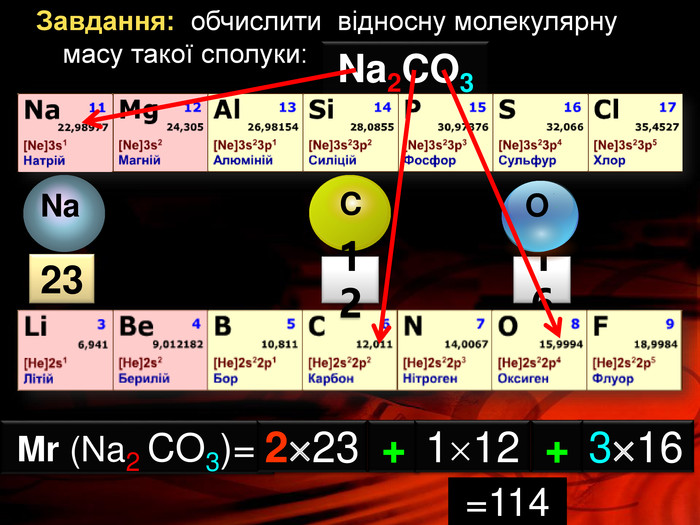
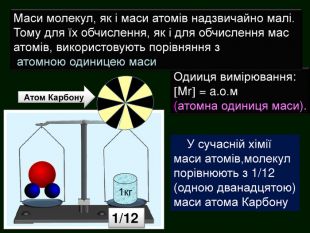
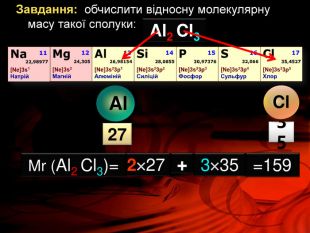
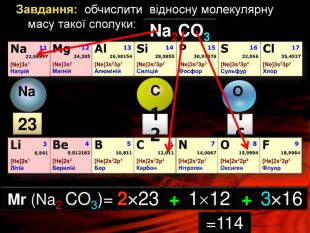
Презентація «Відносна молекулярна маса» допоможе вчителю та учням якісно засвоїти тему. Вміщені приклади обчислення відносної молекулярної маси сполук. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку





























-

Шубіна Вікторія Вікторівна
01.04.2024 в 20:44
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Товстолес Лариса
27.10.2021 в 07:45
дякую. чудова робота
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Kiriyenko Olena
04.01.2021 в 18:30
Дякую за презентацію! Дуже змістовно!
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
-

Буричка Людмила Богданівна
19.11.2020 в 14:07
Загальна:
5.0
Структурованість
5.0
Оригінальність викладу
5.0
Відповідність темі
5.0
Показати ще 1 відгук