Презентація "Явище алотропії"
Про матеріал
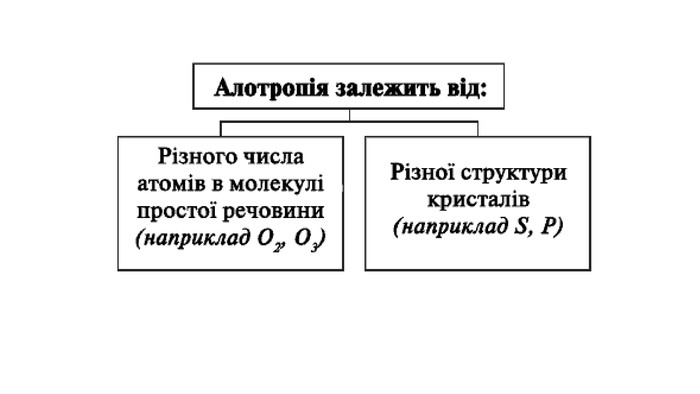
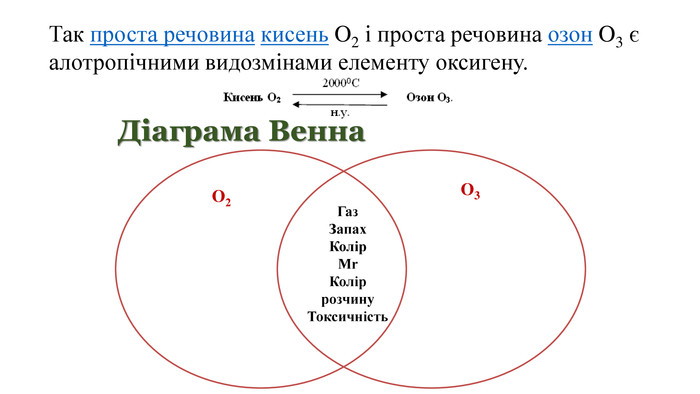
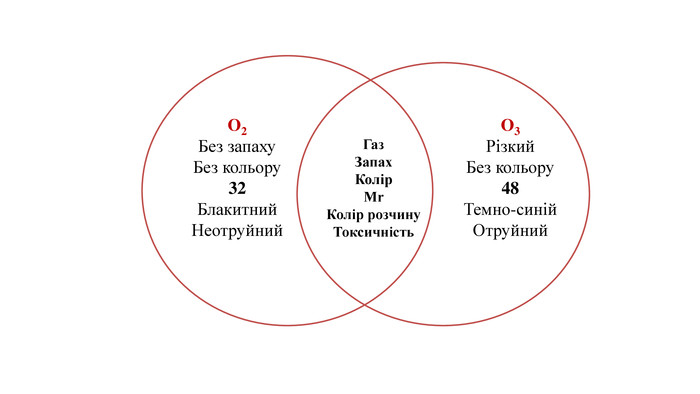
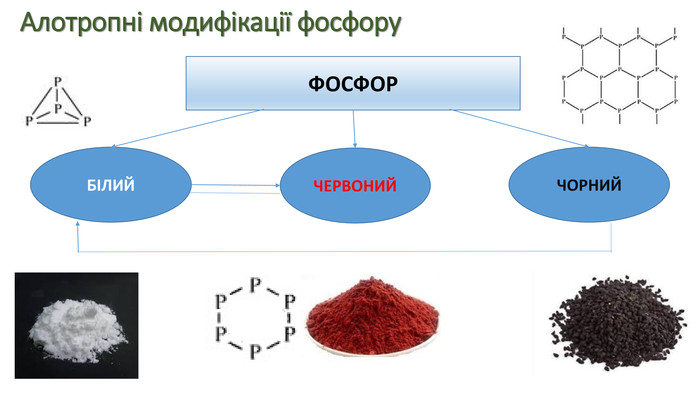
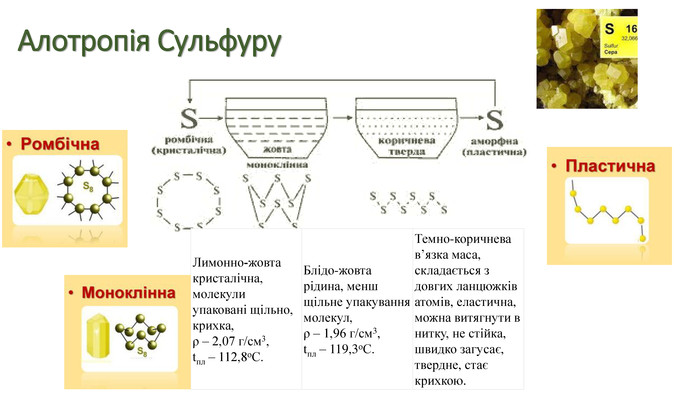
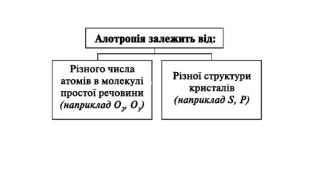
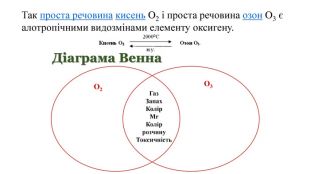
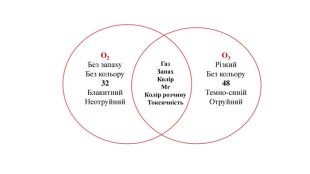
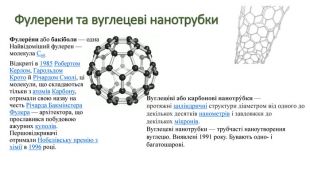
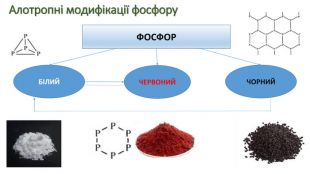
Явище алотропії розкрите на прикладах оксигену, карбону, сульфуру та фосфору. Перегляд файлу
Зміст слайдів
Середня оцінка розробки
Оцінки та відгуки
-
Дякую
pptx
Оцінка розробки


Безкоштовний сертифікат
про публікацію авторської розробки
про публікацію авторської розробки
Щоб отримати, додайте розробку
Додати розробку